Revista Veterinaria. 2026; 37(1)
https://doi.org/10.30972/vet.3719049
Artículo Original




1Cátedra de Virología, Laboratorio de Virología, Centro de Microbiología Básica y Aplicada (CEMIBA), Facultad de Ciencias Veterinarias, Universidad Nacional de La Plata (FCV-UNLP), La Plata, Buenos Aires, Argentina.
2Actividad Privada.
3Consejo Nacional de Investigaciones Científicas y Técnicas (CONICET), Centro Científico Tecnológico (CCT), La Plata, Buenos Aires, Argentina.
 willimanmacarena@gmail.com
willimanmacarena@gmail.com sofiozaeta@gmail.com
sofiozaeta@gmail.com jacappuccio@hotmail.com
jacappuccio@hotmail.com meroilucio@gmail.com
meroilucio@gmail.com diegomgoni@gmail.com
diegomgoni@gmail.com saniagocolina5@gmail.com
saniagocolina5@gmail.com germanmetz@fcv.unlp.edu.ar
germanmetz@fcv.unlp.edu.ar gecheverria@fcv.unlp.edu.ar
gecheverria@fcv.unlp.edu.arResumen
La enfermedad de Aujeszky (EA) fue registrada por primera vez en el año 1978 en Argentina y, si bien es endémica en la zona de mayor producción porcina, los casos clínicos han sido esporádicos y con alta frecuencia en establecimientos poco tecnificados. Sin embargo, en 2023, una granja tecnificada de engorde del sudeste de Córdoba, con medidas de bioseguridad controladas y certificada negativa de EA de acuerdo a la normativa de SENASA, presentó un cuadro clínico que comenzó con signos respiratorios. Estos signos aparecieron posteriormente en otras dos granjas de producción intensiva de esta región y 60 días luego de haberse registrado los primeros signos respiratorios, se observaron signos nerviosos en una cuarta granja cercana (unidad productora de lechones). A partir de tejidos se aislaron cepas virales en pulmón y linfonódulo, confirmado y caracterizado molecularmente como Suid Alphaherpesvirus 1. En esta emergencia se comenzó a vacunar con vacuna atenuada gE deleteada. No obstante, varios meses después se registraron nuevamente signos respiratorios en un sitio de engorde cercano. Los análisis moleculares por PCR resultaron positivos a gE, confirmando circulación viral y descartando una reversión vacunal. Las cepas aisladas en este periodo corresponden al genotipo I del virus de Aujeszky, característico de nuestro país y el análisis filogenético demostró su agrupamiento con cepas previamente reportadas, indicando que el virus circula en las granjas de Argentina. El brote ocurrido en esta región podría deberse a deficiencias en las medidas de bioseguridad, sin introducción de nuevas cepas. Este trabajo reporta además el primer aislamiento viral a partir de muestras de pulmón y linfonódulo de animales de engorde con signos respiratorios.
Palabras clave: Suid Alphaherpesvirus 1, Enfermedad de Aujeszky, aislamiento viral, brote, caracterización molecular, producción porcina.
Abstract. Aujeszky's disease (AD) was first recorded in Argentina in 1978 and, although it remains endemic in the country's main pig-producing region, clinical cases have generally been sporadic and mostly confined to low-technology farms. However, in 2023, a technologically advanced finishing farm in southeastern Córdoba, operating under controlled biosecurity conditions and certified AD-free according to SENASA regulations, presented a clinical outbreak that initially manifested with respiratory signs. Similar symptoms subsequently appeared in two additional intensive production farms in the same region, and 60 days after the first respiratory cases, neurological signs were observed in a nearby piglet production unit. Viral strains were isolated from lung and lymph node tissues and confirmed, through molecular characterization, as Suid Alphaherpesvirus 1. During this emergency, vaccination with a gE-deleted attenuated vaccine was implemented. Nevertheless, several months later, respiratory signs reappeared in a nearby finishing facility. PCR molecular analyses were positive for gE, confirming viral circulation and ruling out vaccine reversion. The isolates obtained during this period belonged to genotype I of the Aujeszky´s disease virus, the genotype historically circulating in Argentina. Phylogenetic analysis revealed clustering with previously reported Argentine strains, indicating ongoing viral circulation in local farms. The outbreak in this region was likely due to deficiencies in biosecurity measures rather than the introduction of a new strain. This study also reports, for the first time, the isolation of the virus from lung and lymph node samples of finishing pigs exhibiting respiratory signs.
Key words: Suid Alphaherpesvirus 1, Aujeszky's disease, viral isolation, outbreak, molecular characterization, swine production.La enfermedad de Aujeszky (EA) es causada por el Varicellovirus suidalpha herpesvirus suino tipo 1 (SuHV-1) que pertenece al género Varicellovirus, familia Orthoherpesviridae y subfamilia Alphaherpesvirinae (ICTV 2021). Los hospedadores naturales son los cerdos silvestres (Sus scrofa) y domésticos (Sus scrofa domesticus), pero también puede infectar de forma aguda y letal a numerosas especies como son los caninos, felinos, bovinos, ovinos, lagomorfos, mapaches, osos y zorros (Liu et al. 2022) que entran en contacto con cerdos o consumen su carne infectada. En los últimos años se ha considerado la posibilidad de que este agente infeccioso sea potencialmente zoonótico, al ser detectado en humanos (Ai et al. 2018, Wang et al. 2019, 2020, Yang et al. 2019, Zheng et al. 2022).
La relación entre la morbilidad y mortalidad dependen de la edad, la presencia de anticuerpos contra el agente y el estado inmunitario y sanitario de los animales. En los lechones de menos de 2 semanas de vida el desenlace es fatal, mientras que en los cerdos de destete se manifiesta con signos nerviosos (ataxia, incoordinación, posturas anormales “perro sentado”, parálisis, salivación, pedaleo), con alta mortalidad (Nauwynck 1997). En cerdos de engorde, la enfermedad tiene una baja mortalidad, pudiendo cursar de forma subclínica o manifestarse clínicamente con signología respiratorios como tos y disnea. Por otro lado, la infección en reproductores puede ocasionar abortos, repetición de celos, pérdida de peso, signos respiratorios, fiebre o presentarse en forma subclínica. En los cerdos que superan la fase clínica, el virus permanece en estado de latencia en el ganglio trigémino y puede generar nuevos ciclos de reinfección al reactivarse debido a diferentes factores como estrés, corticoides o cambios ambientales (Mettenleiter 2020).
El virus puede ser excretado por saliva, secreciones nasales, orina, semen y leche. Las vías de transmisión pueden ser aerógena, sexual y transplacentaria. Por lo tanto, puede llegar a una granja por 4 vías principales: I) por contacto con animales como cerdos silvestres o roedores; II) por vectores como las garrapatas (Liu et al. 2022); III) por contacto con otros cerdos o sus secreciones o fómites durante su traslado o IV) por circulación aérea (Hu et al. 2023).
El virus replica en las células epiteliales del tracto respiratorio superior (tabiques nasales, amígdalas, nasofaringe, tráquea y pulmones) y luego hace viremia atravesando la membrana basal transportado por linfocitos infectados. Luego de la replicación primaria el virus penetra en las terminaciones nerviosas del sistema nervioso periférico alcanzando bulbo olfatorio y ganglio trigémino donde establece latencia (Zheng at al. 2022).
En Argentina, la enfermedad fue registrada por primera vez en 1978 y actualmente es considerada endémica. Existe un plan nacional de control y erradicación, Resolución Nº 474/09, del Servicio Nacional de Sanidad y Calidad Agroalimentaria (SENASA 2023). Esta clasifica a los establecimientos de acuerdo con su estatus serológico y determina una regionalización basada en la prevalencia de granjas positivas. A nivel predio, determina que todo establecimiento porcino positivo a la enfermedad debe implementar un plan de saneamiento, en focos y perifocos y del mismo modo, define a la vacunación de emergencia en zona. Además, la enfermedad es de reporte obligatorio según la Resolución Nº 153/2021.
Los últimos antecedentes serológicos referidos a la población de cerdos domésticos corresponden al año 2010 los cuales determinaron un 19,1% de establecimientos positivos de un muestreo aleatorio realizado en el país (Dibarbora et al. 2017, Aznar et al. 2022), mientras que, en cerdos silvestres, los únicos datos reportados demostraron 5,76% de serología positiva (Williman et al. 2024). A partir del año 2016, el SENASA sólo permitía la vacunación de granjas positivas, con un plan de saneamiento utilizando vacuna inactivada importada (cepa Bartha K61 gE negativa). Un estudio realizado en 2017, en una zona de alta densidad porcina de la provincia de Santa Fe, demostró una alta eficacia de la vacunación sin circulación viral luego de 6 meses de su implementación (Aznar et al. 2022).
Hasta el año 2023, los casos clínicos de la enfermedad en nuestro país fueron escasos y asociados principalmente a establecimientos de baja escala o “traspatio” con pocas o nulas medidas de bioseguridad. Sin embargo, se realizaron estudios moleculares de cepas circulantes en Argentina que determinaron la presencia del genotipo I basado en patrones de restricción con la enzima BamHI (RFLP). La caracterización basada en secuencias parciales del gen gC demostró que las cepas argentinas se agrupan en cuatro «clusters» (Serena et al. 2011, 2018, 2023).
Frente a signos compatibles con la EA en el sudeste de la provincia de Córdoba, este estudio tuvo como objetivo describir las características clínico-epidemiológicas del brote 2023-2024 y caracterizar molecularmente a las cepas actuantes aisladas a partir de muestras de pulmones y linfonódulo.
Descripción y cronología de los signos clínicos observados en las granjas involucradas en el brote. En septiembre de 2023, se detectaron cerdos de 145 días con fiebre, disnea, tos, y una caída aproximada de 16,5% en el consumo de agua y alimento con respecto al consumo esperado. El cuadro clínico generó un aumento de la mortalidad del triple de lo esperado en la granja (13% con relación al histórico de 4,5%). Los hallazgos macroscópicos de las necropsias a nivel pulmonar se correspondieron con bronconeumonías y pleuroneumonías fibrinosas o fibrino-necróticas principalmente y marcado edema en tabiques interlobulares. La respuesta a la medicación con distintos antibióticos fue muy escasa. Esta granja afectada a la cual denominaremos Granja A corresponde a un sistema wean to finish o destete/venta, cerrado, intensivo, que entrega lechones de 21 días a múltiples granjas. El plan de vacunación del sistema incluía vacunas contra: parvovirus-leptospiras, Escherichia coli, Bordetella bronchiseptica, Pasteurella multocida (en reproductoras), Lawsonia intracellularis, Mycoplasma hyopneumoniae y circovirus porcino tipo 2. En relación con la EA, la granja era negativa, siguiendo los protocolos de la normativa vigente.
Ante la severidad del cuadro clínico se enviaron muestras de pulmón para cultivos bacteriológicos al Laboratorio de Sanidad Animal en Porcinos de INTA Marcos Juárez y para virus de influenza a un laboratorio privado; por otro lado, se enviaron muestras de alimento para la determinación de micotoxinas (empresa proveedora de servicios de nutrición). Las muestras para serología se tomaron a 20 días de observado el aumento de mortalidad en la Granja A y se enviaron a un laboratorio privado para determinar anticuerpos contra EA por ELISA (Hipra, Serie CAE96H8 estampilla 171535205M, vencimiento 19/4/2024), muestreo que se repitió a los 15 días.
Se registraron cuadros clínicos similares en dos granjas de engorde asociadas, Granja B a los 21 días y Granja C a los 40 días, situadas a 2,8 y 36 km de distancia de la Granja A, respectivamente. En Granja B con cerdos de entre 100 y 150 días y Granja C con cerdos de más de 150 días. El cuadro clínico-patológico fue similar, caracterizado por bronconeumonías y neumonía intersticial con marcado edema interlobular. Pocos días después de iniciado el cuadro, se observaron, tanto en Granja A como B, gatos muertos en la proximidad de los galpones.
Dos meses después de haberse registrado los primeros signos respiratorios en la Granja A, se observaron signos clínicos nerviosos en la unidad productora de lechones (UPL, Granja D), distante a 13 km de la Granja C. Inicialmente se detectaron temblores, ataxia, incoordinación en lechones de 14 días, siendo la mortalidad de 18% en la primera semana y aumentado hasta el 70% en las semanas siguientes. En función de la severidad y particularidad del cuadro, de esta última granja se enviaron al laboratorio oficial del SENASA, lechones para realizar estudios de PCR para la EA (noviembre 2023). Se comienza a vacunar en enero de 2024 con vacuna gE deleteada atenuada a todos los reproductores de las granjas involucradas.
En noviembre de 2024, se registraron nuevamente signos respiratorios en un sitio de engorde del mismo sistema (Granja E) que recibe únicamente cerdos vacunados de la UPL (Granja D) distante a 6 km. En este caso la mortandad fue menor a lo ocurrido en 2023 (6%), no existiendo aletargamiento ni asfixia. En la Tabla 1 se resumen datos de interés de las 5 granjas mencionadas.
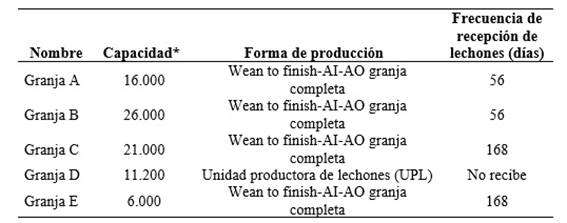
* Granjas A, B, C y E: considerar la capacidad en plazas de lechones para engorde.
* Granja D: considerar la capacidad en número de hembras reproductoras activas.
AI - AO: se refiere al manejo all in - all out de los cerdos.
Bioseguridad de los establecimientos afectados. Todas las granjas involucradas tenían cercos perimetrales que delimitaban físicamente e impedían el ingreso de personas, medios de transporte y animales ajenos al plantel. Los portones de acceso permanecían cerrados la mayor parte del tiempo, admitiendo únicamente el ingreso al sitio de aquellas personas que habían efectuado correctamente el registro de acceso. Dichos portones contaban con indicaciones visibles y claras, indicando la prohibición de entrada de personas y vehículos ajenos al plantel.
En cuanto al ingreso vehicular, todas las granjas cuentan con un arco sanitario verificado regularmente con el objetivo de detectar anomalías en los picos rociadores y controlar y asegurar volúmenes de la solución desinfectante. Cada vehículo que ingresaba a las granjas debía contar con previa autorización por parte del jefe del sector, registrar correctamente el ingreso y luego pasar por el filtro sanitario. Los vehículos para el transporte de los animales debían llegar lavados y desinfectados. Los conductores, sin poder descender de la cabina, avanzaban lentamente a través del filtro sanitario, permitiendo que la solución desinfectante contacte con las superficies externas del vehículo.
En relación al ingreso de personas ajenas al plantel, se solicitó completar una declaración jurada simple indicando no haber tenido, durante mínimo de dos noches, contacto directo o indirecto con cerdos vivos o muertos, planteles porcinos, frigoríficos, ferias de ganado, salas de necropsia u otras instalaciones y/o actividades que supongan riesgos sanitarios. Una vez dentro del establecimiento ingresaban a los vestidores adyacentes y requerían cumplir un flujo unidireccional entre la zona sucia y la restante zona limpia, para vestir ropa exclusiva del plantel. Las visitas ingresaban al vestuario, se desvestía completamente dejando la ropa de calle y calzado en determinados casilleros dispuestos para ese fin, despojándose de artefactos como relojes, cadenas, lentes etc. Luego de este punto, se procedió a la higienización en las duchas utilizando un agente desinfectante como es la clorhexidina, para finalmente colocarse la ropa limpia y exclusiva de las granjas en cuestión.
Por último, los materiales e insumos fueron ingresados a las granjas a través de una cámara de desinfección, luego de recibir una pulverización con un producto comercial compuesto por etanol y fenilfenol.
Recolección y análisis de las muestras. En el mes de noviembre de 2023 y una vez confirmado el diagnóstico serológico de EA por parte de un laboratorio privado, se recibieron en el Laboratorio de Virología de la Facultad de Ciencias Veterinarias de la Universidad Nacional de La Plata, 4 aparatos respiratorios completos y diversas muestras de linfonódulos, cerebros, hígados, bazos y riñones perfectamente conservados en refrigeración provenientes de cerdos de engorde de la Granja C para diagnóstico molecular y aislamiento viral. Asimismo, en 2024 durante el mes de noviembre se recibieron también 3 aparatos respiratorios completos frescos refrigerados pertenecientes a la Granja E. Todas las muestras de órganos recibidas se procesaron para aislamiento viral y para análisis de la EA mediante técnicas moleculares.
Brevemente, para la técnica de aislamiento viral, un trozo (1 cm2) de cada órgano fue disgregado en mortero con tijeras y arena estéril y un volumen de medio esencial mínimo (MEM) en proporción final 1/10. Luego de centrifugar durante 15 min a 5.000 rpm, el sobrenadante fue colectado y centrifugado nuevamente a 12.000 rpm durante 15 min. Finalmente, el sobrenadante fue filtrado mediante filtros de 0,22 µm, diluido con medio de cultivo MEM (1/10 y 1/100) y utilizado como inóculo para la infección de células RK13 en monocapa con un 80% de confluencia. Los cultivos inoculados fueron mantenidos con medio MEM con el agregado de 2% de suero fetal bovino e incubados a 37 ºC en atmósfera con 5% CO2. La presencia de efecto citopático (ECP) compatible con herpes se observó diariamente (Serena et al. 2018).
Para el análisis por técnicas moleculares, a partir del homogenato obtenido en la primera centrifugación descrita anteriormente, se procedió a realizar la extracción de ADN utilizando kit comercial (High Pure PCR Template Preparation Kit, Roche Diagnostics, Mannheim, Alemania). Posteriormente, el ADN extraído se utilizó para la detección molecular por PCR punto final utilizando cebadores que amplifican una porción del gen gD del virus de la EA. Asimismo, a partir de los sobrenadantes de las células inoculadas para aislamiento viral, se procedió a realizar una PCR punto final empleando cebadores que amplifican el gen gC para su posterior secuenciación de acuerdo a lo descrito por Serena et al. (2018).
Para el análisis de polimorfismo de longitud de fragmentos de restricción (RFLP), 1,5 μg de ADN se digirieron durante toda la noche con 2 UI de BamHI a 37 °C y luego se separaron por electroforesis en gel de agarosa al 0,7% (p/v) (140 x 150 x 5 mm) en tampón TAE (40 mM Tris-acetato pH 7,8, 5 mM acetato de sodio y 1 mM EDTA) a 20 V durante 16 h a temperatura ambiente. El gel se tiñó con bromuro de etidio y se visualizó bajo transiluminador UV (Serena et al. 2010).
Los productos de PCR correspondientes al gen gC, se purificaron y se enviaron a secuenciar en ambos sentidos al servicio de la Unidad Genómica del Hospital EL CRUCE-Florencio Varela y al Laboratorio de Salud Pública, área Genómica y Diagnóstico Molecular, Facultad de Ciencias Exactas, Universidad Nacional de La Plata. Las secuencias obtenidas se editaron utilizando el software BioEdit, versión 7.2.1. y se realizó un análisis de homología mediante BLASTN program (National Center for Biotechnology Information [http://www.ncbi.nlm.nih.gov/BLAST/]). Para el análisis filogenético se utilizó el programa MEGA X, donde en primer lugar las secuencias fueron alineadas mediante Clustal W (Kumar et al. 2018) y posteriormente, el árbol filogenético fue realizado utilizando Maximum Likelihood method y JTT matrix-based model. Se compararon con todas las secuencias argentinas disponibles (Tabla 2).
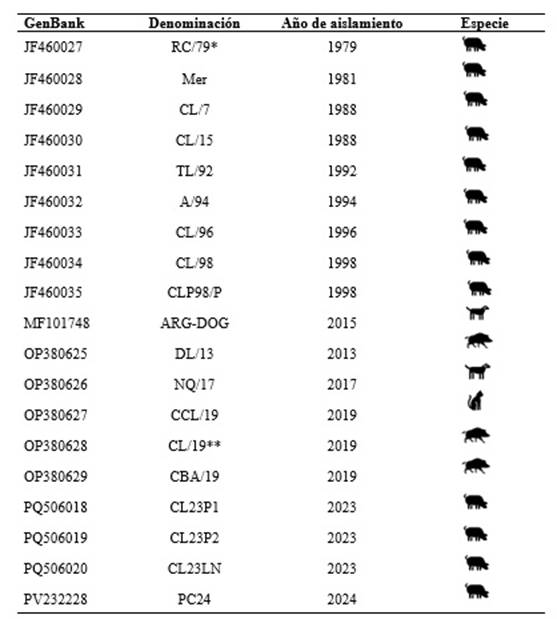
*Primera cepa aislada en Argentina en el laboratorio del Dr. Ambrogi (Ambrogi et al. 1981).
**cepa no incluida en el alineamiento por ser menor a 696 nucleótidos.
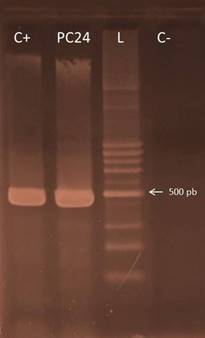
Detección por PCR diferencial mediante detección del gen gE. Con el fin de evaluar si las cepas aisladas del cuadro clínico de 2024 eran vacunales o de campo, se realizó PCR para detección de gE parcial con el siguiente par de primers gE-FW: 5’-CCGCGGGCCGTGTTCTTTGT-3’ y gE-RV: 5’-CGTGGCCGTTGTGGGTCAT-3’ (493 pb) (Huang et al. 2004). Las mezclas de reacción se ciclaron de acuerdo al protocolo descrito por Fonseca et al. (2010).
Detección, diseminación y contagio. Luego de 20 días de presentarse los primeros signos clínicos respiratorios en la Granja A, se detectaron 4 muestras serológicas sospechosas de un total de 30 (13,33%) con valores de 40-45% de acuerdo a las instrucciones del kit utilizado. En el segundo muestreo realizado 15 días posteriores donde se considera seroconversión, se detectaron 28 muestras (93,33%) reactivas, mientras que 1 muestra (3,33%) fue considerada sospechosa y 1 (3,33%) como negativa. Asimismo, se detectaron grandes cantidades de fumonisinas en el alimento.
En los pulmones analizados, se observó edema interlobulillar marcado, áreas de neumonía lobulillar, focos de pleuritis y áreas de bronconeumonía. Además, en uno de los animales analizados se observó dentro de la tráquea abundante contenido mucopurulento (Figura 1).
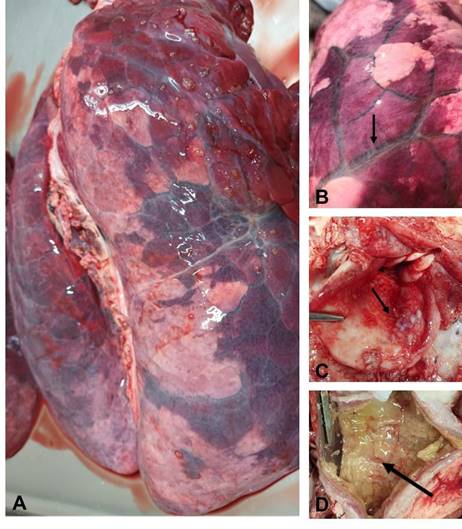
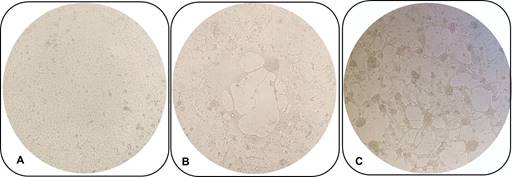
Aislamiento viral. En los cultivos de células RK13 inoculados con las muestras procesadas, se observó un claro ECP compatible con el virus de la EA que posteriormente fue confirmado por secuenciación. En 24 h post infección se observó un claro efecto lítico con formación de sincicios (Figura 2) en las 4 muestras de pulmón y linfonódulo remitidas en 2023 provenientes de la Granja C. De igual modo, se logró el aislamiento a partir de dos de las muestras de pulmón analizadas en el año 2024 provenientes de la Granja E.
Caracterización molecular de las cepas aisladas. El análisis de RFLP muestra que las cepas de 2023 y 2024 pertenecen al tipo genómico I. En la Figura 3 se observa la presencia del fragmento genómico 2 luego de la digestión del ADN con la enzima BamHI lo que determina que las cepas pertenecen al tipo I.

Del total de cepas aisladas (n = 7), se seleccionaron 2 aislamientos obtenidos de pulmón y uno de linfonódulo del año 2023 (Granja C) y uno de pulmón de 2024 (Granja E), que fueron denominadas CL23/P1, CL23/P2, CL23/LN (año 2023) y PC24 (año 2024). Luego de la PCR se realizó la secuenciación parcial del gen gC y las secuencias obtenidas fueron depositadas en el GenBank con la siguiente denominación: PQ506018, PQ506019, PQ506020 y PV232228 (Tabla 3).
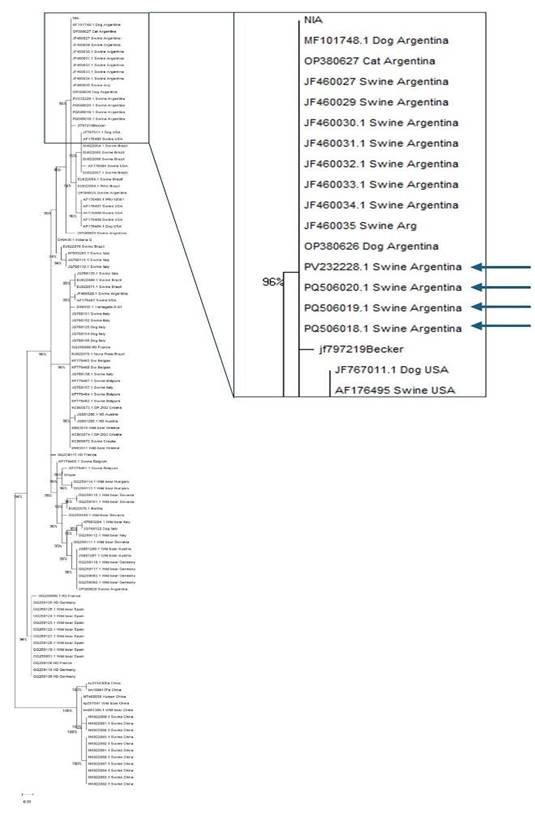
El análisis filogenético de las nuevas cepas obtenidas en este trabajo, evidencia que las mismas se agrupan con la mayoría de las cepas argentinas publicadas anteriormente formando un grupo separado junto con las cepas de referencia NIA y Becker (Figura 4).
PCR para detección del gen gE del aislamiento PC24. La PCR realizada a la cepa PC24 resultó positiva al gen gE como se evidencia en la Figura 5.
En los últimos años, la producción porcina de Argentina ha crecido considerablemente generando mayores desafíos tanto desde el punto de vista sanitario, como desde la gestión de la bioseguridad en las granjas porcinas. Si bien la distribución de granjas abarca todo el país, la mayor producción porcina se concentra en la zona central del territorio. En las zonas noreste y noroeste existen gran cantidad de unidades productoras, las mismas poseen un bajo número de madres (entre 10 y 50 por unidad productiva) (Serena et al. 2023).
En relación con la EA y de acuerdo a datos de SENASA (2023) y con anterioridad a este brote de 2023, los predios positivos eran principalmente granjas pequeñas de 11 a 50 cerdas, considerados de baja escala o "traspatio", donde las medidas de bioseguridad son menores o nulas. Hasta el año 2023, la baja seroprevalencia detectada en granjas comerciales con más de 100 cerdas indicaba que el programa nacional de erradicación, basado en estudios serológicos, vacunación y segregación, se desarrollaba sin ningún tipo de alteración. De acuerdo a la fuente consultada (SIGSA - SENASA), existen 97.268 unidades productivas (UPs), de las cuales el 90% tienen entre 1 a 50 cerdas (87.291 UPs) mientras que sólo el 0,1% (139 UPs) tiene más de 500 cerdas (Anuario SENASA 2023).
Entre los años 2013 y 2019 se aislaron cepas de distintas zonas geográficas, sin aparición clínica explosiva en cerdos, aunque con mortandad de algunos animales centinela como perros y gatos (Serena et al. 2023). Hasta entonces, los reportes de casos clínicos y su posterior aislamiento y caracterización se asociaban a cuadros detectados en granjas de mediana producción y en general localizadas en la zona central del país, región con mayor prevalencia de la enfermedad. La detección de EA en dicha zona implicaba el riesgo de introducción de la enfermedad en las granjas de mayor cantidad de cerdas, con mayor tecnificación y de mejor estatus sanitario.
Los resultados obtenidos en el presente trabajo demuestran la circulación viral en granjas de alta tecnificación, bioseguridad y con un gran número de madres. La presentación clínico-epidemiológica de este brote varía de lo reportado previamente ya que se observó un cuadro respiratorio severo en animales de engorde y, posteriormente, un cuadro clínico nervioso en una UPL. Esto sugeriría, que las granjas de engorde fueron el punto de ingreso del virus al establecimiento, y si bien es difícil determinarlo de manera fehaciente, el contacto con algún camión de carga a faena contaminado sería el punto más probable de ingreso, sin descartar la posibilidad de contacto con cerdos silvestres presentes en la zona. Sin embargo, tras la aparición de problemas respiratorios en las dos granjas cercanas (Granja A y Granja B), se constató que, aunque no se habían detectado movimientos de animales entre ambas granjas, sí compartían equipos de trabajo, operarios y vehículos para el transporte de materias primas comunes, lo que también favoreció la entrada por vía aerógena debido a la escasa distancia que las separa. En el caso de la Granja C, ocurrió un trabajo de reparaciones con un contratista que había visitado la Granja A con anterioridad. En el caso de la Granja D, comparte con la Granja C tanto la logística como la planta de alimento balanceado, mientras que la Granja E se había poblado con lechones provenientes de la UPL bajo plan de saneamiento con vacuna atenuada gE deleteada.
Un dato importante, desde el punto de vista diagnóstico, es que durante la aparición de signos clínicos severos los resultados serológicos fueron no concluyentes (sospechosos) y requirieron un nuevo muestreo confirmatorio luego de 15 días. Lo que resalta la importancia de un enfoque diagnóstico integral para llegar a un diagnóstico rápido debido a las limitaciones de la serología en fase aguda. El diagnóstico serológico si bien es muy útil a la hora de realizar seguimientos epidemiológicos de la enfermedad, frente a cuadros clínicos agudos, debe siempre acompañarse de otro tipo de técnicas directas como son las técnicas moleculares y/o de inmunohistoquímica (OIE 2018). La relevancia de la notificación oficial temprana al SENASA cobra fuerza una vez más: la importancia de un diagnóstico específico y rápido permite tomar medidas sanitarias de emergencia y reforzar las medidas de bioseguridad, internas y externas, para reducir el riesgo de diseminación de la enfermedad.
La forma explosiva de la presentación clínica observada en el brote descrito, en un principio, orientaba a que se podría tratar de una nueva cepa de alta patogenicidad. Sin embargo, la comparación entre secuencias del gen gC parcial demuestra que no existe variación significativa ni a nivel nucleotídico ni aminoacídico como se observa en el análisis filogenético realizado. La topología del árbol obtenido no difiere de la disposición descrita previamente por Serena et al. (2023) para las 11 cepas argentinas previamente publicadas que incluyen cepas aisladas de cerdos domésticos, perro y gato.
Al igual que la mayoría de las cepas argentinas detectadas anteriormente, estas nuevas cepas pertenecen al mismo tipo genómico I, excepto la cepa Mer -clasificada como tipo II- correspondiente a la clasificación de Herrmann et al. (1984) (Echeverría et al. 1994, Serena et al. 2010, 2018, 2023).
Tras la confirmación del diagnóstico de la enfermedad en el 2023 y dada la severidad del cuadro, se gestionó la importación de emergencia de una vacuna viva deleteada, debido a que no se disponía de vacunas inactivadas. Es así como el SENASA dispuso la importación y comercialización de 1.200.000 dosis de vacunas atenuadas deleteadas (gE negativa) como vía de excepción, que arribaron al país en enero de 2024 continuando con la modalidad de la resolución del 2009, de manera de diferenciar animales vacunados de infectados en forma natural. A partir de enero 2024 se vacunaron a todos los animales reproductores machos y hembras de entre 70 y 150 días de vida (Granja D-UPL). Sin embargo, 10 meses después el cuadro clínico respiratorio volvió a evidenciarse en cerdos de engorde del mismo sistema asociado.
De los aislamientos obtenidos en 2024, los resultados evidenciaron que la cepa recuperada es de campo y no vacunal. Un estudio realizado en Argentina en 2017 en un criadero comercial demuestra que luego de aplicar 3 dosis de vacuna gE negativa inactivada no se logró impedir la transmisión oral y que recién luego de mantener la medida sanitaria durante 4 años, el control se consideró eficiente (Aznar et al. 2022). Asimismo, otro estudio describe que cerdos de engorde vacunados con el mismo tipo de vacuna, no desarrollaron anticuerpos neutralizantes (Cane et al. 2021).
El presente trabajo describe las principales características del brote de EA ocurrido recientemente en Argentina, resaltando la importancia de la realización de un diagnóstico completo con el fin de identificar y caracterizar las cepas actuantes. Los resultados obtenidos en este trabajo permiten inferir que las nuevas cepas detectadas mantienen las mismas características genéticas que las demás cepas argentinas aisladas previamente, sugiriendo que no hubo introducción de nuevas cepas y que posiblemente el virus ha sido introducido en las explotaciones por deficiencias en las medidas de bioseguridad. El potencial zoonótico del virus de la EA ha sido reportado, causando principalmente encefalitis y éstos subrayan la necesidad de que los trabajadores de la industria porcina y los investigadores aumenten las medidas de bioseguridad y protección personal en la rutina de trabajo (Wang et al. 2019, 2020, Yang et al. 2019).
En este contexto, a partir de las muestras recibidas en el laboratorio de La Plata, se logró aislar virus de la EA a partir de pulmón y linfonódulo de animales de engorde que hasta el momento no había sido descrito en nuestro país.
Agradecimientos. Al personal no docente del Laboratorio de Virología, Facultad de Ciencias Veterinarias de la Universidad Nacional de La Plata, Téc. Claudio Leguizamón y Lic. Micaela Irure por su valioso trabajo.
Contribución de los autores. MMW: realizó los experimentos de laboratorio, procesó los datos experimentales y redactó el artículo con la colaboración de todos los autores. DSO: colaboró en la ejecución de los experimentos y análisis de necropsia. JAC: contribuyó al muestreo y colaboró en la redacción del manuscrito. LM y DMG: realizaron los muestreos y contribuyeron en la redacción y análisis de los resultados. SEC: colaboró en la ejecución de los experimentos. GEM: realizó los experimentos, preparó las versiones del manuscrito y supervisó todas las tareas experimentales. MSS: realizó la filogenia y banco de datos. MGE: procesó los datos experimentales, revisó las versiones del manuscrito y supervisó la actividad del grupo.
Declaración de conflictos de intereses. Los autores declaran no tener conflictos de intereses financieros ni relaciones personales conocidas que pudieran haber influido en el trabajo presentado en este artículo.
Disponibilidad de datos. Los datos estarán disponibles previa solicitud.