Revista Veterinaria. 2026; 37(1)
https://doi.org/10.30972/vet.3719055
Artículo Original




1Universidad de los Llanos, Facultad de Ciencias Agropecuarias y Recursos Naturales, Escuela de Ciencias Animales, Grupo de investigación en Farmacología Experimental y Medicina Interna – Élite, Programa de Medicina Veterinaria y Zootecnia, Villavicencio 1745, Meta, Colombia.
2Universidad de los Llanos, Facultad de Ciencias Agropecuarias y Recursos Naturales, Doctorado en Ciencias Agrarias. Villavicencio 1745, Meta, Colombia.
3Universidad de los Llanos, Facultad de Ciencias Agropecuarias y Recursos Naturales, Escuela de Ciencias Animales, Laboratorio de Microbiología. Villavicencio 1745, Meta, Colombia.
4Universidad de los Llanos, Facultad de Ciencias Agropecuarias y Recursos Naturales, Escuela de Ciencias Animales, Laboratorio de Farmacología. Villavicencio 1745, Meta, Colombia.
 chaira.vasquez@unillanos.edu.co
chaira.vasquez@unillanos.edu.co
 dumar.jaramillo@unillanos.edu.co*
dumar.jaramillo@unillanos.edu.co*
Recibido: 16 agosto 2025 / Aceptado: 03 noviembre 2025
Resumen
Toxocara spp. es el principal geohelminto zoonótico que causa la toxocariosis, una enfermedad globalmente desatendida. Caninos y felinos son los hospederos definitivos de este parásito y los principales dispersores de huevos embrionados a través de sus heces. En Colombia, el departamento del Meta adolece datos epidemiológicos de este parásito, siendo el propósito de este trabajo el de hallar la prevalencia de huevos de Toxocara spp. en parques públicos y correlacionar la carga y presencia parasitaria con área del parque y estratos socioeconómicos, respectivamente, de las 10 comunas de la ciudad de Villavicencio. Para ello, se colectaron heces frescas en 51 parques públicos seleccionados aleatoriamente dentro de las 10 comunas de la ciudad. Las heces se procesaron usando la técnica de Kato-Katz para determinar la carga parasitaria de huevos de Toxocara spp. por gramo de materia fecal (hpg). Se analizó la prevalencia y hpg por comuna, se correlacionó hpg con el área del parque y prevalencia con el estrato socioeconómico usando razón de prevalencia (RP) y Chi cuadrado (X2), con un intervalo de confianza del 95% (IC95%). El estudio reveló una prevalencia de huevos de Toxocara spp. del 60,7% (31/51, con Me 73,75 rango 0 a 248,8 hpg) de los parques. Hubo mayor contaminación de los parques de las comunas 4 (87,5%, 7/8, Me: 160, rango 20 a 260 hpg) y 5 (72,7%, 8/11, Me: 140, rango 0 a 280). No hubo correlación significativa entre hpg y el área del parque (Spearman, p = 0,326). Los parques ubicados en el estrato socioeconómico 3 mostraron mayor prevalencia (73%, 11/15) que los parques ubicados en los otros estratos, aunque sin correlación significativa entre estas dos variables (RP:1,46; IC95%: 0,52–4,1, X2 p = 0,34). Los parques públicos de Villavicencio presentan alta contaminación por Toxocara, lo que exige mayor control y tenencia responsable de mascotas.
Palabras clave: ecoepidemiología, geohelmintiasis, salud pública, zoonosis.
Abstract. Toxocara spp. is the most prevalent zoonotic geohelminth worldwide and the causative agent of toxocariosis, a globally neglected disease. Dogs and cats serve as the definitive hosts and are the main disseminators of embryonated eggs through their feces. In Colombia, the department of Meta lacks epidemiological data on this parasite. Therefore, this study aimed to determine the prevalence of Toxocara spp. eggs in public parks and to assess the relationship between parasite load, park area, and socioeconomic stratum across the ten communes of Villavicencio city. Fresh fecal samples were collected from 51 randomly selected public parks distributed among the ten communes. Samples were processed using the Kato-Katz technique to quantify Toxocara spp. eggs per gram of feces (epg). Prevalence and epg were analyzed by commune; epg was correlated with park area, and prevalence was compared among socioeconomic strata using the prevalence ratio (PR) and Chi-square (X2) test, with a 95% confidence interval (95% CI). Toxocara spp. eggs were detected in 60.7% (31/51, median: 73.75, range: 0-248.8 epg) of the parks. Higher contamination levels were found in communes 4 (87.5%, 7/8, median: 160, range: 20-260 epg) and 5 (72.7%, 8/11, median: 140, range: 0-280 epg). No significant correlation was observed between epg and park area (Spearman, p = 0.326). Parks located in socioeconomic stratum 3 showed a higher prevalence (73%, 11/15) than those in the other strata, although the association was not statistically significant (PR: 1.46; 95% CI: 0.52-4.1; X2 p = 0.34). The high level of Toxocara contamination in Villavicencio's public parks underscores the need for improved control measures and responsible pet ownership to reduce environmental and public health risks.
Key words: Ecoepidemiology, Geohelminthiasis, Public health, Zoonosis.
Caninos y felinos son los hospederos definitivos de Toxocara spp. y los principales dispersores de huevos embrionados a través de sus heces. Otros focos de exposición a huevos embrionados son el pelaje de las mascotas, el calzado de los propietarios y las almohadillas de los animales, representando un riesgo considerable porque incluso gatos y perros desparasitados pueden actuar como diseminadores de Toxocara (Airs et al. 2022, Merigueti et al. 2022).
La estrecha interacción que genera un lugar público (ej., parque) entre los reservorios y hospedadores definitivos (caninos y felinos silvestres y domésticos -de vida libre o de compañía-) y hospedadores paraténicos (ej., humanos) permite la transmisión rápida que generalmente ocurre a través de la ingesta de larvas infectantes (L3) de Toxocara spp. presentes en huéspedes accidentales o de huevos embrionados en el ambiente (Salazar-Garcés et al. 2020, Keegan et al. 2025).
Toxocara spp. en humanos presenta diversas formas clínicas como larva migrans visceral (VLM), ocular (OT), neurotoxocariasis (NT) y subclínicas como la toxocariasis encubierta (CT), con casos reportados en múltiples países (Wu y Bowman 2020, Zheng et al. 2020). Los niños son la población más vulnerable a este tipo de parásito, debido a baja inmunidad, deficientes hábitos de higiene y frecuente interacción con mascotas (Rojas-Salamanca et al. 2016).
En el mundo la prevalencia promedio de huevos de Toxocara spp. en espacios públicos se estima en 21%, aunque varía considerablemente según la región, donde se presumen valores aproximados del 35% en Asia-Pacífico, 27% en África y 25% en América Latina (Fakhri et al. 2018). Sin embargo, estudios en países de habla hispana de América del Sur han informado prevalencias más amplias, que pueden oscilar entre 33% y 90,9%, reflejando las diferencias en las condiciones ambientales y los métodos de muestreo empleados (López et al. 2020).
Por otro lado, en Estados Unidos se reportó una prevalencia de entre 21,3% y 28,4% (Duncan et al. 2020). En Argentina se ha registrado una mayor presencia de huevos en primavera (20,9%) a comparación con invierno (12,7%), sugiriendo una relación entre el clima y la persistencia de este parásito (Avila et al. 2023). En Brasil, tanto en mascotas como en perros y gatos callejeros se presentó una alta exposición a T. canis, con prevalencias entre 0,7 y 48,9% en perros, que son similares a los datos encontrados en gatos de entre 0,3 y 43,1% (Dantas 2020).
En Colombia, la prevalencia de Toxocara spp. ha sido medida en algunos parques públicos determinando la cantidad de huevos por gramo, con diferentes niveles de riesgo dependiendo de la ubicación. En la localidad de Suba (Bogotá) se reportaron bajas prevalencias de Toxocara spp. de 5,4% (Polo et al. 2007). Sin embargo, en Ipiales (Nariño) se hallaron altas prevalencias alrededor de 45,71 - 50% (Martínez et al. 2016). En Duitama (Boyacá) se notificó una prevalencia de 34,7 % en T. canis (Guarín et al. 2016).
Los estudios citados muestran tasas variables de contaminación con Toxocara spp. en áreas públicas y recreativas como parques, es así, que en Colombia existe una prevalencia general estimada de Toxocara 40,4-54,4% (Rodriguez-Morales et al. 2020). La afinidad de este parásito por climas cálidos como los del trópico bajo (López et al. 2020) y la falta de datos epidemiológicos de Toxocara en Villavicencio (Meta), hacen de esta investigación una necesidad. El objetivo de este trabajo fue determinar la carga parasitaria de huevos de Toxocara spp. por gramo de materia fecal (hpg) para analizar la prevalencia y hpg por comuna, correlacionar hpg por área del parque y hallar prevalencia con el estrato socioeconómico en los parques de la ciudad de Villavicencio (Meta, Colombia).
Localización. El estudio se llevó a cabo en la ciudad de Villavicencio (Meta), a 467 msnm, con temperatura promedio de 27 °C, humedad relativa entre 77-83% y precipitaciones de 1.200 cm3 (Hurtado-Moreno et al. 2017). Según el Acuerdo 458 de 2021 del Concejo de Villavicencio, esta ciudad se distribuye en 10 comunas agrupadas en 510 barrios, planes parciales y urbanizaciones (Consejo municipal de Villavicencio 2021).
Población y tipo de estudio. El tamaño de la muestra se calculó mediante el software Epi-info, v. 7.0 de los Centros para el control y prevención de enfermedades de Estados Unidos (CDC https://www.cdc.gov/eplinfo/esp/es_index.html), utilizando la fórmula: n = [EDFF*Np (1-p)]/[(d2/Z21-α/2*(N-1) +p*(1-p)], ajustado por un factor de corrección (EDFF) para el diseño del estudio de 1.0, donde N fue 325, siendo la cantidad de parques públicos (Decreto 1000-24-195 de 2022, secretaria Planeación municipal). Se consideró un intervalo de confianza del 95% (IC95%), z21-α/2 = 1,96, un límite de confianza (d) del 5%, y respecto a la proporción esperada (p) se tuvieron en cuenta resultados obtenidos por Díaz-Anaya et al. (2015) donde halló un 4% de contaminación de los parques de Tunja con huevos de Toxocara spp. La muestra representativa fue de 51 parques, los cuales se estratificaron en 10 comunas de acuerdo con la cantidad de parques de cada comuna (Tabla 1).
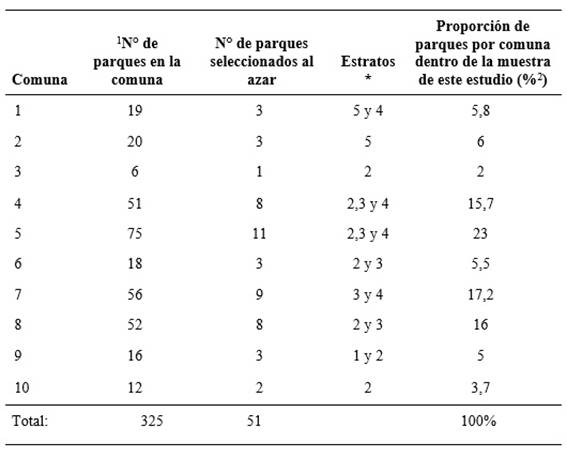
N°: Número. 2 %: Porcentaje. *Decreto 1000-24-195 de (2022) *Resolución N° 156 del 2019.
Recolección y procesamiento de muestras de heces. En cada parque se inspeccionó su superficie total y se dividió en nueve subáreas homogéneas. En cada una de estas subáreas, se recolectaron todas las heces frescas (no deshidratadas) de caninos. De cada subárea se tomaron 5 g de estas, así cada parque debería tener entre 0 a 9 muestras tomadas el mismo día y tiempo (0 sí no había heces de caninos, 9 si cada subárea tenía heces). En 20 días se realizó el muestreo de los 51 parques seleccionados aleatoriamente dentro de las 10 comunas. Estas muestras se identificaron registrando la fecha, lugar de colecta y almacenadas a 4 °C hasta su procesamiento antes de 24 horas. Con el fin de determinar la caracterización morfológica de los huevos de Toxocara spp. se utilizó la guía de clave taxonómica de Soulsby (De vries et al. 2008); para establecer la carga parasitaria se usó la técnica de Kato-Katz estandarizada por Cárdenas et al. (2021). Donde se realizó el conteo de los huevos de Toxocara spp. colocando el portaobjetos bajo un microscopio con aumento de 40x. Se establecieron como positivos parques con al menos 1 huevo en las muestras procesadas y el número total de huevos observados se multiplicó por 20, como valor constante, para determinar la cantidad de huevos por gramo (hpg).
Análisis estadístico. La prevalencia (P) general, P por comunas y P por estrato socioeconómico (ES) de huevos de Toxocara spp. en parques públicos de la ciudad de Villavicencio se expresó como proporción mediante la siguiente fórmula, considerando un intervalo de confianza 95% (IC95%), p<0,05. Donde P = N.º de parques públicos positivos a Toxocara spp. Total de parques públicos en riesgo en la ciudad, en cada comuna y en cada ES, respectivamente, expresando la P en porcentaje. A los resultados de hpg por parque y por comunas se les aplicó la prueba de Bartlett para determinar su comportamiento heterocedástico, presentando estos como mediana (Me) y rangos mínimo y máximo. Mediante la prueba de Spearman, IC95%, p<0,05, se evaluó la correlación entre hpg con el área por parque (m²). Además, se estableció la razón de prevalencia (RP), IC95%, y el Chi cuadrado (X 2 , p<0,05) entre la positividad a Toxocara spp. por parques de acuerdo con su ES, que van del 1 al 6 según las metodologías del DANE en la resolución 392 de 2004. Las estimaciones estadísticas se realizaron utilizando el software Epi Info v. 7.0 del CDC y los mapas epidemiológicos utilizando el software QGIS 3.10.
Aspectos éticos. Este trabajo recibió aval del Comité de Bioética de la Universidad de los Llanos, según Acta 005 del 01/09/2022.
Se recolectaron 217 muestras de heces frescas en los 51 parques de Villavicencio dentro de las 10 comunas, con una mediana (Me) 4 muestras por parque y un rango mínimo y máximo de 0 - 9 (rango 0 - 9). Los parques de las comunas 4 (Me 5,5; rango 3 - 8) y 7 (Me 5, rango 2 - 8) presentaron la mayor cantidad de muestras de heces recolectadas. En la Tabla 2 se presenta la cantidad de muestras de heces frescas colectadas por parque y por comuna.
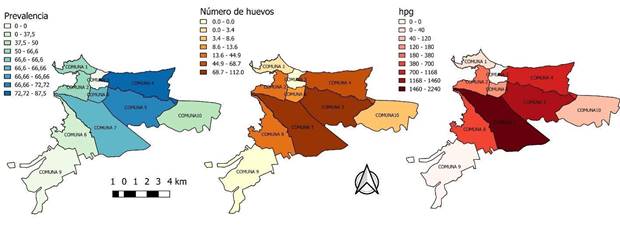
La prevalencia general de contaminación por huevos de Toxocara spp. en parques de Villavicencio fue del 60,7% (31/51, Me 280 hpg, rango 0 - 1.260). En la Tabla 2 y en la Figura 1A se pueden observar la frecuencia, Me y rangos encontrados por cada comuna.
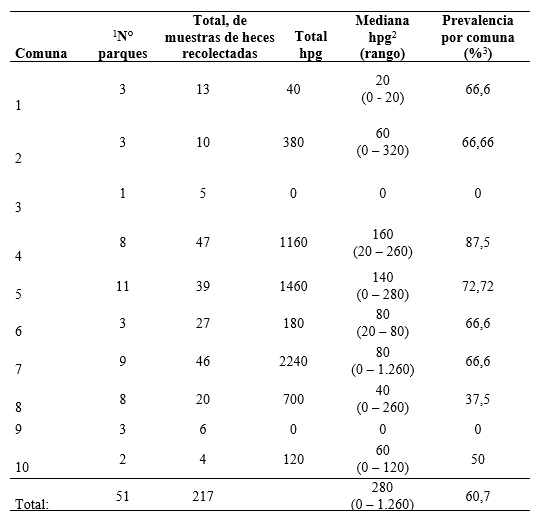
N°: Número de los parques muestreados; 2hpg: Huevos Toxocara spp. por gramo de heces. (%) Porcentaje.
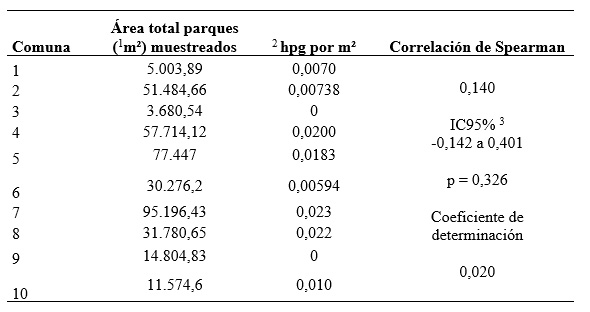
m²: Metro cuadrado; 2 hpg/m²: Huevos por gramo de materia fecal por metro cuadrado de parque; 3 IC95%: Intervalo de confianza del 95%.
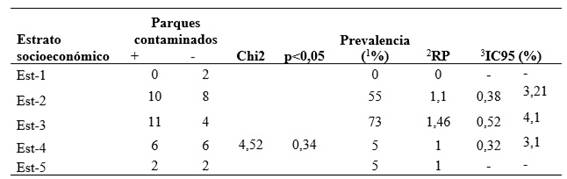
%: Porcentaje; 2RP: Razón de prevalencia; 3IC95%: Intervalo de confianza 95%
La prevalencia general hallada aquí, supera la prevalencia mundial estimada por Fakhri et al. (2018) en lugares públicos para Toxocara spp., que es del 21%. También sobrepasa las reportadas en regiones como Europa (18%, IC95% 14-22%), América del Norte y Central (13%, IC95% 8-23%) y el Sudeste Asiático (21%, IC95% 3-49%). Sin embargo, este estudio muestra una prevalencia inferior a los datos reportados por Bonilla-Aldana et al. (2023) en Latinoamérica, quienes encontraron prevalencias del 100% en Argentina, 66% en Brasil y 63% en Venezuela. De igual forma, se encontró que países ecuatoriales reportaban cifras inferiores a las halladas en este estudio, por ejemplo, Ecuador con una prevalencia del 36,4% (Moscoso 2022), posiblemente debido a la técnica coprodiagnóstica utilizada, donde Kato-Katz, técnica utilizada en este estudio, tiene una mayor sensibilidad para Toxocara spp. que otras técnicas habituales en Medicina Veterinaria (Cárdenas et al. 2021).
En Colombia existen reportes que concuerdan con la prevalencia de 60,7% encontrada en este estudio (Martínez et al. 2016, Rodriguez-Morales et al. 2020), no obstante, esta misma varía considerablemente entre regiones con diferentes características climáticas. En zonas de clima cálido como Barranquilla, donde las temperaturas oscilan entre los 27 a 32 °C, se reportó una prevalencia del 53,84% de T. canis (Erofeeva y Vasenev 2020). Sin embargo, en regiones de clima más templado o frío, los resultados son más variables. Por ejemplo, en Pasto (Nariño), con temperaturas promedio entre 13 a 15 °C se estimó una prevalencia del 54,83% (Benavides et al. 2017), mientras que en Tunja (Boyacá), con un promedio de temperaturas similares entre 12 a 14 °C se registró una prevalencia menor (9,7%) (Díaz-Anaya et al. 2015), difiriendo con los reportes presentados en este estudio. Estas diferencias sugieren que, si bien la temperatura ambiental puede influir en la prevalencia, otros factores ecológicos, sociales y de manejo sanitario también pueden jugar un papel importante en la distribución de este parásito (Bonilla-Aldana et al. 2023).
Toxocara spp. es un parásito con distribución cosmopolita y puede encontrarse una variedad de entornos y ambientes. Sin embargo, su persistencia y capacidad de generar focos de infección está influenciada por condiciones ambientales que favorecen su ciclo de vida (Guimarães et al. 2005; Raissi et al. 2021). La variación de las prevalencias a nivel nacional e internacional pueden estar relacionadas con las condiciones climáticas, debido a que la temperatura óptima para la embrionación de los huevos de Toxocara se encuentra entre 15 y 30 °C, se ha identificado que, a temperatura de 34 °C, se genera una disminución de la viabilidad, mientras que a 37 °C la temperatura es letal para los huevos, así el desarrollo embrionario ya hubiera iniciado (Liotta et al. 2024). De igual forma, otra condición para el desarrollo y la supervivencia de los huevos de Toxocara, es la humedad relativa (HR), ya que estos pueden sobrevivir en suelos que tengan un contenido de HR tan bajo como el 4,1%, sin embargo, el nivel óptimo para el desarrollo de los huevos oscila entre HR 51 al 59% (Maya et al. 2010).
Respecto a hpg y m2 (hpg/m²) por parques de cada comuna (Tabla 3), la comuna 7 con el área de 95.196,43 m² en sus nueve parques muestreados (Tabla 2), fue la más extensa y obtuvo la mayor contaminación de Toxocara spp. (0,023 hpg/m²) en comparación con las áreas de los parques que integran las demás comunas. No obstante, no se encontró una relación significativa entre hpg y m² (Spearman, p = 0,326). Desde el conocimiento de los autores no hay estudios que relacionen estadísticamente hpg y m2. Sin embargo, se ha encontrado que la contaminación con Toxocara spp. depende tanto de la presencia y actividad de animales hospedadores (principalmente perros y gatos domésticos), así como el uso y características del área evaluada (Carrada et al. 2005; Joy et al. 2017), como de las condiciones que acompañan la superficie de suelo como mayor cobertura vegetal y área sombreada presentan una correlación directa con la contaminación con huevos de este parásito, ya que favorecen la resistencia y viabilidad de los huevos, tal y como se evidencia en un estudio realizado por Avila et al. (2023) en San Juan, Argentina.
Por otro lado, la Tabla 4 evidencia la distribución y prevalencia de contaminación de los 51 parques en relación con su ES del 1 al 5, en donde: ES-5 7,8% (4/51), ES-4 23,5% (12/51), ES-3 29,4% (15/51), ES-2 35,3% (18/51) y ES-1 3,9% (2/51). Se encontró que los parques ubicados en ES-3, dentro de las diferentes comunas, tienen la mayor prevalencia (73%), observando una probabilidad 1,46 veces más de encontrarse contaminados frente a los otros parques que integran los otros ES. Sin embargo, este no fue significativo (RP 1,46, IC95% 0,52-4,1). Se encontró que la contaminación por huevos de Toxocara spp. en los parques era independiente a su ES (X 2 p = 0,34).
A pesar de la falta de asociación significativa en este estudio, evidencia internacional ha demostrado la relación entre la contaminación ambiental por Toxocara spp. y el ES. Un estudio realizado por Tyungu et al. (2020) en New York (Estados Unidos) encontró que el Bronx (zona de bajo estrato socioeconómico) tenía una prevalencia de 66,7%, mayor a la que se registró en Manhattan (zona más acomodada) donde solo alcanzó 29,6%. De forma similar, en Brasil, Capuano y Rocha (2005) reportaron menores tasas de contaminación en las zonas céntricas (nivel socioeconómico más alto) en comparación con las periferias (nivel socioeconómico más bajo). En el sureste de Estados Unidos, Crudo et al. (2024) evidenciaron que las tasas de contaminación del suelo con Toxocara spp. se correlaciona positivamente con mayores índices de pobreza e ingresos bajos a nivel comunitario. Esto demuestra que la toxocariosis no solo es una enfermedad desatendida, sino también un marcador de desigualdad socioeconómica.
Si bien este estudio no halló relación estadística entre el ES y la contaminación con huevos de Toxocara spp. en parques públicos (Tabla 4), la alta prevalencia de la toxocariosis presentada en otros estudios, evidencia que la pobreza y las zonas económicamente deprimidas están más expuestas a estar contaminadas a este parásito debido a que el de acceso limitado a servicios de saneamiento básicos, las condiciones de hacinamiento, la falta de educación sanitaria, la presencia de animales callejeros no desparasitados y la exposición a suelos contaminados con heces de perros y gatos aumentan el riesgo de infección con Toxocara spp. (Moreira et al. 2014).
En conclusión, los hallazgos de este estudio confirman la contaminación ambiental por huevos de Toxocara spp. en los parques de Villavicencio, lo que refuerza la preocupación de exposición ambiental a agentes zoonóticos en espacios de uso público. Aunque los resultados permiten evidenciar una alta prevalencia, es importante considerar factores ambientales que podrían estar relacionados a estos índices elevados como la temperatura y la humedad relativa (Raissi et al. 2020), los cuales no fueron considerados y representan una limitación para interpretar completamente las condiciones que favorecen la persistencia del parásito en el suelo. Tampoco se incluyeron otras especies parasitarias de interés zoonótico que podrían estar presentes en estos (Avila et al. 2023). A pesar de estas limitaciones, los datos obtenidos evidencian la necesidad de fortalecer programas de control sanitario y promoción de la tenencia responsable de mascotas lo que permitirá reducir el riesgo de zoonosis y propagación ambiental de Toxocara.
Agradecimientos. Al Laboratorio de Farmacología de la Escuela de Ciencias Animales de la Universidad de los Llanos por el soporte general para el desarrollo de esta investigación.
Contribución de los autores. RSDF: realizó los experimentos, procesó los datos experimentales y redactó el artículo con la colaboración de todos los autores. MAJP: contribuyó al muestreo y colaboró en la ejecución de los experimentos. TDLF: realizó los experimentos, procesó los datos experimentales y redactó el artículo con la colaboración de todos los autores. VTCLA: procesó las muestras. VTA: procesó y analizó los datos experimentales. JHDA: realizó los experimentos, procesó los datos experimentales y redactó el artículo con la colaboración de todos los autores.
Declaración de conflictos de intereses. Los autores declaran no tener conflictos de intereses financieros ni relaciones personales conocidas que pudieran haber influido en el trabajo presentado en este artículo.
Disponibilidad de datos. Los datos estarán disponibles previa solicitud.