Revista Veterinaria. 2026; 37(1)
https://doi.org/10.30972/vet.3719058
Artículo Original




1EEA INTA Mercedes, Corrientes, Argentina.
1Instituto de Patobiología Veterinaria (IPVET), Unidad de Doble Dependencia, Instituto Nacional de Tecnología Agropecuaria (INTA), Consejo Nacional de Investigaciones Científicas y Técnicas (CONICET), Hurlingham B1686, Argentina.
1Instituto de Investigación en Veterinaria, Facultad de Ciencias Agrarias y Veterinarias, Universidad del Salvador, Buenos Aires, Argentina.
 schnittger.leonhard@inta.gob.ar
schnittger.leonhard@inta.gob.ar
Recibido: 09 junio 2025 / Aceptado: 27 noviembre 2025
Resumen
La piroplasmosis equina (PE) es una enfermedad parasitaria causada por Theileria equi y Babesia caballi, protozoos intraeritrocíticos transmitidos principalmente por garrapatas. En Argentina, la PE es endémica en el noreste, causando un impacto sanitario y económico negativo en la producción equina. No obstante, los animales infectados generalmente se presentan como portadores asintomáticos. En este trabajo, se estudió la tasa de infección por T. equi y B. caballi en caballos de trabajo (n = 98). Para ello, se realizaron frotis de sangre y PCR para detectar cada patógeno. De los equinos estudiados, no se encontraron parásitos en ninguno de los frotis analizados. Sin embargo, 52 animales resultaron positivos para T. equi (53,1%) mediante PCR. Los animales se clasificaron en tres categorías etarias y se encontró que la tasa de infección fue del 55,6% (15 de 27 caballos) en caballos de 1 a 3 años, del 55,4% (31 de 56 caballos) en animales de 4 a 10 años y del 40% (6 de 15 caballos) en animales mayores de 10 años. Notablemente, las tasas de infección fueron estadísticamente similares en las tres categorías estudiadas (p = 0,55). Como los animales de mayor edad estuvieron expuestos a las garrapatas durante un tiempo superior, cabría esperar un incremento en la tasa de infección en los grupos con aminales longevos. Asimismo, no se observó una diferencia significativa entre la tasa de infección y el sexo de los animales (p = 0,46). Por otra parte, no se han detectado animales positivos para B. caballi mediante PCR. El examen clínico reveló buena condición general y ausencia de ectoparásitos en los animales, con la excepción de un solo espécimen de Rhipicephalus microplus. Este estudio revela una alta frecuencia de caballos infectados con T. equi y enfatiza la importancia de implementar medidas de control y desarrollar estrategias de diagnóstico más sensibles.
Palabras clave: piroplásmidos, hemoparásitos, PCR, parasitemia, theileriosis equina, babesiosis equina.
Abstract. Equine piroplasmosis (EP) is caused by Theileria equi and Babesia caballi, intraerythrocytic protozoa transmitted by ticks. In Argentina, EP is endemic in the northeast, negatively affecting equine health and economic productivity. Nevertheless, infected animals generally appear as asymptomatic carriers. This study evaluated the infection rate of T. equi and B. caballi in working horses (n = 98). Blood smears from all animals were prepared and examined microscopically, followed by direct parasite detection using diagnostic PCR. No parasites were detected in the examined smears. However, 52 horses tested positive for T. equi (53.1%) by PCR. Three age categories were compared, revealing infection rates of 55.6% (15/27) in 1–3-year-old horses, 55.4% (31/56) in horses aged 4–10 years, and 40% (6/15) in horses older than 10 years. Notably, the infection rates across age categories did not differ significantly (p = 0.55). Considering that older animals have longer exposure to ticks, a higher infection rate in these groups might have been expected. Additionally, no significant association was found between infection status and the sex (p = 0.46). All horses tested negative for B. caballi by PCR. Clinical examination revealed good general condition and absence of ectoparasites, except for a single specimen of Rhipicephalus microplus found in one horse. The high rate of T. equi infection in the studied horses in this region underscore the need for improved control measures, treatment strategies, and the development of more sensitive diagnostic tools.
Key words: piroplasmids, hemoparasites, PCR, parasitemia, equine theileriosis, equine babesiosis.
La piroplasmosis equina (PE) es una enfermedad causada por Theileria equi y Babesia caballi, protozoos intraeritrocíticos pertenecientes al Phylum Apicomplexa, presentes en caballos y otros équidos como mulas, burros y cebras, produciendo un impacto económico negativo en la industria equina (Schnittger et al. 2012, Onyiche et al. 2019). Esta enfermedad tiene una distribución global, pero es altamente endémica en países tropicales, subtropicales y algunos templados, sitios aptos para el desarrollo de las garrapatas, que inoculan los parásitos al hospedador durante la alimentación (Uilenberg 2006, Scoles y Ueti 2015). Tanto T. equi como B. caballi se transmiten principalmente a los équidos por especies de garrapatas de los géneros Amblyomma, Dermacentor, Hyalomma y Rhipicephalus (Scoles y Ueti 2015). En Argentina, se ha documentado la presencia de garrapatas potencialmente vectores de estos protozoos como por ejemplo R. microplus (Battsetseg et al. 2002, Guglielmone et al. 2014, Copa et al. 2023). Además, estos parásitos pueden transmitirse en forma iatrogénica a través de transfusiones de sangre, agujas y jeringas contaminadas e instrumental quirúrgico (Georges et al. 2011, Ueti y Knowles 2018).
Ambos parásitos tienen un ciclo de vida complejo. En el hospedador equino, T. equi y B. caballi se reproducen asexualmente dentro de los eritrocitos infectados, causando hemólisis masiva, anemia grave y otros signos clínicos, lo que en ocasiones puede provocar la muerte del animal (Uilenberg 2006, Schnittger et al. 2022). Por su parte, en T. equi se ha reportado la transmisión transestadial, en la que la garrapata adquiere el parásito durante la alimentación y lo transmite en el siguiente estadio (de larva a ninfa o de ninfa a adulto) al hospedador vertebrado (Schnittger et al. 2022, Ravindran et al. 2023). Sin embargo, se reportó también la transmisión intraestadial de este patógeno por la garrapata R. microplus (Ueti et al. 2008). Además, en T. equi la transmisión por vía transplacentaria está bien documentada (Allsopp et al. 2007, Tirosh-Levy et al. 2020a). En lo que respecta a B. caballi, se ha evidenciado la transmisión transovárica desde la garrapata hembra a las larvas de la siguiente generación a través de los huevos (Randolph et al. 1996, Georges et al. 2011, Ravindran et al. 2023). Esto permite que la infección se perpetúe en las siguientes generaciones de garrapatas y que estas transmitan los patógenos durante cualquier etapa de su desarrollo. En general, las infecciones producidas por B. caballi son clínicamente leves y menos comunes que las causadas por T. equi, pero es imposible diferenciar entre ambos parásitos basándose únicamente en los signos clínicos. En el caso de T. equi, los animales se convierten en portadores asintomáticos con baja parasitemia de por vida y contribuyen a la propagación del parásito al actuar como fuente de infección para otras garrapatas. Por el contrario, se ha reportado que los animales infectados con B. caballi pueden eliminar los parásitos de forma natural en un plazo de 4 años en ausencia de reinfecciones (Scoles y Ueti 2015).
La PE es considerada un problema sanitario regional en Argentina debido al impacto que causa en la salud equina y la economía de los productores (Spath et al. 1994). En este sentido, la detección de portadores es crucial para diseñar estrategias de manejo, como así también, para prevenir la introducción de la PE en áreas o países no endémicos mediante el movimiento de animales infectados aparentemente sanos. El objetivo de este estudio fue estimar la tasa de infección por T. equi y B. caballi en equinos del Departamento de Santo Tomé (Corrientes) mediante microscopía y la técnica de PCR, utilizando oligonucleótidos específicos para la detección de cada parásito.
Animales, toma de muestras y frotis sanguíneo. Se analizaron equinos (n = 98; 40 hembras y 58 machos) pertenecientes a 22 propietarios ubicados en la localidad de Gobernador Virasoro, Corrientes, Argentina (Lat. 28º 02’46, 05”S; Long. 56º 02’07,03”O) entre mayo de 2022 y marzo de 2023. Los animales muestreados son utilizados para la fabricación artesanal de ladrillos, criados en pequeñas granjas familiares o en tierras de pastoreo comunales, en una zona endémica para la garrapata común del ganado, R. microplus (Nava et al. 2024, Torrents et al. 2025). Se registró la edad y el sexo de cada animal para su análisis posterior. El análisis por microscopía se llevó a cabo mediante frotis sanguíneos teñidos con Giemsa que se realizaron a partir de sangre periférica con objetivo de inmersión en aceite y un aumento final de 1.000 X. Se examinaron aproximadamente 100 campos por preparado de cada equino. Se tuvieron en cuenta los parámetros morfológicos y biométricos, incluyendo la forma, la ubicación y el tamaño del parásito en los eritrocitos infectados (OMSA 2023). El ADN genómico se extrajo utilizando un kit comercial (INBIO Highway, Argentina) a partir de 500 µL de sangre obtenida asépticamente por punción de la vena yugular (Vacutainer™, Becton Dickinson, una muestra por animal) con anticoagulante citrato al 5%. Las muestras recolectadas fueron almacenadas a -20 °C hasta su procesamiento. Se realizó la determinación taxonómica de la garrapata recolectada utilizando caracteres morfológicos establecidos previamente (Nava et al. 2017). Algunos pocos propietarios usaron ocasionalmente acaricidas cuando observaron un excesivo número de garrapatas, pero no han realizado el registro de su uso.
Los procedimientos realizados en este estudio contaron con el consentimiento informado de todos los propietarios y la aprobación del Comité Institucional para el Cuidado y Uso de Animales de Estudio (CICUAE) del Vicerrectorado de Investigación y Desarrollo de la Facultad de Ciencias Agrarias y Veterinarias de la Universidad del Salvador (Protocolo SIGEVA USAL N° 80020210100026US).
Detección de los parásitos por PCR. Se amplificó por PCR una región del gen 18S ARN ribosomal de los hemoparásitos T. equi y B. caballi con la utilización de oligonucleótidos específicos (Tabla 1) como se describió previamente, pero con las siguientes modificaciones (Bashiruddin et al. 1999, Alhassan et al. 2005, OMSA 2023). Para ello, cada mezcla de reacción de PCR se preparó para un volumen final de 25 µL conteniendo: 0,5 µM de cada primer, 0,2 mM de cada dNTP (INBIO Highway, Argentina), 0,3 U de Dream Taq DNA Polymerase (Thermo Scientific, Estados Unidos), 1 µL de ADN. Ambas reacciones de amplificación se realizaron bajo las mismas condiciones: desnaturalización inicial a 95 °C durante 5 minutos, seguida de 30 ciclos de desnaturalización a 95 °C por 30 s, hibridación a 51 °C por 30 s y extensión a 72 °C por 1 minuto. Tras una elongación final a 72 °C durante 7 minutos, los productos de amplificación fueron analizados en un gel de agarosa al 1,5%, (TransGen, China) y visualizados con EcoGel (INBIO Highway, Argentina) en un transiluminador. Como control positivo se utilizó ADN obtenido a partir de cultivos in vitro de cada parásito, y agua destilada ultrapura como control negativo. Las muestras que produjeron amplicones del tamaño esperado en los respectivos ensayos de PCR se consideraron positivas.
Análisis estadístico. Las estimaciones estadísticas entre las tasas de positividad de los diferentes grupos de edad de los animales se calcularon mediante la prueba de chi cuadrado y la posterior determinación de los valores p (https://www.medcalc.org/calc/comparison_of_proportions.php). Se presentan los valores de chi-cuadrado (Χ2), los grados de libertad (gl) y los valores p correspondientes.

En este trabajo se investigó la presencia de T. equi y B. caballi, agentes etiológicos de la PE en equinos en la localidad de Gobernador Virasoro, Corrientes, Argentina. Ninguno de los animales analizados mostró signos de enfermedad clínica al momento del muestreo. La examinación microscópica no permitió confirmar la presencia de ninguno de los hemoparásitos en los frotis de sangre analizados. Comúnmente, el examen morfológico de frotis de sangre para el diagnóstico de la piroplasmosis es útil en la fase aguda de la enfermedad, mientras que no permite detectar estos parásitos en animales portadores crónicos y/o asintomáticos (Tirosh-Levy et al. 2020a). Esto se debe a que, en esta fase, la enfermedad cursa con una muy baja parasitemia sin sintomatología clínica (Benitez et al. 2018). Además, se requiere mucha experiencia por parte del operador para poder diferenciar estas especies de piroplásmidos, debido a su similitud morfológica (OMSA 2023).
Se han establecido varios métodos de detección molecular basados en PCR dirigidos a diversos genes que facilitan la diferenciación entre ambas especies con mayor sensibilidad, aun en casos de coinfección (OMSA 2023). Sin embargo, se ha demostrado que las infecciones de piroplásmidos durante la fase crónica de la enfermedad pueden escapar a la detección, incluso con la utilización de métodos altamente sensibles basados en PCR anidada, lo que impulsa a la optimización del diseño de ensayos para aumentar la sensibilidad de detección (Calder et al. 1996, Álvarez et al. 2019, Ganzinelli et al. 2022).
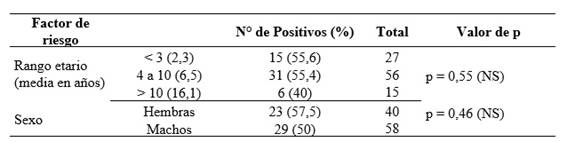
En este trabajo, se utilizaron oligonucleótidos específicos para la amplificación por PCR de una región del gen 18S ARN ribosómico de cada una de las especies estudiadas. En el análisis de detección molecular de las muestras estudiadas se observó que 52 de los 98 equinos (53,1%) fueron positivos para T. equi. La tasa de infección en los diferentes rangos etarios fue 55,6% (15 de 27) en el grupo etario de 1 a 3 años, 55,4% (31 de 56) en animales de 4 a 10 años de edad y 40% (6 de 15) en los animales mayores de 10 años (Tabla 2). Las tasas de infección por T. equi observadas fueron similares en cada uno de los tres grupos de edad examinados, como demostró una prueba de chi-cuadrado (χ²gl=2, α<0,05 = 1,21 => p = 0,55; Tabla 2). Además, se observó una tasa de infección estadísticamente similar entre los sexos de los animales. (χ²gl=1, α<0,05 = 0,5347 => p = 0,46).
El parásito T. equi es transmitido por garrapatas, por lo que su presencia está limitada a las regiones donde se encuentra el vector. Asimismo, al aumentar la edad de los animales, se incrementa el tiempo de exposición a las garrapatas, por lo que cabría esperar que la tasa de infección (probabilidad de infectarse) con los parásitos aumentará conforme con la edad de los animales. Es decir, que haya un aumento progresivo del número de animales infectados en las categorías etarias con animales más longevos. En el presente estudio se plantea la hipótesis de la observación de este patrón de dinámica de la infección, tal y como se ha reportado en numerosos estudios previos (Rüegg et al. 2008, Guidi et al. 2015, Tirosh-Levy et al. 2020a,b, Nadal et al. 2022). Contrariamente a nuestra expectativa, los datos muestran proporciones estadísticamente similares en los grupos de animales estudiados. Existe la posibilidad de que el parásito se transmita principalmente por vía transplacentaria en esta región, mientras que su transmisión por garrapatas sea poco relevante. Así, la proporción de animales infectados se mantendría estable a medida que los caballos envejecen. Hay que señalar que resultados similares fueron descriptos en la misma región por Ferreira et al. (2016), quienes no encontraron una tasa de infección significativamente más alta al comparar la presencia de garrapatas, la edad, o el sexo, mediante técnicas serológicas y moleculares. Sin embargo, un estudio reciente muestra que la transmisión transplacentaria en este hospedador es posiblemente poco frecuente (Tirosh-Levy et al. 2020c). Por ello, no se pueden excluir otros factores responsables para estas observaciones y serán necesarios futuros estudios para determinar la verdadera razón que explique los resultados obtenidos.
Por el contrario, en el presente estudio no se obtuvieron muestras positivas para B. caballi. Las investigaciones sobre la presencia de este parásito en la región son escasas, pero en un estudio reciente se demostró que el 25% de los caballos examinados (12 de un total de 47 animales) fueron serológicamente positivos para T. equi, mientras que ningún caballo fue positivo para B. caballi (Barrandeguy et al. 2019). Sin embargo, se encontraron garrapatas Dermacentor nitens infectadas con B. caballi, lo que indica la circulación de este patógeno en la región (Copa et al. 2023). Se ha reportado que la parasitemia de este hemoparásito en animales portadores es menor que para T. equi, y posiblemente escape a la detección con PCR (Schnittger et al. 2022). Por esta razón, por el momento no se puede descartar que B. caballi no esté presente en la región estudiada.
Los agentes etiológicos de la piroplasmosis equina son transmitidos por varias especies de garrapatas. En el cono sur de Sudamérica, los caballos están infestados mayormente con tres especies de garrapatas: D. nitens, A. sculptum y R. microplus, aunque hay reportes de infestaciones ocasionales con otras especies de los géneros Amblyomma, Haemaphysalis e Ixodes (Scoles y Ueti 2015). En Argentina, la única garrapata que está reportada como vector de T. equi y B. caballi en equinos es D. nitens (Copa et al. 2023). En cuanto a la garrapata común del bovino, R. microplus, se sabe que también parasita frecuentemente a equinos (Guglielmone et al. 2014). Estudios experimentales han demostrado que R. microplus posee competencia vectorial para transmitir T. equi (Paulino et al. 2021), y ensayos a campo en Brasil detectaron ADN de T. equi y B. caballi en esta especie de garrapata (Battsetseg et al. 2002). En este trabajo, se realizó la determinación taxonómica de una garrapata recolectada sobre un animal, la cual fue identificada como una hembra adulta perteneciente a la especie R. microplus. Sin embargo, la presencia de hemoparásitos no fue investigada en este espécimen. En Argentina, el impacto de la transmisión de la PE por las garrapatas autóctonas, al igual que R. microplus, se desconoce.
La PE causa un impacto económico significativo en la producción equina, desde una reducción en el rendimiento hasta la muerte de los animales (Uilenberg 2006, Onyiche et al. 2019). Se ha reportado la presencia de EP en la Argentina y en países vecinos como Brasil y Paraguay (Asenzo et al. 2008, Ferreira et al. 2016, Valente et al. 2019, Ahedor et al. 2023b). La alta proporción de animales infectados con piroplásmidos en el presente y otros estudios pone en evidencia el problema sanitario de la región. Recientemente, se ha reportado la presencia de T. equi en equinos de la Ciudad de Corrientes, pero el bajo número de animales muestreados no permitió estimar la prevalencia en la población (Sebastian et al. 2021, Benitez-Ibalo et al. 2024). La tasa de infección más alta obtenida (81%, 34 positivos de un total de 42 animales) en comparación con el presente estudio, podría deberse al uso de una PCR anidada, que es un método más sensible. Disponer de herramientas de diagnóstico de laboratorio sensibles y específicas es esencial para maximizar la detección de equinos portadores de piroplásmidos asintomáticos (Ganzinelli et al. 2020).
No obstante, estos estudios preliminares han descrito la existencia de dos genotipos diferentes, el genotipo A (T. equi sensu stricto) y el genotipo C (T. equi sensu lato/Theileria haneyi), que circulan en la misma población de caballos (Benitez-Ibalo et al. 2024), y permitirían afirmar que los genotipos A y C están presentes en Argentina. Más aún, los mismos genotipos se han reportado como las variantes predominantes en caballos de Brasil y Paraguay (Valente et al. 2019, Ahedor et al. 2023a). Más estudios son necesarios para determinar la prevalencia de estas variantes y potencial presencia de otros genotipos de T. equi en Argentina.
La identificación específica y sensible de los agentes etiológicos y los vectores implicados permitirá realizar estudios epidemiológicos para llenar las carencias de conocimiento sobre la distribución y prevalencia de T. equi y B. caballi en Argentina. Esta información es esencial para el diseño de métodos de control mejorados contra la piroplasmosis equina.
Se estudió la tasa de infección por T. equi y B. caballi en caballos de trabajo pertenecientes a 22 propietarios asociados con la fabricación de ladrillos en Gobernador Virasoro, provincia de Corrientes. Más de la mitad de los animales (53,1%, 52 de un total de 98 equinos) fueron positivos para T. equi mientras que no se logró la detección de B. caballi. Los datos revelados muestran que la tasa de caballos infectados es la misma en los grupos de animales jóvenes (menos de 3 años), adultos (de 4 a 10 años) y mayores (>10 años). Tampoco se observaron tasas de infección significativamente diferentes con relación al sexo. La alta tasa de infección en los animales estudiados pone en evidencia la necesidad de una aplicación efectiva de programas de vigilancia y medidas de control para la PE en el norte de Argentina.
Agradecimientos. Los autores desean expresar su sincero agradecimiento al Dr. Naoaki Yokoyama por su generosa colaboración y habernos facilitado muestras de ADN de T. equi y B. caballi, como así también a la Dra. María Barrandeguy por su desinteresada colaboración. Proyecto financiado por SIGEVA-USAL: 80020210100026US e INTA: 2023-PE-L01-I044.
Contribución de los autores. Conceptualización: LS, SG; Metodología: SG, DB; Análisis formal: LS, SG, DB, JS, SL; Investigación: DB, SL; Recursos: DB, JS; Curación de datos: DB; Redacción: borrador original: SG, SL, DB, JS; Redacción: revisión y edición: LS, SG; Supervisión: DB, SL; Administración del proyecto: JS, SL, DB; Adquisición de fondos: JS; Los siguientes autores contribuyeron igualmente a este estudio: SG, DB.
Declaración de conflictos de intereses. Los autores declaran no tener conflictos de intereses financieros ni relaciones personales conocidas que pudieran haber influido en el trabajo presentado en este artículo.
Disponibilidad de datos. Los datos pueden obtenerse previa solicitud a los autores.