Revista Veterinaria. 2026; 37(1)
https://doi.org/10.30972/vet.3719059
Artículo Original




1Facultad de Ciencias Veterinarias. Universidad Nacional del Nordeste. Sargento Cabral Nº 2139 - Corrientes, Corrientes, Argentina.
2Facultad de Ciencias Exactas y Naturales y Agrimensura de la Universidad Nacional del Nordeste. 9 de Julio 1449 -Corrientes, Corrientes, Argentina.
 frangenetica.vet@comunidad.unne.edu.ar
frangenetica.vet@comunidad.unne.edu.ar
Recibido: 15 marzo 2025 / Aceptado: 05 diciembre 2025
Resumen
El impacto del herbicida 2,4-diclorofenoxiacético (2,4-D) en los ecosistemas acuáticos y, particularmente, en la biología de los peces, ha sido escasamente documentado. En este estudio se evaluó el potencial efecto genotóxico del 2,4-D en Piaractus mesopotamicus mediante el análisis de aberraciones cromosómicas en células renales. Se realizaron dos ensayos con 2,4-D: en uno se utilizó el producto puro (P) y en el otro una formulación comercial, 2,4-D Amina Sumagro® (FC). En ambos ensayos, los peces se distribuyeron en un grupo control (C) y cinco grupos tratados (T1 = 1 ppm; T2 = 1,8 ppm; T3 = 3,2 ppm; T4 = 5,6 ppm y T5 = 10 ppm). Tras un período de exposición de 70 días, los ejemplares fueron sacrificados mediante sobredosis de clorhidrato de lidocaína, y se analizaron un total de 1.100 metafases mitóticas. Las aberraciones cromosómicas observadas incluyeron gaps y quiebras cromosómicas, adhesividad, endomitosis y pulverización. No se registraron diferencias significativas entre los grupos tratados y los controles. Sin embargo, al considerar conjuntamente las concentraciones equivalentes de las formulaciones pura y comercial, se observó una diferencia estadísticamente significativa a 10 ppm en comparación con los controles. Estos resultados sugieren que la exposición crónica a concentraciones subletales de 2,4-D podría inducir alteraciones genotóxicas en P. mesopotamicus, especialmente a concentraciones elevadas. En consecuencia, se destaca la necesidad de fortalecer la vigilancia ambiental y la regulación del uso de herbicidas en sistemas agrícolas, con el fin de prevenir impactos adversos sobre la biota acuática.
Palabras clave: peces, pacú, ácido 2,4-diclorofenoxiacético, mutagenicidad, alteraciones cromosómicas.
Abstract. The impact of the herbicide 2,4-dichlorophenoxyacetic acid (2,4-D) on aquatic ecosystems and, particularly, on fish biology has been poorly documented. This study evaluated the potential genotoxic effect of 2,4-D on Piaractus mesopotamicus by analysing chromosomal aberrations in kidney cells. Two tests were conducted with 2,4-D: one using the pure product (P) and the other using a commercial formulation, 2,4-D Amina Sumagro® (FC). In both tests, the fish were divided into a control group (C) and five treated groups (T1 = 1 ppm; T2 = 1.8 ppm; T3 = 3.2 ppm; T4 = 5.6 ppm and T5 = 10 ppm). After a 70-day exposure period, the specimens were sacrificed by overdose of lidocaine hydrochloride, and a total of 1100 mitotic metaphases were analysed. The chromosomal aberrations observed included gaps and breaks, adhesivity, endomitosis and pulverisation. No significant differences were recorded between the treated groups and the controls. However, when considering the equivalent concentrations of the pure and commercial formulations together, a statistically significant difference was observed at 10 ppm compared to the controls. These results suggest that chronic exposure to sublethal concentrations of 2,4-D could induce genotoxic alterations in P. mesopotamicus, especially at high concentrations. Consequently, there is a need to strengthen environmental monitoring and regulation of herbicide use in agricultural systems in order to prevent adverse impacts on aquatic biota.
Key words: fish, pacu, 2,4-dichlorophenoxyacetic acid, mutagenicity, chromosomal alterations.
La intensificación de la agricultura ha incrementado la vulnerabilidad de los cultivos frente a las plagas. Prácticas como los cultivos múltiples por temporada, la reducción del barbecho y el establecimiento de monocultivos han favorecido la aparición y propagación de plagas, al reducir las barreras naturales que limitan su expansión (Reyes-Palomino y Cano Ccoa 2022). Como consecuencia, el ecosistema se ve inevitablemente afectado por el uso de plaguicidas, dada su toxicidad, persistencia y capacidad de bioacumulación.
El ácido 2,4-diclorofenoxiacético (2,4-D) es uno de los herbicidas sintéticos más antiguos, introducido en el mercado en la década de 1940. Actualmente, se encuentra entre los agroquímicos más utilizados a nivel mundial (Freisthler et al. 2022). Pertenece al grupo de los herbicidas fenoxi o fenoxiacéticos, también conocidos como clorofenólicos y se clasifica como “herbicida hormonal”, ya que actúa de forma análoga a la auxina natural ácido indol-3-acético (AIA) (Magnoli et al. 2020). Las concentraciones más elevadas de 2,4-D suelen detectarse en el suelo, el aire y las aguas superficiales cercanas a las áreas agrícolas, lo que genera la presencia de residuos relativamente altos y potencialmente peligrosos en el ambiente (Islam et al. 2018).
En Argentina, el Servicio Nacional de Sanidad y Calidad Agroalimentaria (SENASA), mediante las resoluciones N.º 466/2019 y 875/2019, dispuso la baja automática, a partir del 25 de julio de 2021 de los productos formulados con 2,4-D en base a ésteres butílicos e isobutílicos del Registro Nacional de Terapéutica Vegetal. Asimismo, se prohibió su importación desde diciembre de 2019 y su producción y fraccionamiento local desde julio de 2020. Esta medida respondió a la alta volatilidad de dichas formulaciones, capaces de provocar daños por deriva en cultivos no objetivos, con consecuencias económicas y riesgos potenciales para la salud humana y el ambiente. Cabe señalar que la disposición no incluyó al 2,4-D en su formulación como sal dimetilamina, de menor volatilidad y, por tanto, menos propensa a generar efectos adversos (SENASA 2019).
Los organismos acuáticos son particularmente sensibles a la exposición a plaguicidas, y numerosos estudios han documentado su toxicidad tanto en exposiciones agudas como crónicas (Soto et al. 2020). Entre ellos, los peces han sido ampliamente utilizados como bioindicadores debido a su sensibilidad ante alteraciones ambientales, las cuales pueden manifestarse a distintos niveles biológicos, desde cambios celulares y enzimáticos hasta efectos poblacionales, generando posibles disfunciones fisiológicas que afecten la reproducción y, en consecuencia, la estructura trófica de la comunidad (Tagliaferro 2020).
Asimismo, órganos como las branquias, los riñones, el hígado y la piel son considerados blancos útiles para la evaluación de la contaminación ambiental, y su análisis resulta valioso como biomarcador de exposición (Palma Leotta 2022). Estudios experimentales en peces han demostrado que diversas sustancias pueden inducir daño genético (Paravani et al. 2024), mientras que otras no presentan efectos genotóxicos detectables (Belpaeme et al. 1996).
Debido a su sensibilidad y confiabilidad, la técnica de aberraciones cromosómicas se emplea como herramienta útil para detectar la presencia de xenobióticos en ambientes acuáticos. En este contexto, el objetivo del presente estudio fue evaluar el posible efecto genotóxico del 2,4-D en juveniles de pacú (Piaractus mesopotamicus), mediante el análisis de la frecuencia de aberraciones cromosómicas en células renales. Para alcanzar dicho objetivo, se utilizaron dos formulaciones del herbicida: una pura (P) y otra comercial, 2,4-D Amina Sumagro®.
Animales. Ejemplares juveniles de P. mesopotamicus con 20 ± 3,2 g y 8 ± 1,8 cm (media ± DE; n = 24) fueron proporcionados por el Instituto de Ictiología del Nordeste (INICNE, Corrientes, Argentina). Antes de iniciar los ensayos de exposición, los peces fueron aclimatados durante 30 días en estanques de 300 L con agua de pozo artesiano, a una temperatura de 20 °C, pH 7,0 y un fotoperíodo controlado de 12 h luz: 12 h oscuridad. Durante el período de aclimatación, los especímenes fueron alimentados cada 48 h y se realizaron controles periódicos de su estado sanitario y comportamiento.
Producto químico. Se emplearon dos formulaciones del herbicida ácido 2,4-diclorofenoxiacético (2,4-D; C₈H₆Cl₂O₃): una formulación pura (P) y una formulación comercial, 2,4-D Amina Sumagro® (contenido: 58,4 g de sal amina del ácido 2,4-diclorofenoxiacético y compuestos inertes en cantidad suficiente para 100 cm3).
Ensayo de exposición in vivo. En los dos ensayos con 2,4-D, tanto en su forma pura (P) como con la formulación comercial (FC), los peces se dividieron en un grupo control (C; mantenido en agua de pozo artesiano) y cinco grupos tratados: T1 = 1 ppm, T2 = 1,8 ppm, T3 = 3,2 ppm, T4 = 5,6 ppm y T5 = 10 ppm. Cada experimento se desarrolló en seis acuarios de 20 L, con dos ejemplares por acuario. El volumen de agua se calculó considerando una relación de 1 L por cada centímetro de longitud corporal del pez, a fin de mantener condiciones adecuadas de bienestar y equilibrio ambiental.
Durante los períodos experimentales (70 días), se registraron las siguientes condiciones del agua: temperatura = 24,4 ± 0,4 °C; pH = 6,73 ± 0,02; oxígeno disuelto = 5 mg L⁻¹ y conductividad = 51 µS cm⁻¹. Se observaron dos muertes atribuidas al canibalismo en los distintos tratamientos; sin embargo, el resto de los ejemplares mantuvo un comportamiento normal durante todo el ensayo.
Sacrificio y muestreo tisular. Finalizado el período de exposición, los peces fueron sacrificados mediante sobredosis de clorhidrato de lidocaína (100 ppm). Para el análisis citogenético se extrajeron las porciones anterior y posterior del riñón de cada ejemplar.
Los procedimientos metodológicos utilizados en este estudio se adecuaron a los criterios sugeridos por el Comité de Ética y Bioseguridad de la Facultad de Ciencias Veterinarias de la Universidad Nacional del Noroeste, protocolo Nº: 0033.
Preparación cromosómica. La obtención de cromosomas mitóticos se realizó siguiendo la metodología de Foresti et al. (1993). Las aberraciones cromosómicas se identificaron de acuerdo con los criterios descriptivos propuestos por Savage (2004). Fueron analizados un total de 50 metafases por individuo.
Análisis estadístico. Los datos obtenidos fueron sometidos a un análisis de varianza (ANOVA) seguido de la prueba de comparaciones múltiples de Tukey, con un nivel de significancia de α = 0,05. Los análisis se efectuaron utilizando el software InfoStat, versión 2020 (Di Rienzo et al. 2020).
Los ejemplares de P. mesopotamicus se distribuyeron en grupos control (C) y tratados (T), analizándose un total de 1.100 metafases mitóticas para determinar la frecuencia de aberraciones cromosómicas (AC).
En el ensayo con 2,4-D puro (P) se evaluaron 100 metafases del grupo control y 450 del grupo tratado. En el control, el 96% de las metafases no presentó AC, mientras que el 4% mostró algún tipo de alteración cromosómica. En los grupos tratados, 399 metafases (89%) fueron normales y 51 (11%) presentaron AC.
En el ensayo con la formulación comercial 2,4-D Amina Sumagro® (FC) se analizaron 100 metafases en el grupo control y 450 en el tratado. En el control, el 97% de las metafases no presentó AC y el 3% evidenció alteraciones. En el grupo tratado, 396 metafases (88%) fueron normales y 54 (12%) mostraron aberraciones cromosómicas.
Las aberraciones observadas incluyeron gaps, fracturas, adhesividad cromosómica, endomitosis y pulverización (Figura 1).
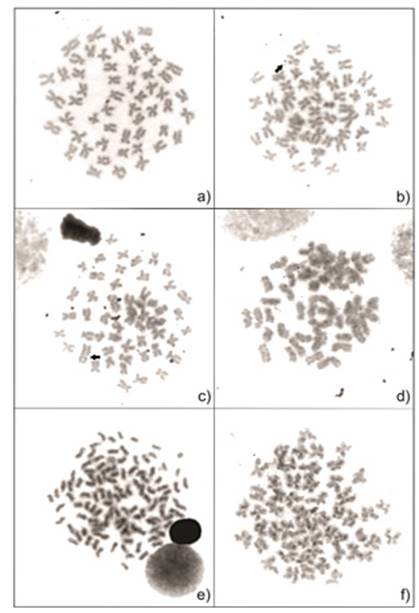
Al comparar cada concentración de 2,4-D con su respectivo control, tanto para la formulación pura como para la comercial, no se registraron diferencias significativas entre los tratamientos individuales (Figuras 2 y 3). Asimismo, no se observaron diferencias entre las formulaciones P y FC (Figura 4).
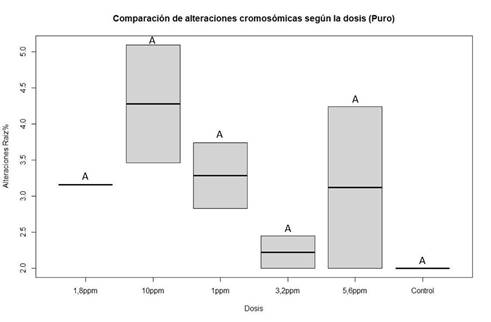
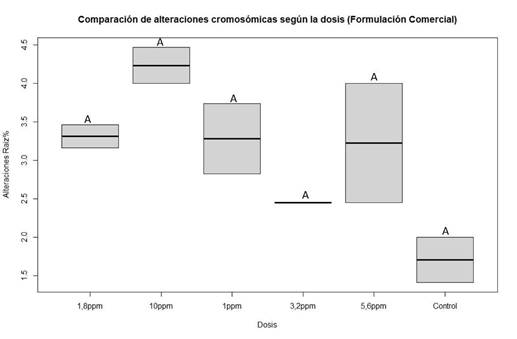
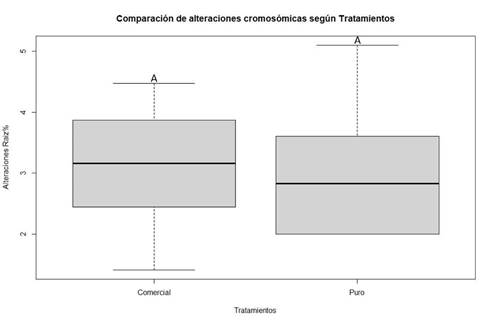
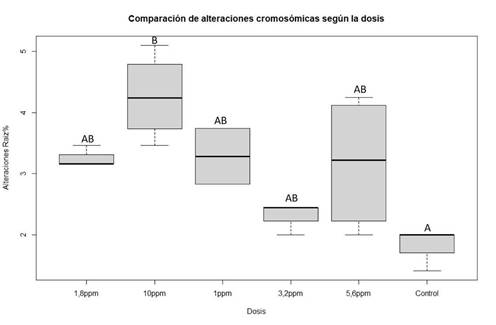
Sin embargo, al agrupar las concentraciones equivalentes de ambos ensayos, se determinó que las concentraciones de 1 ppm, 1,8 ppm, 3,2 ppm y 5,6 ppm no difirieron significativamente del control, mientras que la concentración de 10 ppm mostró una diferencia estadísticamente significativa (Figura 5). Este resultado sugiere una posible relación dosis-dependiente entre la exposición al 2,4-D y la aparición de alteraciones cromosómicas en P. mesopotamicus.
Considerando el impacto inmediato del herbicida 2,4-D sobre las especies acuáticas, resulta pertinente analizar su clasificación toxicológica según los organismos reguladores. De acuerdo con la Oficina del Programa de Pesticidas de la EPA, el 2,4-D se considera un compuesto de baja ecotoxicidad para peces (Borges et al. 2004). Sin embargo, la Organización Mundial de la Salud lo clasifica como moderadamente peligroso (categoría II) (WHO 2019).
El 2,4-D es un herbicida de amplia utilización agrícola y de creciente relevancia ambiental, que ha demostrado efectos tóxicos tanto in vitro como in vivo (Laborde 2024). Estudios en larvas de pez cebra (Danio rerio) evidenciaron su capacidad para alterar la expresión génica y comprometer la integridad del ADN (Gaaied et al. 2022), destacando la necesidad de evaluar no solo los efectos agudos, sino también las posibles consecuencias genotóxicas a largo plazo en los ecosistemas acuáticos.
Los resultados del presente estudio mostraron que los ensayos con 2,4-D puro y con la formulación comercial (Sumagro®) presentaron frecuencias similares de aberraciones cromosómicas, sin diferencias significativas entre tratamientos. Las alteraciones observadas (gaps, fracturas, adhesividad, endomitosis y pulverización) coinciden con las reportadas en bioensayos con otros plaguicidas en distintas especies de peces. Rishi y Grewal (1995) reportaron en Channa punctatus expuestos a diclorvos la presencia de gaps, fracturas y adhesividad; Das y John (1999) observaron efectos similares en Etroplus suratensis tratados con metilparatión y fosfamidón; y Chandra y Khuda-Bukhsh (2004) describieron fracturas cromosómicas en Oreochromis mossambicus tras exposición a azadiractina. De manera análoga, Ramadan (2007) y Caramello et al. (2017) hallaron en O. niloticus y Prochilodus lineatus, respectivamente, un incremento significativo de alteraciones cromosómicas luego de la exposición a distintos herbicidas.
En cuanto a estudios específicos con 2,4-D en peces, la información disponible es escasa. Farah et al. (2006) fueron los primeros en evidenciar el potencial genotóxico del 2,4-D mediante el ensayo de aberraciones cromosómicas, observando fracturas y pulverización en Channa punctatus expuestos a 75 ppm del herbicida durante 48-96 h. A diferencia de dichos autores, en el presente trabajo sólo se registraron diferencias significativas a la dosis de 10 ppm cuando se agruparon los ensayos de 2,4-D puro y comercial, probablemente debido a las diferencias en dosis y tiempo de exposición.
Resultados similares fueron reportados por Zafra-Lemos et al. (2021) en Astyanax lacustris, quienes hallaron aberraciones cromosómicas significativas a concentraciones de 10-40 mg L⁻¹. La discrepancia entre los resultados de esos autores y los obtenidos en Piaractus mesopotamicus podría explicarse por la mayor duración de la exposición en el presente estudio, lo que permitiría mecanismos de reparación del ADN.
Según Valbuena et al. (2020), los plaguicidas pueden inducir lesiones en el ADN cuya naturaleza depende del tipo de compuesto, su concentración y el tiempo de exposición. Sin embargo, los estudios que cuantifican el tipo y frecuencia de aberraciones cromosómicas en peces expuestos a plaguicidas siguen siendo escasos. Aldana-Salazar et al. (2024) destacan que, además del estrés oxidativo y las alteraciones epigenéticas, polimorfismos genéticos en genes asociados con la reparación del ADN, el metabolismo de xenobióticos y el control del ciclo celular podrían influir en la susceptibilidad diferencial de las especies a estos compuestos.
Carriquiriborde (2021) señala que el daño genético inducido por sustancias genotóxicas resulta de su interacción directa con la molécula de ADN, generando lesiones como rupturas, fusiones, deleciones, amplificaciones o errores en la segregación cromosómica. En el caso del 2,4-D, si bien los mecanismos de acción aún no están completamente dilucidados, se ha propuesto que su efecto genotóxico podría estar asociado al estrés oxidativo derivado de la formación de radicales libres electrofílicos capaces de interactuar con el ADN (Farah et al. 2006, Mesnage et al. 2021).
En conclusión, los resultados obtenidos sugieren una posible relación dosis-respuesta entre la concentración del herbicida y la estabilidad cromosómica al considerar conjuntamente los tratamientos con 2,4-D puro y comercial. La ausencia de diferencias significativas entre tratamientos individuales podría deberse a variaciones en las concentraciones empleadas, el tiempo de exposición o una baja sensibilidad de P. mesopotamicus al 2,4-D.
Los autores declaran que no existen conflictos de intereses relacionados con la realización de este estudio.
Contribución de los autores. CCF: realizó los experimentos, procesó los datos experimentales, realizó el análisis y redactó el artículo con la colaboración de todos los autores. JMJ: colaboró con el análisis formal de los datos. JLC: colaboró con las muestras.
Declaración de conflictos de intereses. Los autores declaran no tener conflictos de intereses financieros ni relaciones personales conocidas que pudieran haber influido en el trabajo presentado en este artículo.
Disponibilidad de datos. Los datos estarán disponibles previa solicitud.