Revista Veterinaria. 2026; 37(1)
https://doi.org/10.30972/vet.3719102
Revisión bibliográfica




1Medicina Veterinaria, Facultad de Ciencias Agropecuarias, Grupo de Investigación de Salud Animal, Universidad Técnica de Ambato, Tungurahua, Ecuador.
Recibido: 01 septiembre 2025 / Aceptado: 10 diciembre 2025
Resumen
La infección por el virus del distemper canino (VDC) constituye uno de los problemas sanitarios más relevantes en medicina veterinaria debido a su elevada capacidad de contagio, su notable diversidad genética y su impacto simultáneo en la fauna doméstica y silvestre. Esta revisión compiló información reciente sobre distintos aspectos del VDC, abarcando su etiología, transmisión, reservorios, impacto clínico y ecológico, así como los avances diagnósticos, las estrategias de prevención y las alternativas terapéuticas. Los estudios epidemiológicos muestran que los perros domésticos continúan siendo el principal foco de transmisión, especialmente cuando no cuentan con inmunización adecuada; sin embargo, numerosas especies silvestres incluyendo cánidos, félidos, mustélidos, úrsidos y prociónidos actúan como reservorios y amplificadores, favoreciendo la persistencia del virus en diversos ecosistemas. Además, la variabilidad genética del VDC, particularmente en el gen H, influye en su tropismo y patogenicidad, facilitando la emergencia de linajes con mayor capacidad de afectar el sistema nervioso o cruzar barreras interespecie. Los avances diagnósticos como la RT-qPCR y la secuenciación genómica han permitido detectar mutaciones relevantes y mejorar la vigilancia molecular. Por otro lado, las estrategias preventivas basadas en vacunas atenuadas y recombinantes han demostrado alta eficacia en perros y algunas especies silvestres, aunque su respuesta es variable según el hospedador. Las nuevas aproximaciones terapéuticas como las nanopartículas de plata o los inhibidores metabólicos representan alternativas prometedoras que podrían mejorar la supervivencia en animales afectados. En conjunto, la evidencia disponible confirma que el VDC persiste como una amenaza multiespecie cuya dinámica depende de la interacción entre perros domésticos y fauna silvestre, lo que refuerza la necesidad de fortalecer la vigilancia molecular y optimizar las estrategias de prevención para mitigar sus repercusiones sanitarias y ecológicas.
Palabras clave: virus del distemper canino, fauna silvestre, Canis lupus familiaris, Morbillivirus.
Abstract. Canine distemper virus (CDV) infection is one of the most significant health problems in veterinary medicine due to its high transmissibility, notable genetic diversity, and simultaneous impact on domestic and wild animals. This review compiles recent information on various aspects of CDV, including its etiology, transmission, reservoirs, clinical and ecological impact, as well as diagnostic advances, prevention strategies, and emerging therapeutic alternatives. Epidemiological studies indicate that domestic dogs remain the primary source of transmission, particularly when vaccination coverage is insufficient. However, numerous wild species—including canids, felids, mustelids, ursids, and procyonids—act as reservoirs and amplifiers, contributing to the virus's persistence in diverse ecosystems. The genetic variability of CDV, particularly in the H gene, influences its tropism and pathogenicity, facilitating the emergence of lineages with increased neurovirulence or enhanced ability to cross interspecies barriers. Diagnostic tools such as RT-qPCR and genomic sequencing have improved the detection of relevant mutations and strengthened molecular surveillance. Preventive strategies based on attenuated and recombinant vaccines have shown high efficacy in dogs and some wild species, although immune response may vary across hosts. Additionally, new therapeutic approaches, including silver nanoparticles and metabolic inhibitors, offer promising alternatives that could improve survival in affected animals. Overall, current evidence confirms that CDV remains a multispecies threat whose epidemiology depends on the complex interaction between domestic dogs and wildlife. This underscores the need to strengthen molecular surveillance and optimize prevention strategies to mitigate its health and ecological consequences.
Key words: canine distemper virus, wildlife, Canis lupus familiaris, Morbillivirus.
Esta patología se manifiesta a través de una amplia gama de signos clínicos, predominantemente sistémicos, incluyendo fiebre, secreción nasal, dificultad respiratoria, tos seca, vómitos, diarrea, anorexia y deshidratación; conforme la infección progresa en el organismo del hospedador, aumentan las probabilidades de que se presenten afecciones neurológicas graves, como: ataxia, convulsiones y parálisis (Wu et al. 2021). Un estudio realizado en las Islas Galápagos en 2019 reveló la gravedad del problema: de un total de 125 perros evaluados, 93 resultaron positivos para VDC, lo que representa una tasa de positividad del 74,4% (Vega-Mariño et al. 2023).
A pesar de la creencia común de que esta infección se limita a animales domésticos, existe amplia evidencia que contradice dicha suposición. En Nepal se realizó un estudio en 2014 que ofrece la primera evidencia de infección por VDC en carnívoros silvestres, específicamente en leopardos con anticuerpos desarrollados para VDC, en los cuales 3 de los 6 leopardos que se capturaron tenían signos de disnea, déficits neurológicos y pérdida de peso. Tan solo 6 años después, entre 2020-2022 se informaron la muerte de otros 5 leopardos con convulsiones agudas, que está relacionado al virus del distemper canino (VDC) (McDermott et al. 2023).
De igual forma, la detección de casos de infección en primates no humanos despierta gran preocupación, ya que abre la posibilidad de un riesgo zoonótico. La aparición del moquillo en focas (VMF) la cual surgió a partir del VDC a través del contacto entre carnívoros terrestres y focas, lo que explica su capacidad de propagación entre múltiples especies marinas y terrestres. Un ejemplo de ello fue la transmisión de la enfermedad a visones que habitaban cerca de focas enfermas en Europa a finales de la década de 1990 (Kennedy et al. 2019).
Por lo tanto, nuestro objetivo es sintetizar los hallazgos científicos mediante una revisión bibliográfica, destacando cómo el VDC afecta a la fauna doméstica y silvestre, documentar casos reportados y cuales especies actúan como reservorios, provocando así, que muchas más sean susceptibles.
Metodología. La presente revisión se desarrolló bajo un enfoque sistemático, utilizando como referencia los lineamientos PRISMA, tal como se muestra en la Figura 1. La recopilación de información se efectuó en bases de datos científicas como Scopus, PubMed y Google Académico, además de incluir literatura gris proveniente de tesis y repositorios institucionales. El proceso de búsqueda comprendió publicaciones hasta el año 2025, abarcando documentos tanto en inglés como en español.

La búsqueda bibliográfica se realizó mediante combinaciones de palabras clave y operadores booleanos, tales como: “canine distemper virus” OR “virus del distemper canino” AND “wildlife” OR “fauna silvestre” AND “domestic dogs” OR “perros domésticos”. También se incluyeron términos específicos como “Morbillivirus”, “seroprevalence” y “transmission”.
Criterios de inclusión:
Reportes de casos en fauna doméstica o silvestre relacionada con VDC.
Artículos originales, revisiones, tesis o documentos con datos epidemiológicos, clínicos o moleculares sobre el virus.
Investigaciones que evaluaran factores de riesgo, prevalencia, transmisión o impacto ecológico.
Publicaciones disponibles a texto completo en inglés o español.
Trabajos centrados en otros Morbillivirus no relacionados con VDC.
Documentos duplicados.
La selección de literatura se llevó a cabo en tres etapas consecutivas: revisión de títulos, análisis crítico de resúmenes y lectura completa del documento. De cada estudio se extrajeron variables como autores, año, especie afectada, región geográfica, método diagnóstico empleado y hallazgos relevantes sobre prevalencia, transmisión y factores de riesgo asociados al distemper canino.
Etiología y características del virus. El virus del distemper canino (VDC) es un Morbillivirus de la familia Paramyxoviridae, estrechamente relacionado con el virus del sarampión y el de la peste bovina. Posee un genoma de ARN monocatenario negativo, no segmentado, de 15 690 nt, que codifica ocho proteínas (F (fusión), H (hemaglutinina), N (nucleocápside), M (matriz), P (fosfoproteína), L (polimerasa)) (Duque-Valencia et al. 2019). Estructuralmente es pleomórfico, con envoltura lipídica, donde destacan la hemaglutinina (H), que media la unión a receptores, y la proteína de fusión (F), esencial para la entrada viral. El receptor principal de los Morbillivirus es la molécula SLAM/CD150 en células inmunitarias, cuya infección conduce a inmunosupresión marcada y linfopenia; algunas cepas de laboratorio utilizan receptores alternativos como CD46 (Tatsuo y Yanagi 2002). La variabilidad genética del VDC, en particular en la proteína H, y la acción de las proteínas V y C que inhiben la respuesta de interferón, complican su control mediante vacunas (Rendon-Marin et al. 2019).
El genoma del virus del distemper canino (VDC) presenta una alta tasa de mutación, lo que contribuye a una notable diversidad genética. La proteína H desempeña un papel esencial en la determinación del tropismo celular y del rango de especies que puede infectar, ya que interactúa con el receptor SLAM presente en los tejidos linfoides. Este gen es el más variable dentro del genoma del virus, mostrando una divergencia de hasta un 8% entre aislados de campo y hasta un 11% en comparación con las cepas utilizadas en vacunas (Rivera-Martínez et al. 2024).
Transmisión y patogénesis. El virus del distemper canino (VDC) es altamente contagioso y se transmite principalmente por vía aérea, iniciando su replicación en células inmunológicas que expresan el receptor SLAM/CD150 (Zhao et al. 2015, Shi et al. 2025). Los signos clínicos iniciales comprenden apatía, deshidratación, falta de apetito y disminución de peso, a los que posteriormente se suman manifestaciones más evidentes como la rinitis purulenta, conjuntivitis, hiperqueratosis y pústulas. Un rasgo típico de la enfermedad es la fiebre de carácter bifásico (Beineke et al. 2009). El desenlace de la infección depende principalmente de la virulencia de la cepa, la edad del individuo y su estado inmunológico. Una respuesta inmune humoral débil puede favorecer la viremia secundaria, mientras que una respuesta antiviral sólida puede eliminar el virus y permitir la recuperación. La viremia secundaria propaga el virus a tejidos epiteliales, mesenquimales y al sistema nervioso central, afectando principalmente mucosas bronquiales y gastrointestinales, queratinocitos y fibroblastos (Lempp et al. 2014). Produciendo una respuesta inflamatoria intensa en los pulmones, mediada por células inmunitarias innatas como macrófagos y células presentadoras de antígenos, lo que ocasiona neumonía y destrucción del tejido bronquial (Chludzinski et al. 2022).
Cuando la infección progresa a un compromiso nervioso, puede manifestarse una fase aguda tras semanas o meses, causando desmielinización aguda en donde la mayoría de los animales fallecen entre la segunda y cuarta semana posterior a la infección. Debido a su efecto inmunosupresor, los signos clínicos suelen agravarse por infecciones bacterianas secundarias en la piel y el tracto respiratorio. La diseminación en el sistema nervioso ocurre principalmente por vía hematógena, propagándose a través del líquido cefalorraquídeo y afectando la sustancia blanca ependimaria y subependimaria, así como otras áreas como el nervio olfatorio y las meninges (Loots et al. 2017, Oliver 2023). En diversas especies silvestres se ha evidenciado un fuerte tropismo neurológico y una marcada capacidad de inmunosupresión. En una comunidad de prociónidos neotropicales, como mapaches (Procyon lotor) y coatíes de cabeza blanca (Nasua narica), se observaron signos agudos como fiebre, secreciones oculares y nasales, conjuntivitis, diarrea, vómitos, erupciones cutáneas, linfopenia y síntomas neurológicos consistentes con encefalitis. Estudios en tigres de Amur (Panthera tigris) apuntan a que el virus ha emergido como una amenaza de extinción para esta especie; los casos letales incluyen progresión a enfermedad neurológica fatal, donde los animales presentan signos graves que culminan en convulsiones y muerte (Gilbert et al. 2020, Rodríguez-Cabo-Mercado et al. 2020, Vandevelde y Zurbriggen 2005).
Especies susceptibles. Los perros domésticos han sido considerados históricamente como los principales huéspedes del virus del distemper canino. No obstante, debido a que el virus no se mantiene de forma latente en individuos recuperados, su persistencia depende de la transmisión continua hacia animales que aún no han desarrollado inmunidad. La envoltura lipídica del virus lo vuelve muy frágil fuera del organismo hospedador, lo que restringe su capacidad para permanecer viable en el ambiente, especialmente en climas templados (Wilkes 2023).
El perro no es el único huésped susceptible, el VDC tiene una capacidad notable para adaptarse a una gran variedad de especies, especialmente dentro del orden carnívora. Entre las primeras especies silvestres afectadas se encuentran el chacal plateado (Vulpes chama), tejón (Taxidea taxus) y diversos felinos. Con el pasar del tiempo, se ha confirmado que varios carnívoros salvajes cumplen una función significativa en la circulación del virus, especialmente en regiones donde la vacunación en perros ha reducido su papel como fuente principal de infección (Martinez-Gutierrez y Ruiz-Saenz 2016).
El rango de hospedadores del VDC se ha ampliado significativamente, extendiéndose a familias como Procyonidae, Ailuridae, Ursidae, Mustelidae, Felidae, Viverridae, Hyaenidae, Myrmecophagidae y Choloepodidae, lo que demuestra su versatilidad biológica (Tabla 1) (Beineke et al. 2015, Watson et al. 2020).

ALA: ácido alfa-linolénico (18:3n-3), EPA: ácido eicosapentaenoico (20:5n-3), DHA: ácido docosahexaenoico (22:6n-3).
Impacto en la fauna doméstica. El virus del distemper canino (VDC) continúa siendo una amenaza crítica para los perros domésticos, en especial para aquellos sin vacunación, donde la prevalencia alcanza entre el 33% y el 46% en animales sospechosos. Se ha evidenciado que los perros callejeros y no vacunados presentan un riesgo significativamente mayor de resultar positivos. En contraste, los perros vacunados, mostraron una menor probabilidad de infección (Da Costa et al. 2019).
Se han descrito daños cardíacos relevantes. Según Kim et al. (2021), en un estudio retrospectivo en cachorros de 4 a 7 semanas reveló la presencia de miocarditis multifocal, caracterizada por infiltración de linfocitos, neutrófilos y macrófagos, necrosis, fibrosis miocárdica y, en un caso, cuerpos de inclusión intracitoplasmáticos en cardiomiocitos, hallazgo poco frecuente pero característico de esta infección (Kim et al. 2021).
A diferencia de otros casos analizados de cachorros entre 2,5 y 4 meses que desarrollaron esclerosis metafisaria en huesos largos. Estos animales presentaron síntomas neurológicos severos, incluyendo convulsiones y temblores, junto con complicaciones respiratorias como neumonía y signos sistémicos como letargo y fiebre. El estudio demostró que la esclerosis metafisaria simétrica visible en radiografías sirve como un marcador distintivo del VDC, diferenciándolo de otras enfermedades óseas como la osteopatía metafisaria (Johnson et al. 2022).
En el Hospital Veterinario de la Universidad Ferdowsi de Mashhad evidenció su alto impacto epidemiológico y clínico en la población canina. La prevalencia general fue del 4,04 % en todos los animales atendidos y ascendió al 7,44 % en aquellos que presentaban signos clínicos compatibles con la infección. La enfermedad mostró una elevada tasa de mortalidad, alcanzando el 69,57 %, lo que refleja su carácter letal en ausencia de medidas preventivas eficaces (Mousafarkhani et al. 2023).
Impacto en la fauna silvestre. Los primeros casos documentados de distemper canino en especies no caninas se remontan a 1937, cuando se reportó un brote en chacales plateados (V. chama) en un zoológico de Johannesburgo, seguido por la detección del virus en tejones americanos (T. taxus) en colorado en 1942. Estos eventos marcaron el inicio del reconocimiento del VDC como una amenaza para la vida silvestre. Posteriormente, en la década de 1960, se identificaron infecciones en primates no humanos, como macacos japoneses (Macaca fuscata), y en la década de 1990, un brote devastador en leones del Serengueti causo la muerte de un tercio de la población (Martinez-Gutierrez y Ruiz-Saenz 2016).
En Europa durante la última década, al noroeste de Italia, se detectaron brotes recurrentes entre 2018 y 2021, con una mortalidad elevada en zorros rojos (V. vulpes) y la identificación de dos linajes distintos del virus: Europe/South America-1 y European Wildlife. Estos brotes estuvieron asociados con mutaciones en la proteína H, como la Y549H, vinculada a una mayor virulencia y tropismo neuronal (Trogu et al. 2022).
Entre 2022 y 2024 en Campania (Italia), se examinaron muestras de tejido de 136 animales silvestres -como tejones, zorros, lobos y martas- y se detectó ARN de VDC en 14 (10,3%), correspondieron a tejones (M. meles), zorros (V. vulpes), lobos (C. lupus italicus) y una marta (M. martes); los hallazgos post mortem más frecuentes incluyeron congestión pulmonar (y posiblemente traqueal) en cuatro animales (28,5%) y enteritis en tres (21,4%); las causas de muerte en estos casos fueron tanto infección como trauma en igual proporción, lo que sugiere que la debilidad inducida por el virus puede predisponer a lesiones traumáticas, como choques vehiculares, en la fauna silvestre analizada (Alfano et al. 2025).
Estudios realizados en Asturias (España) entre 2020 y 2021 confirmaron la circulación endémica del VDC en tejones (M. meles), con una seroprevalencia del 43,4% y brotes esporádicos que causaron mortalidad en mustélidos y cánidos. La cepa detectada pertenecía al linaje europeo, con una distribución espacial vinculada a zonas de alta densidad humana, lo que sugiere un posible rol de los perros domésticos como reservorios. La patología mostró afectación del sistema nervioso central y pulmones, con inmunotinción positiva en neuronas y epitelio respiratorio, indicando una alta patogenicidad (Oleaga et al. 2022).
La subpoblación de lobos de los Apeninos en el centro de Italia sufrió un brote de VDC en 2013 provocó la muerte de al menos 30 individuos, lo que tuvo consecuencias potencialmente devastadoras para esta población restringida geográficamente. En contraste, los lobos ibéricos (C. lupus signatus) mostraron una mayor inmunidad a nivel poblacional, con infecciones detectadas principalmente entre 2005 y 2008, mientras que los lobos alpinos (C. lupus) han sido menos afectados por los eventos epidémicos severos que impactaron a la fauna silvestre del norte de Italia desde 2006 (Di Francesco et al. 2020).
En el Parque Nacional de Emas, en la sabana del Cerrado de Brasil central, se recolectaron muestras de suero de 169 individuos de especies como lobo guará (Chrysocyon brachyurus), zorro cangrejero (C. thous), gato pampeano (L. colocolo), yaguarundí (Herpailurus yagouaroundi) y coatí (N. nasua). Los resultados muestran que el 10,6% de los carnívoros silvestres, específicamente lobos guará, zorros cangrejeros y ocelotes, presentaron anticuerpos contra el VDC, indicando exposición previa, aunque sin casos clínicos activos durante el estudio (Furtado et al. 2016).
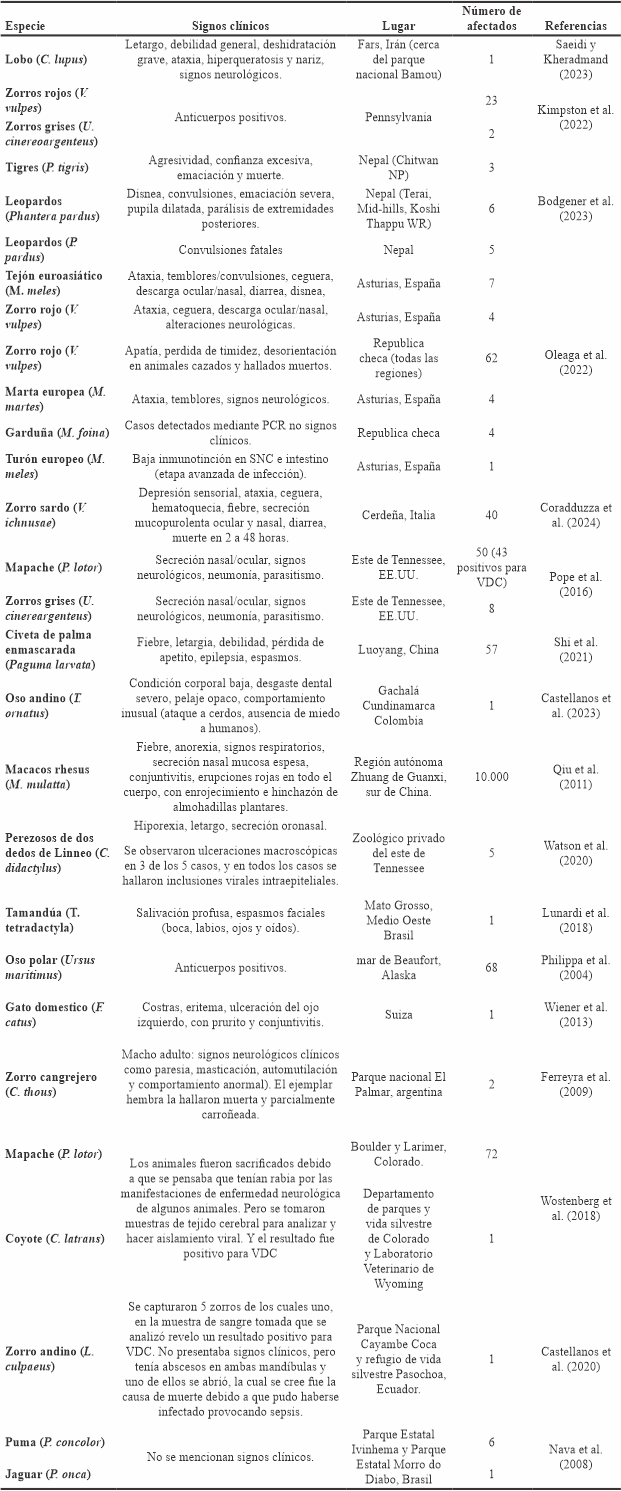
Estas epidemias de VDC han revelado su alta mortalidad en carnívoros, afectando a poblaciones silvestres y contribuyendo a la disminución y posible extinción de especies en peligro (Duque-Valencia et al. 2019). En la Tabla 2 se sintetiza la información disponible sobre algunos casos de VDC en fauna silvestre.
ALA= ácido alfa-linolénico (18:3n-3), EPA= ácido eicosapentaenoico (20:5n-3), DHA= ácido docosahexaenoico (22:6n-3).
Factores de riesgo. En el último siglo la población humana ha crecido de forma acelerada, generando una mayor presión sobre los ecosistemas a través del uso intensivo del suelo y la explotación de los recursos naturales. Como resultado, muchas especies silvestres se ven obligadas a sobrevivir en hábitats cada vez más fragmentados y modificados por la actividad humana, lo que incrementa sus interacciones con las personas y sus entornos (Balseiro et al. 2024).
Partiendo de esa premisa la transmisión del VDC entre perros domésticos no vacunados y especies silvestres, es un factor crítico en la propagación de la enfermedad (Macías-González et al. 2025). Estudios en México e Irak destacan en perros callejeros actúan como reservorios, facilitando el salto del virus a otros animales de campo. En Irak se observó que el 19,62% de los perros callejeros presentaban infección crónica, lo que sugiere una transmisión sostenida debido a la ausencia de inmunización. De igual manera, en México la vacunación irregular en mascotas no tradicionales amplia el rango de huéspedes susceptibles (Mohammad et al. 2022).
Se cree que el clima y la estación del año son otros factores que pueden influir en la prevalencia del VDC. Esto debido a que Liang et al. (2024) en su investigación mostró que la prevalencia del VDC era más alta en la franja comprendida entre 120°E-180° de longitud y 30°-60°N de latitud. Sus resultados indican que Asia y América del Norte se ubican dentro de este mismo sector geográfico. Además, ambos continentes presentan un clima templado influenciado por el monzón y comparten condiciones ambientales similares, caracterizadas por marcadas variaciones térmicas a lo largo del año e inviernos fríos. Estas particularidades coincidieron con sus hallazgos obtenidos, que evidencian un incremento de casos durante la estación invernal. En contraste con Dorji et al. (2020) que mediante estudio en Bután encontró que los perros muestreados en invierno tenían menor probabilidad de ser seropositivos al VDC en comparación con los muestreados en verano, pero la prueba ELISA al no alcanzar una sensibilidad y especificidad absoluta, es posible que algunas muestras hayan presentado falsos positivos o falsos negativos. Por lo que sugiere interpretar esos resultados con prudencia.
A pesar de esto Alfano et al. (2022), sostiene que los linajes genéticos del VDC se distribuyen de manera distinta entre regiones, pero no varían en función de la especie infectada. Además, la frecuencia de la enfermedad cambia a lo largo del tiempo y tiende a incrementarse durante estaciones más frías.
En los últimos años, las técnicas moleculares han revolucionado el diagnóstico del VDC, destacando la RT-qPCR por su alta sensibilidad y especificidad. Este método, basado en sondas TaqMan dirigidas a los genes N y P del virus, permite una detección rápida y cuantificación precisa del ARN viral en muestras clínicas, superando a otras pruebas tradicionales (Martinez-Gutierrez y Ruiz-Saenz 2016, Dorji et al. 2020).
Prueba de esto fue el caso de un perro vacunado signos de distemper del cual se recibió una muestra sanguínea, y mediante RT-PCR dirigida al gen NP se confirmó la infección. A partir de las PBMC aisladas se inocularon distintas líneas celulares, observándose amplificación por RT-PCR únicamente en B95a y VeroSLAM, esta última mostrando además el efecto citopático típico. El virus obtenido fue denominado Arg 24, cuyo pasaje 3 alcanzó 3.86×10⁴ DICT₅₀/ml. La cinética viral en VeroSLAM reveló un mayor título de virus asociado a células que en el sobrenadante. El análisis genético por RT-PCR y secuenciación demostró que Arg 24 presenta marcadas diferencias con la cepa vacunal, incluyendo nuevos sitios de N-glicosilación en H y F. El análisis filogenético confirmó su pertenencia a un clado distinto al vacunal, validando así el primer aislamiento de una cepa salvaje de VDC en Argentina (Romanutti et al. 2017).
La secuenciación genómica ha adquirido un papel crucial, especialmente con el uso de tecnologías de secuenciación de próxima generación, que facilitan la caracterización completa de cepas circulantes y la identificación de mutaciones relevantes. Un ejemplo notable es su aplicación durante un brote en zorros en Hungría en 2021, donde se obtuvieron 19 genomas completos de VDC (Lanszki et al. 2022).
Por otro lado, los ensayos serológicos han evolucionado hacia formatos más rápidos y accesibles. El diagnostico mediante ELISA sigue siendo una herramienta clave, con versiones mejoradas que detectan anticuerpos IgM e IgG con una sensibilidad del 94% y especificidad del 91,8% incluso en etapas tempranas de infección (Hassenin et al. 2023). La microscopia electrónica de transmisión sigue siendo valiosa para estudios patológicos, permitiendo visualizar partículas virales y daños tisulares en modelos animales, como en mapaches infectados (Stancu et al. 2023). No obstante, su uso en diagnóstico rutinario ha disminuido debido al auge de técnicas moleculares más rápidas y menos costosas. Estos avances reflejan un enfoque integrado que combina rapidez, precisión y accesibilidad para el control del VDC en diversas poblaciones de animales (Wilkes et al. 2014, Lanszki et al. 2022).
Se debe destacar el uso de vacunas vivas modificadas y los virus recombinantes, aunque también se han probado formulaciones inactivadas y basadas en ADN. En perros y visones, estas vacunas han demostrado una protección global cercana al 98%, con tasas de supervivencia superiores al 80%, mientras que en especies como mapaches, zorros y turones siberianos se han alcanzado resultados de hasta un 100% de supervivencia tras la inmunización (Rendon-Marin et al. 2024).
En una revisión se analizó la respuesta a la vacunación contra el distemper canino en 812 grandes felinos, incluyendo tigres, leones, leopardos de las nieves, jaguares y leopardos. En total se registraron 2.846 aplicaciones, predominando las vacunas con vector de viruela del canario, que mostraron una tasa mínima de efectos adversos (0,5%). Las vacunas de virus vivo modificado, utilizadas únicamente en tigres, leones y leopardos de las nieves, también presentaron pocas reacciones (2,9%). Los resultados serológicos de 159 individuos vacunados evidenciaron que el 66 % desarrolló títulos protectores, con mayor seroconversión tras esquemas con varias dosis. Además, la mayoría de los felinos que respondieron mantuvieron niveles de anticuerpos durante 12 a 36 meses, demostrando así que estas especies desarrollan una inmunidad efectiva y duradera frente al distemper canino mediante la vacunación (Georoff et al. 2020).
No obstante, la eficacia de la vacunación varía según la especie y el tipo de formulación empleada. En mapaches salvajes, la vacuna recombinante Purevax generó una respuesta inmunitaria moderada, con solo un 67% de los animales seronegativos desarrollando anticuerpos neutralizantes tras un refuerzo, lo que evidencia la influencia de factores como los anticuerpos maternos en la respuesta humoral (Selleck et al. 2024). En especies en peligro, como los pandas gigantes, las vacunas diseñadas para perros han mostrado ser limitadas, pues si bien inducen una fuerte respuesta inmune innata y celular, la producción de anticuerpos y células de memoria es insuficiente para garantizar protección a largo plazo, lo que resalta la necesidad de desarrollar vacunas específicas o adyuvantes que optimicen la inmunogenicidad en estas especies (Geng et al. 2020).
Según Rendon-Marín et al. (2024) realizaron una recopilación de vacunas contra el VDC en animales domésticos y silvestres e identificaron que las vacunas atenuadas y recombinantes son las más utilizadas, con altas tasas de supervivencia post-desafio en perros y visones. El control de epidemias es importante mediante cuarentenas y tratamientos para disminuir su contagiosidad. Propuso exámenes en individuos sanos para identificar casos tempranos, campañas de inmunización contra el VDC, también implementar medidas ambientales como limitar el ingreso de perros y gatos en áreas protegidas (Suwanpakdee et al. 2025, Tonchiangsai et al. 2025).
Sistémico. Actualmente no existen antivirales aprobados contra el virus del distemper canino (VDC), por lo general se sigue una terapia de soporte la cual consta en administrar antibióticos de amplio espectro como ampicilina o amoxicilina-clavulánico para complicaciones como neumonía causada bacterias. La fluidoterapia es esencial en todos los casos para combatir la deshidratación por vómitos, diarreas o anorexia, administrando soluciones electrolíticas balanceadas por vía intravenosa. Se pueden suministrar vitaminas del grupo B para reemplazar pérdidas por anorexia y diuresis, estimulando el apetito, junto con posibles beneficios del ácido ascórbico intravenoso. Los antipiréticos están justificados en fiebres superiores a 40 °C (Pinotti 2011).
Sin embargo, se han explorado alternativas prometedoras. Un estudio clínico demostró que el uso de nanopartículas de plata (AgNPs), administradas por vía oral o nasal junto con terapia de soporte, incrementó notablemente la supervivencia de perros domésticos infectados, alcanzando un 84,6% en casos no neurológicos y un 65,5% en neurológicos, además de reducir la progresión de síntomas graves y favorecer la recuperación sin secuelas en un alto porcentaje de animales (Gastelum-Leyva et al. 2022).
Por otro lado, investigaciones in vitro han evidenciado que el compuesto A77 1726, metabolito activo de la leflunomida, inhibe la replicación del VDC al bloquear rutas metabólicas esenciales para la síntesis de pirimidinas, reduciendo la producción de proteínas virales y nuevas partículas infecciosas. Estos resultados sugieren que tanto las AgNPs como los inhibidores metabólicos representan estrategias terapéuticas con gran potencial para mejorar la calidad de vida y supervivencia en perros domésticos afectados por esta enfermedad (Li et al. 2021).
Neurológico. La acupuntura combinada con electroacupuntura demostró una efectividad significativa en el tratamiento de perros con secuelas neurológicas del virus del distemper canino (VDC), según el estudio clínico realizado en 24 perros infectados que recibieron sesiones semanales durante 24 semanas. Las puntuaciones neurológicas mejoraron notablemente desde la semana 7 hasta la 24 en comparación con los valores previos al tratamiento (p<0,001). En cuanto a la recuperación funcional de las extremidades, el 75% de los perros restableció la locomoción en 16 semanas, y al final del tratamiento, el 79,2% (19/24) recuperó la ambulación funcional; además, el 95,8% (23/24) mostró respuestas normales en propiocepción, postura y salto al final (p<0.001 para cada uno). El mioclonus, presente en el 50% (12/24) de los perros antes del tratamiento, mejoró en el 100% de los casos afectados, con reversión completa en el 25% (3/12) y mejora parcial en el 75% (9/12). La función urinaria, anormal en el 20,8% (5/24), se recuperó en todos los casos afectados para la semana 21 (Santos et al. 2022).
Otros tratamientos poco convencionales, para tratar perros domésticos con signos neurológicos de distemper consistió en la inyección en el espacio subaracnoideo de 0,10 a 0,50 mL de la vacuna contra la enfermedad de Newcastle, después de retirar entre 0,10 y 1,00 mL de líquido cefalorraquídeo (LCR), seguida de la inyección de 0,50 a 1,00 mL de solución salina para limpiar la aguja. La vacuna utilizada fue la viva atenuada LaSota o B1. De nueve perros en los que se confirmó la infección por distemper con distintas pruebas, dos perros (22,2%) mostraron mejoría significativa tras el tratamiento: uno se recuperó completamente y otro mejoró considerablemente. Un tercer perro, cuyas pruebas para distemper fueron negativas, pero tenía signos clínicos, también mejoró significativamente. No se observaron efectos secundarios específicos causados por la inyección de la vacuna (Sarchahi et al. 2022).
Cabe recalcar que dichos tratamientos aplicados, no fueron probados en animales silvestres. En los casos donde se logró aplicar un tratamiento, los resultados no alcanzaron la eficacia esperada, tal es el caso de una Tamandúa (T. tetradactyla) la cual fue tratada con antibióticos, antiepilépticos, antioxidantes y terapia de apoyo. Se realizaron muchos esfuerzos, pero sufrió una convulsión que derivó en la ingestión de su propia lengua; ante el avance de la enfermedad y el mal pronóstico, se optó por la eutanasia (Lunardi et al. 2018).
El distemper canino continúa consolidándose como una de las enfermedades virales con mayor impacto sanitario y ecológico, dada su amplia capacidad para infectar múltiples especies y su tendencia a generar brotes con alta mortalidad en perros domésticos y en carnívoros silvestres. Los tratamientos disponibles se centran en la terapia de soporte en perros, mientras que los reportes en fauna silvestre evidencian escasa respuesta terapéutica y, frecuentemente, un pronóstico fatal. Esto evidencia una brecha significativa en el manejo clínico de especies silvestres afectadas.
Resulta prioritario llevar a cabo investigaciones sistemáticas que incluyan la vigilancia tanto de perros domésticos como de carnívoros silvestres que se desplazan dentro y en los alrededores de distintas áreas protegidas (Castellanos et al. 2020). De igual manera, es fundamental registrar las variantes circulantes del VDC en estas poblaciones, con el fin de profundizar en los factores que favorecen la transmisión interespecie. Por último, se debe fortalecer el desarrollo de nuevos tratamientos antivirales y protocolos terapéuticos adaptados a la fisiología y necesidades de las especies silvestres.
Contribución de los autores. PBES: Redactó el artículo con la colaboración de todos los autores. AEDF: Planificación del tema y el contenido, el orden del contenido, revisión de citas y bibliografía.
Declaración de conflictos de intereses. Los autores declaran no tener conflictos de intereses financieros ni relaciones personales conocidos que pudieran haber influido en el trabajo presentado en este artículo.