Revista Veterinaria. 2026; 37(1)
https://doi.org/10.30972/vet.3719103
Artículo Original




1Universidad de los Llanos, Facultad de Ciencias Agropecuarias y Recursos Naturales, Escuela de Ciencias Animales, Grupo de investigación en Farmacología Experimental y Medicina Interna – Élite, Programa de Medicina Veterinaria y Zootecnia, Villavicencio 1745, Meta, Colombia.
2Universidad de los Llanos, Grupo de investigación en Farmacología Experimental y Medicina Interna – Élite, Programa de Medicina Veterinaria y Zootecnia, Villavicencio 1745, Meta, Colombia.
3Universidad de los Llanos, Facultad de Ciencias de la salud, Grupo de investigación en Farmacología Experimental y Medicina Interna – Élite, Programa de Medicina Veterinaria y Zootecnia, Villavicencio 1745, Meta, Colombia.
a mcgonzalez.prada@unillanos.edu.co
mcgonzalez.prada@unillanos.edu.co
c carolina.garcia@unillanos.edu.co
carolina.garcia@unillanos.edu.co
e dumar.jaramillo@unillanos.edu.co
dumar.jaramillo@unillanos.edu.co
Resumen
Las infecciones del sitio quirúrgico son una de las complicaciones más comunes, y la presencia de bacterias multirresistentes en entornos quirúrgicos incrementa el riesgo de infecciones nosocomiales. En veterinaria, es necesario identificar estos agentes para comprender su impacto y fortalecer las medidas de bioseguridad. Este estudio tuvo como objetivo identificar bacterias resistentes a antimicrobianos en áreas quirúrgicas de clínicas veterinarias en Villavicencio-Meta. Se seleccionaron tres clínicas con sala quirúrgica, avaladas por la Secretaría de Salud. En cada una se recolectaron muestras en tres estratos (mesa quirúrgica, sistema de aireación y piso) y en tres momentos del procedimiento (preoperatorio, intraoperatorio y posoperatorio). Las muestras fueron sembradas en medios de cultivo especializados y posteriormente se realizó antibiograma. Los aislamientos correspondieron a Bacillus spp. y Staphylococcus spp., con mayor frecuencia de Bacillus spp. en el piso y el aire, y predominio de Staphylococcus spp. en la mesa quirúrgica. No hubo diferencias significativas entre momentos quirúrgicos (p = 0,731), ni entre superficies de la sala quirúrgica (p = 0,374), pero sí entre quirófanos de las clínicas (p = 0,004), mostrando variaciones en la carga microbiana entre establecimientos. Bacillus spp. presentó resistencia a ciprofloxacina y norfloxacina, mientras que Staphylococcus spp. a rifampicina y un comportamiento variable frente a ciprofloxacino y trimetoprim. Estos hallazgos subrayan la necesidad de reforzar los protocolos de limpieza, antisepsia y desinfección en los quirófanos veterinarios para disminuir el riesgo de infecciones nosocomiales y la diseminación de bacterias resistentes.
Palabras clave: Antibióticos, resistencia antimicrobiana, infecciones nosocomiales.
Abstract. Surgical site infections are among the most common postoperative complications, and the presence of multidrug-resistant bacteria in surgical environments increases the risk of nosocomial infections. In veterinary medicine, identifying these agents is essential to assess their impact and to strengthen biosafety measures. This study aimed to identify antimicrobial-resistant bacteria in surgical areas of veterinary clinics in Villavicencio, Meta. Three clinics with authorized surgical rooms were selected. In each facility, samples were collected from three sites (surgical table, air-conditioning system, and floor) at three surgical stages (preoperative, intraoperative, and postoperative). Samples were cultured on selective media, followed by antimicrobial susceptibility testing. The isolates consisted mainly of Bacillus spp. and Staphylococcus spp., with Bacillus spp. being more frequently detected on the floor and in the air, and Staphylococcus spp. predominating on surgical tables. No significant differences were observed among surgical stages (p = 0.731) or among sampled surfaces within operating rooms (p = 0.374); however, significant differences were found among clinics (p = 0.004), indicating variability in microbial load between facilities. Bacillus spp. exhibited resistance to ciprofloxacin and norfloxacin, whereas Staphylococcus spp. showed resistance to rifampicin and variable resistance to ciprofloxacin and trimethoprim. These findings highlight the need to strengthen cleaning, antisepsis, and disinfection protocols in veterinary operating rooms to reduce the risk of nosocomial infections and limit the spread of antimicrobial-resistant bacteria.
Key words: Antibiotics, antimicrobial resistance, nosocomial infections.
Ante un procedimiento quirúrgico la infección del sitio quirúrgico (ISQ) representa un riesgo significativo, esta puede comprometer la evolución postoperatoria del paciente deteriorando la recuperación y aumentando la mortalidad y morbilidad. Según el estudio de Moretti et al. (2020) la ISQ puede tener múltiples orígenes, incluyendo la microbiota cutánea del paciente, así como factores relacionados al entorno quirúrgico, como el instrumental, las superficies, el aire ambiental e incluso el personal involucrado (Rodríguez et al. 2020, Stryja 2021).
La aparición de la ISQ está determinada por el grado de contaminación que se presente en la zona intervenida y la patogenicidad de los microorganismos, en equilibrio con la respuesta inmunitaria del huésped (Kalicha et al. 2025). Por ende, es fundamental el uso de medidas de bioseguridad para prevenir la entrada y propagación de agentes infecciosos, los cuales se pueden transmitir a través de fómites o superficies no estériles (Byers 2020).
Actualmente se ha comprobado que la presencia de microorganismos en superficies de contacto frecuente con pacientes incrementa el riesgo ISQ (Stevanović et al. 2019). Las bacterias son los microorganismos de mayor vigilancia y control en la práctica de antisepsia de los centros quirúrgicos, esto debido a su variada presencia, alta tasa de supervivencia y adaptabilidad a los distintos ambientes mediante los diferentes mecanismos que poseen, uno de ellos es la formación de biopelículas (Hrynyshyn et al. 2022). Llegando a ocasionar gran parte de las infecciones intraoperatorias, donde varía según el grado de intervención (Mellinghoff et al. 2023). La presencia de los géneros Bacillus y Staphylococcus, se ha aislado de forma prevalente en los ambientes quirúrgicos, a nivel de sus superficies (Tomé-Méndez et al. 2024).
La resistencia bacteriana es la capacidad que desarrollan ciertos microorganismos, como bacterias, para sobrevivir y multiplicarse a pesar del uso de antimicrobianos destinados a eliminarlos, lo que les permite persistir en el hospedero o en el ambiente tras el tratamiento antimicrobiano (OMS 2024). La administración indiscriminada de antibióticos ha fomentado que los microorganismos, al exponerse de manera continua a ellos, desarrollen resistencia y comprometan su eficacia terapéutica, dando aparición a una de las principales problemáticas de salud pública en la actualidad (Bashir et al. 2023).
Las bacterias multirresistentes, por su alta capacidad de diseminación en entornos clínicos, pueden permanecer viables durante semanas, esto depende de qué tan efectivos sean sus mecanismos de supervivencia en las superficies (Wißmann et al. 2021). Además, se ha evidenciado la presencia de microorganismos específicamente en la mesa de instrumental y en el flujo de aire del quirófano (Zuzkov et al. 2024). Por otro lado, en Colombia se han identificado bacterias multirresistentes como Pseudomonas, Streptococcus, Klebsiella, Staphylococcus en diversos centros clínicos veterinarios (Sánchez et al. 2015).
La limpieza y la desinfección tiene como fin ejercer un control sobre las concentraciones de microorganismos y reducir el grado de transferencia y contaminación cruzada (Assadian et al. 2021). Sin embargo, según lo descrito en el trabajo de Casini et al. (2023), después de la aplicación de los protocolos estándar de limpieza se ha encontrado un alto grado de contaminación en diversas superficies intrahospitalarias, al menos en un 64,7%. Esto puede atribuírsele al poco tiempo que se les permite a los productos ejercer su acción o por la poca rotación de desinfectantes la cual previene eventos de resistencia que predisponen al riesgo de presentar infecciones nosocomiales (Otter et al. 2011). El objetivo de este estudio fue determinar la presencia de agentes microbianos multirresistentes en salas quirúrgicas de centros hospitalarios veterinarios, de la ciudad de Villavicencio.
Delimitación del muestreo. El estudio se llevó a cabo en tres clínicas veterinarias de la ciudad de Villavicencio (Meta, Colombia), que cuentan con el permiso de la Secretaría de Salud para la prestación del servicio quirúrgico. Las muestras para análisis microbiológico se tomaron desde tres puntos diferentes en las salas quirúrgicas, los cuales fueron la mesa quirúrgica, el piso y lo emanado directamente desde el sistema de ventilación. Estas muestras fueron seleccionadas dado el grado de exposición que tienen con el paciente y con personal clínico; por otro lado, también permiten evaluar el ambiente del quirófano en tres niveles distintos: alto, medio y bajo (Stevanović et al. 2019, Alsing-Johansson et al. 2024).
Toma y procesamiento de muestras. Para la toma de muestras se realizó la técnica de hisopado usando hisopos estériles Kennedy® (Laboratorios Kennedy S.A.S., Bogotá, Colombia), sumergidos previamente en solución salina estéril 0,9%, se efectuó un barrido sobre la mesa y piso, delimitado por un recuadro de 10 x 10 cm teniendo un área de 100 cm², para posteriormente realizar la siembra (Yimer et al. 2022). Para el muestreo del aire circulante en la sala quirúrgica, emanado directamente desde el sistema de ventilación, se utilizó la técnica de placa expuesta pasiva, siguiendo la metodología de sedimentación propuesta por Alsing-Johansson et al. (2024), donde en cada tiempo establecido, las placas se dejaron en exposición durante 15 minutos.
Todas las muestras fueron inoculadas en medios de cultivo seleccionados que facilitan la identificación presuntiva de géneros microbianos al presentar mayor selectividad: Agar MacConkey (Merck®, Darmstadt, Alemania), Agar sangre (Merck®, Darmstadt, Alemania), Agar EMB (Merck®, Darmstadt, Alemania), Agar B. cereus (yema de huevo-manitol-polimixina, (MYP)) (Merck®, Darmstadt, Alemania), Agar Cetrimida (Merck®, Darmstadt, Alemania), Agar Cromogenico (Merck®, Darmstadt, Alemania) y Agar SS (Merck®, Darmstadt, Alemania).
Las muestras fueron tomadas en tres tiempos diferentes del acto quirúrgico y preparación del quirófano: previo a la intervención quirúrgica (T1), durante la intervención (T2) y después de la aplicación del protocolo de desinfección establecido por el centro clínico posterior al procedimiento (T3). Las muestras de las superficies en los tiempos preoperatorio y postoperatorio fueron recolectadas 10 minutos antes y 10 minutos después del procedimiento quirúrgico, respectivamente, esto en función de la elección de tiempos estandarizados luego de las limpiezas de los quirófanos. En el tiempo intraoperatorio se contabilizaron 5 minutos luego del abordaje quirúrgico. En cada área de muestreo se utilizaron los siete agares previamente mencionados en cada uno de los tiempos establecidos (T1, T2 y T3), lo que correspondió a un total de 21 placas por estrato. Considerando que en cada clínica se evaluaron tres estratos (aire, mesa y piso), se emplearon en total 63 placas de cultivo por establecimiento. Los cultivos fueron embalados y transportados bajo refrigeración a 8ºC, máximo tiempo de procesamiento de 2 horas, según indicaciones del Instituto Nacional de Salud en Colombia (INS 2020).
Se incubaron las muestras manteniendo una temperatura de 37 °C, durante 24 horas, para el adecuado crecimiento de las colonias, transcurrido este periodo, en cada placa se evaluó la presencia o ausencia de crecimiento bacteriano. La concentración microbiana se expresó en unidades formadoras de colonia (UFC) /m³ para muestra del aire y UFC/m² para superficies, según Alsing-Johansson et al. (2024). Para la cuantificación de la carga bacteriana en aire, las colonias obtenidas en las placas expuestas se contaron, después de un período de incubación de 24 horas, manualmente empleando un contador de colonias, y el resultado se expresó utilizando la fórmula descrita por Omeliansky (1940): N = 5a x 104 (bt)-1 Donde N = corresponde al número de UFC/m³, a = es el número total de colonias desarrolladas en la placa, b = es el área de la superficie expuesta de la placa y t = el tiempo de exposición en minutos. El factor 5 × 10⁴ permite estandarizar los valores obtenidos a volumen de aire y tiempo de muestreo (Atalay et al. 2023).
En las placas con crecimiento positivo, se realizó el aislamiento de las colonias formadas para posterior antibiograma.
Caracterización de los agentes. La clasificación morfológica de los agentes bacterianos se realizó mediante el análisis general de colonias a nivel macroscópico evaluando características como la forma, consistencia, aspecto, color según indicaciones de Rattray et al. (2023). También, pruebas complementarias básicas de catalasa y coagulasa siguiendo los procedimientos descritos por MacFaddin (2000). Adicional, se aplicó la técnica de tinción diferencial de Gram (1884), la cual distingue. por microscopia, los microorganismos en Gram Positivos y Gram negativos según la composición y grosor de su pared celular, dependiendo del contenido de peptidoglicano. Esta tinción se realizó aplicando cristal violeta, lugol, alcohol-cetona y safranina, generando una coloración púrpura en bacterias Gram positivas y rosada en Gram negativas. La determinación de los géneros se orientó con base en macroscopía, microscopía y pruebas complementarias de acuerdo con los lineamientos propuestos por Sizar et al. (2023).
Sensibilidad a los antibióticos. Para determinar la presencia de multirresistencia en los microorganismos aislados se realizó la técnica de difusión de disco descrita por Kirby-Bauer (1966). Se utilizaron discos Condalab® (Condalab S.A., Madrid, España) con las siguientes concentraciones estandarizadas: amoxicilina 25 µg, ampicilina 10 µg, ceftriaxona 30 µg, ciprofloxacino 5 µg, doxiciclina 30 µg, enrofloxacina 5 µg, gentamicina 10 µg, norfloxacina 10 µg, oxitetraciclina 30 µg, rifampicina 5 µg y sulfametoxazol/trimetoprim 25 µg.
Esto con el fin de determinar la susceptibilidad a los antimicrobianos mediante la técnica de difusión en agar, se siguieron los lineamientos establecidos por el Clinical and Laboratory Standards Institute (CLSI) (CLSI 2020) y European Committee on Antimicrobial Susceptibility Testing (EUCAST 2025). Para ello, se utilizó agar Mueller-Hinton (Scharlau®, Barcelona, España), donde se sembraron las cepas bacterianas previamente aisladas según las normas internacionales establecidas por el CLSI (2020) mediante el ajuste de escala de McFarlan ajustada a 0,5 (~1x108 UFC ml-1), una vez transcurridos 15 minutos de la inoculación, se colocaron los discos de sensibilidad y se incubaron las placas a 37 °C durante 24 h a 48 h (según crecimiento). La interpretación de los resultados se realizó comparando los diámetros de inhibición con los puntos de corte establecidos por la normativa mencionada, clasificando las cepas como sensibles o resistentes (Weinstein et al. 2020, Menezes et al. 2022).
Análisis estadístico. Se realizó estudio comparativo entre grupos independientes, evaluando el recuento de UFC por las tres clínicas veterinarias, los tres momentos de muestreo (preoperatorio, intraoperatorio y postoperatorio) y los tres estratos de exposición (aire, mesa y piso). Con el fin de identificar diferencias preliminares en los patrones de distribución, se aplicó la prueba no paramétrica de Kruskal-Wallis. Posteriormente, se utilizó un análisis de varianza de una vía (ANOVA) para cada uno de los factores evaluados. Se empleó un nivel de significancia de α = 0,05 para todas las pruebas, considerando diferencias estadísticamente significativas cuando p<0,05. Todos los análisis se realizaron en el software RStudio®, empleando las funciones kruskal.test() y aov().
Aspectos éticos. El estudio se diseñó garantizando la confidencialidad y protección de la información y la identidad de las clínicas veterinarias muestreadas. Todas las clínicas participantes otorgaron autorización institucional previa para la realización de los muestreos en áreas quirúrgicas, cumpliendo con los requisitos administrativos y de bioseguridad exigidos para el ingreso, permanencia y manipulación de superficies en estos entornos. Los nombres y datos identificativos de los establecimientos se mantuvieron en anonimato, empleando códigos alfanuméricos para su registro y análisis. El tratamiento de la información suministrada por los responsables de cada clínica se realizó conforme a la normativa colombiana vigente en protección de datos personales (Ley 1581 de 2012). No se realizaron procedimientos experimentales en animales, ni en seres humanos, dado que las muestras fueron tomadas exclusivamente de superficies y objetos inertes. En cuanto a bioseguridad, todas las actividades de muestreo, manipulación y análisis microbiológico se llevaron a cabo siguiendo los lineamientos del Decreto 2323 de 2006, que regula la Red Nacional de Laboratorios y establece los criterios para el manejo seguro de muestras y residuos biológicos. Asimismo, las pruebas de susceptibilidad antimicrobiana se realizaron en concordancia con las disposiciones aplicables al uso de productos farmacéuticos contempladas en el Decreto 2200 de 2005, dado que se emplearon antibióticos en los procedimientos analíticos.
En esta investigación se analizaron 189 medios de cultivo correspondientes a las muestras recolectadas en las tres clínicas veterinarias. En total se presentó crecimiento bacteriano en 25 de los medios (13,23%). Donde, en la clínica 1 hubo crecimiento en 8 de los medios (32%), en la clínica 2 en 11 medios (44%) y en la clínica 3 en 6 de los medios (24%). Los medios a los que se atribuye este crecimiento son Agar B. cereus MYP y Agar sangre. En los otros cinco medios de cultivo no se determinó crecimiento satisfactorio de colonias bacterianas de interés.
Los conteos de UFC aisladas en Agar B. cereus MYP en cada clínica veterinaria, según la superficie muestreada y el momento del acto quirúrgico se observan en las Tabla 1 y 2.
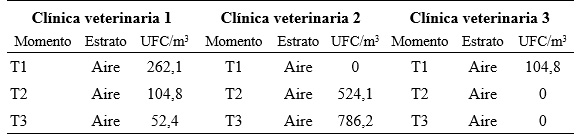
T1: muestra tomada en el momento preoperatorio, T2: muestra tomada en el momento intraoperatorio, T3: muestra tomada en el momento postoperatorio, UFC/m3: unidades formadoras de colonia en metro cúbico.
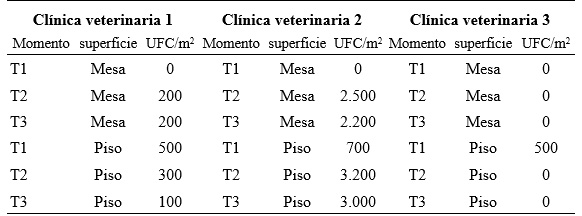
T1: muestra tomada en el momento preoperatorio, T2: muestra tomada en el momento intraperatorio, T3: muestra tomada en el momento posperatorio, UFC/m2: unidades formadoras de colonia en metro cuadrado.
En cuanto al Agar sangre, las UFC aisladas se observaron en el aire, únicamente en T3 de la clínica veterinaria 2 (366,9 UFC/m3), y en mesa y piso, en diferentes tiempos de muestreo de las clínicas veterinarias 2 y 3 (Tabla 3), mientras que la clínica 1 no presentó este tipo de aislamiento.
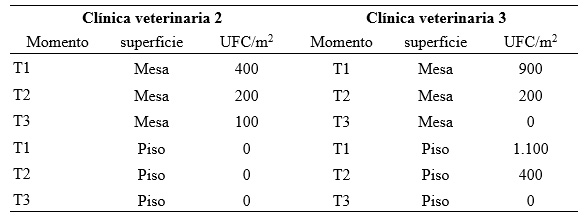
T1: muestra tomada en el momento preoperatorio, T2: muestra tomada en el momento intraperatorio, T3: muestra tomada en el momento posperatorio, UFC/m2: unidades formadoras de colonia en metro cuadrado.
Cuando se reunieron los resultados de las Tablas 1, 2, 3 y lo aislado en Agar sangre del aire de la clínica veterinaria 2, no se encontraron diferencias significativas de UFC entre los tiempos de muestreo (T1, T2, T3) (ANOVA: p = 0,731; Kruskal-Wallis: p = 0,934; p>0,05) o entre superficies (ANOVA: p = 0,374; Kruskal-Wallis: p = 0,581; p > 0.05). Por el contrario, sí hubo diferencias significativas de UFC entre clínicas (ANOVA, p = 0,004, p<0,05).
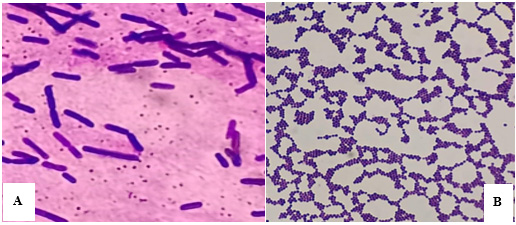
Las colonias que crecieron en el Agar B. cereus MYP presentaron un aspecto seco y rugoso, con coloración rosada y un halo de precipitación sobre fondo igualmente rosado, compatible con cepas productoras de lecitinasa. Estas a la tinción de Gram fueron Gram positivas y según su morfología microscópica bacilos (Figura 1A), determinando así el género Bacillus spp. Por otro lado, las colonias del Agar sangre tuvieron morfología circular de aspecto cremoso y opaco, coloración blanquecina y un halo transparente a su alrededor, que permitía visualizar el fondo del agar sin tonalidad rojiza. Estas a la tinción de Gram fueron Gram positivas y según su morfología microscópica cocos agrupados en racimos (Figura 1B). Las pruebas de catalasa y coagulasa para las colonias obtenidas en Agar sangre fueron positivas, determinando así el género Staphylococcus spp.
Por otro lado, en el antibiograma de los aislamientos compatibles con Bacillus spp. y Staphylococcus spp. se observan en las Tabla 4 y 5, respectivamente.
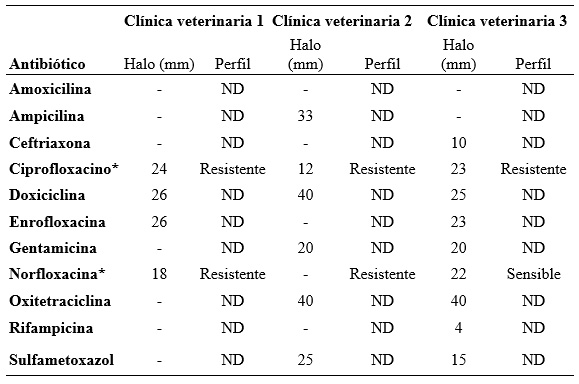
“-”: sin halo. “*”: antibióticos con puntos de corte disponibles según EUCAST (2025). ND: No Determinado (debido a la ausencia de puntos de corte por parte de las guías internacionales estandarizadas como lo son CLSI (2020) y EUCAST (2025)).
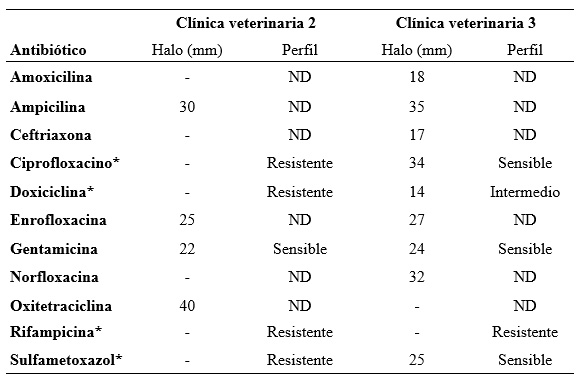
“-”: sin halo. “*”: antibióticos con puntos de corte disponibles según CLSI (2020) para ciprofloxacino, doxiciclina, rifampicina y sulfametoxazol-trimetoprim; y EUCAST (2025) para la gentamicina. ND: no determinado (debido a la ausencia de puntos de corte por parte de las guías internacionales estandarizadas como lo son CLSI (2020) y EUCAST (2025)).
En Colombia se ha documentado la presencia de bacterias con potencial nosocomial en entornos veterinarios, que confirma su circulación en áreas clínicas y quirúrgicas (Sánchez 2015, Arroyave et al. 2019). La presencia de estos agentes representa además un riesgo clínico y zoonótico, donde procedimientos quirúrgicos prolongados y el compromiso inmunológico del paciente favorecen infecciones nosocomiales y la transmisión de patógenos entre animales, personal y el ambiente hospitalario (Bucataru et al. 2024, Rizzo et al. 2025).
La resistencia antimicrobiana incrementa el riesgo clínico al permitir la supervivencia bacteriana y la diseminación de patógenos mediante mecanismos como la inactivación enzimática y la transferencia de genes de resistencia (Prestinaci et al. 2021). La Organización Mundial de la Salud (WHO 2025) advierte que antibióticos de uso común, como las cefalosporinas de tercera generación, fluoroquinolonas, penicilinas, e incluso antibióticos de último recurso están perdiendo efectividad debido al aumento de la resistencia bacteriana, especialmente en Escherichia coli, K. pneumoniae y P. aeruginosa.
Los resultados obtenidos en las tres clínicas veterinarias, donde el crecimiento bacteriano se evidenció únicamente en Agar B. cereus MYP y Agar sangre, son concordantes con reportes de contaminación ambiental en entornos clínicos, en los que la presión de limpieza y una baja carga bacteriana favorecen la recuperación de microorganismos oportunistas (Spratt et al. 2024, Farina et al. 2024). Esta persistencia se explica por la capacidad de Bacillus spp. para formar esporas y resistir condiciones adversas (Ramlucken et al. 2021). Por su parte, el crecimiento en Agar sangre puede atribuirse a su carácter enriquecido y no selectivo, que favorece la recuperación de bacterias con capacidad hemolítica presentes en ambientes clínicos. Asimismo, los procesos de desinfección limitan el crecimiento de bacterias más exigentes, mientras que microorganismos esporulados o tolerantes a estos procedimientos presentan mayor capacidad de recuperación (Bintsis 2017).
Actualmente desde el conocimiento de los autores no existen estudios publicados que reporten recuentos cuantitativos de UFC en aire o superficies de quirófanos utilizando Agar Bacillus cereus MYD. En este estudio, los recuentos obtenidos mediante este Agar alcanzaron hasta 786 UFC/m³ en aire y 3.200 UFC/m² en superficies de piso, con detección intermitente y momentos del acto quirúrgico con valores nulos (Tablas 1 y 2). Este comportamiento puede explicarse por las limitaciones técnicas del muestreo utilizado en este estudio, el cual fue placa de sedimentación, un método pasivo dependiente de la gravedad y del tiempo de exposición, asociado a menor sensibilidad y a la ocurrencia de falsos negativos en concentraciones bajas o variables de bioaerosoles (Napoli 2020). No obstante, la mayor recuperación en aire durante los momentos T1 y T3, junto con su detección en el piso, en este estudio, sugiere deposición aérea de esporas, coherente con la capacidad de Bacillus spp. de formar endosporas resistentes a la desecación y a los desinfectantes ambientales (Ramlucken et al. 2021).
El Agar sangre ha sido utilizado en estudios de microbiología ambiental hospitalaria como medio no selectivo y enriquecido para la evaluación de la carga bacteriana total en aire y superficies de áreas quirúrgicas (Chawla et al. 2021). En este estudio el recuento promedio en aire (366,9 UFC/m³) supera los rangos de referencia propuestos para quirófanos en actividad (<180 UFC/m³), establecidos por Pasquarella et al. (2020). En superficies, los recuentos entre 400 y 900 UFC/m² exceden los valores orientativos sugeridos tras la desinfección (<5-10 UFC/cm²), de acuerdo con Rutala y Weber (2020).
La actividad humana en el quirófano, incluyendo el tránsito de personal y el contacto frecuente con superficies, contribuye a la dispersión y redistribución de microorganismos; aunque los procesos de limpieza y desinfección aplicados antes y durante el intraoperatorio reducen la carga bacteriana superficial, su efecto puede verse limitado por la recontaminación posterior (Byers 2020).
La literatura muestra resultados heterogéneos respecto a la variación de la contaminación microbiológica en ambientes quirúrgicos. En relación con el momento de muestreo, estudios en quirófanos de humanos reportan diferencias significativas en la carga bacteriana del aire entre fases quirúrgicas (p<0,001) (Fu et al. 2025) o entre distintos momentos (p = 0,00) (Yimer et al. 2022). Hallazgos similares en veterinaria documentan una interacción significativa entre el tiempo y el hospital, vinculada a la limpieza y el uso del quirófano (p = 0,0028) (Harper et al. 2013). Respecto al tipo de superficie, la evidencia es contradictoria, mientras algunos estudios no encuentran diferencias significativas (p>0,05) (Bartoli et al. 2025), otros sí las reportan (p = 0,003) (Prasek et al. 2025).
Al respecto, los resultados del presente estudio no evidenciaron diferencias significativas entre tiempos de muestreo o superficies (p>0,05). Esta falta de significancia podría atribuirse a la elevada variabilidad inherente a los recuentos microbianos, la distribución heterogénea de los microorganismos y el número limitado de réplicas, factores descritos como limitantes metodológicas que pueden reducir el poder estadístico (Pasquarella et al. 2012, Serdar et al. 2020).
Sin embargo, en este estudio sí se encontró diferencia significativa en los recuentos de UFC entre las clínicas veterinarias evaluadas (p<0,05). Este hallazgo concuerda con la literatura, que identifica a la institución o ubicación específica como un factor crítico. Harper et al. (2013) reportaron diferencias significativas entre hospitales y salas en veterinaria, asociadas a rutinas de limpieza y actividad. Yimer et al. (2022) observaron diferencias entre instituciones hospitalarias humanas, vinculadas al flujo de personal, la ocupación y la ventilación.
Por otro lado, en este estudio se identificó el género Bacillus spp. en quirófanos veterinarios (Figura 1A). Al respecto, la Administración de Alimentos y Medicamentos de los Estados Unidos (FDA 2024), recomienda en su Manual Analítico Bacteriológico, el uso de placas de Agar Bacillus cereus MYP para confirmación de Bacillus spp. y especies relacionadas aisladas con el grupo de B. cereus sensu latu para casos esporádicos, brotes y muestras de vigilancia ambiental de rutina. En este estudio, las colonias del Agar B. cereus MYP presentaron una morfología característica con zona de precipitación alrededor del crecimiento, atribuida a la hidrólisis de la lecitina presente en la yema de huevo, junto con la ausencia de fermentación del manitol y la acción selectiva de la polimixina, rasgos fenotípicos propios del género Bacillus spp. (Gdoura-Ben et al. 2018, Biolife Italiana 2020, Kubota et al. 2022). Adicionalmente, la tinción de Gram y morfología microscópica permitió observar bacilos Gram positivos, dispuestos de forma aislada o en cadenas cortas (Figura 1A), lo que reforzó la clasificación de dichas colonias dentro del género Bacillus spp. (Tallent et al. 2021).
La presencia de Bacillus spp. como microorganismo dominante en los quirófanos veterinarios de Villavicencio, coincide con lo reportado por Farina et al. (2024), quienes destacan la capacidad de sus esporas para persistir en superficies, aire y material particulado ambiental; incluso después de la limpieza, dada su resistencia estructural (Harper et al. 2013, Sfaciotte et al. 2021). Hallazgos similares a este estudio, se han descrito en hospitales y clínicas veterinarias, donde Bacillus spp. ha sido aislado de mesas, pisos y equipos, tanto en áreas quirúrgicas como no quirúrgicas (Sfaciotte et al. 2021, Spratt et al. 2024). Otros estudios han documentado que, junto a Bacillus spp., las superficies de contacto pueden albergar diversos patógenos de relevancia clínica como S. aureus, E. coli, Pseudomonas spp. y Clostridium difficile (van der Merwe y Naidoo 2023, Spratt et al. 2024), lo que refuerza la importancia de estas áreas como reservorios y fuentes de contaminación en entornos veterinarios.
Por otro lado, la identificación de los aislamientos asociados al crecimiento en Agar sangre presentaron morfología compatible con una zona clara de hemólisis completa (β), resultado de la lisis total de los eritrocitos en el medio, un patrón típico de estafilococos β-hemolíticos en Agar sangre (Comenius University 2018, Murray et al. 2020). La morfología microscópica y tinción de Gram de los aislamientos en el Agar sangre para este estudio, corresponden, según pautas de Barbuti et al. (2023), a cocos Gram positivos agrupados en racimos, una disposición microscópica característica de Staphylococcus spp. (Figura 1B). La prueba de catalasa positiva permitió diferenciar estos cocos Gram positivos de otros géneros como Streptococcus spp., y la prueba de coagulasa positiva respaldó su clasificación dentro de Staphylococcus spp., ya que muchos estafilococos clínicamente relevantes, incluyendo S. aureus, producen coagulasa (Mahon et al. 2007).
La detección de Staphylococcus spp. en superficies quirúrgicas (ej., mesa quirúrgica) en este estudio, concuerda con lo descrito en estudios previos que señalan a este género como un contaminante frecuente del ambiente hospitalario veterinario, asociado a la descamación epitelial, la manipulación del paciente y el contacto indirecto del personal con superficies críticas (Guo et al. 2020, Hunter et al. 2021). Diversas investigaciones han indicado que su presencia en el ambiente no siempre refleja una contaminación persistente, sino fluctuaciones relacionadas con las prácticas de limpieza, el manejo del paciente, la ventilación y las características propias de cada establecimiento (Akwuobu et al. 2021). En este contexto, el aislamiento de Staphylococcus spp. adquiere relevancia clínica, dado que especies coagulasa-positivas han sido reportadas como contaminantes frecuentes de superficies ambientales en hospitales veterinarios y como agentes implicados en infecciones del sitio quirúrgico en medicina humana y veterinaria (Velázquez-Guadarrama et al. 2017, Hunter et al. 2021).
La interpretación de los resultados del presente estudio, respecto a la confirmación del género de las bacterias aisladas, presenta limitaciones metodológicas, dado que no se aplicaron pruebas bioquímicas específicas, ni técnicas moleculares para la identificación bacteriana. En consecuencia, no fue posible realizar una determinación taxonómica precisa a nivel de especie, especialmente en grupos bacterianos con alta similitud fenotípica como Bacillus cereus sensu lato y Staphylococcus spp. (Kabir et al. 2017, Velázquez-Guadarrama et al. 2017).
En cuanto a la resistencia antimicrobiana, se evidenció que, debido a la ausencia de puntos de corte establecidos por las guías CLSI (2020) y EUCAST (2025) para la mayoría de los antimicrobianos evaluados, únicamente fue posible interpretar el perfil de susceptibilidad de los aislamientos frente a ciprofloxacina y norfloxacina. Para el resto de los antibióticos, los diámetros de los halos de inhibición se reportaron exclusivamente como datos descriptivos, sin categorización clínica (EUCAST 2024).
Bajo este enfoque, Bacillus spp. mostró resistencia a ciprofloxacina y norfloxacina (Tabla 4), un hallazgo que, aunque no es predominante en la literatura, ha sido documentado en ambientes hospitalarios. Haque et al. (2024) reportaron que el 37,7% de los aislamientos de Bacillus spp. fueron resistentes a ciprofloxacina, asociando este fenómeno a mutaciones en los genes gyrA y parC, así como a la activación de bombas de eflujo. Atalay et al. (2023) identificaron la presencia de Bacillus spp. resistentes a fluoroquinolonas en aire y superficies de un hospital humano, atribuyendo esta resistencia a la exposición continua a desinfectantes y antibióticos en el entorno clínico. Asimismo, la resistencia a norfloxacina ha sido observada en diferentes especies del género Bacillus spp., con un 65,7% de los aislamientos resistentes según Adamski et al. (2023).
Por su parte, para Staphylococcus spp. se utilizaron los puntos de corte establecidos por CLSI (2020), para ciprofloxacino, doxiciclina, rifampicina y sulfametoxazol-trimetoprim. Además, de los criterios de EUCAST (2025), para la gentamicina. Los antibióticos que no pudieron ser interpretados se reportaron únicamente de forma descriptiva, como indica EUCAST (2024).
Por consiguiente, Staphylococcus spp. presentó un perfil de resistencia a rifampicina y variabilidad a ciprofloxacina y trimetoprim sulfametoxazol (Tabla 5). Este comportamiento coincide con Hunter et al. (2021), donde se ha documentado la presencia de estafilococos ambientales multirresistentes, reportando la persistencia de Staphylococcus spp. resistentes a rifampicina, fluoroquinolonas y otros antimicrobianos, incluso después de los procesos de limpieza rutinarios. De manera similar, Leite et al. (2023) evidenciaron una alta frecuencia de resistencia a fluoroquinolonas, rifampicina y sulfonamidas. Asimismo, según Sebola et al. (2023) estos aislados de Staphylococcus spp. muestran patrones comparables a los observados en hospitales humanos, destacando la importancia del enfoque Una Salud en el control y monitoreo de la resistencia antimicrobiana en instalaciones quirúrgicas veterinarias.
Este estudio presenta una limitación metodológica en la evaluación de la susceptibilidad antimicrobiana, derivada de la falta de puntos de corte interpretativos para difusión en disco de varios antimicrobianos evaluados. Dado que tanto el CLSI (2020), como el EUCAST (2025) han restringido progresivamente los criterios para este método, favoreciendo las técnicas cuantitativas como la microdilución para obtener una concentración mínima inhibitoria (CMI), cuando los puntos de corte para disco no están disponibles. Los resultados correspondientes a estos antimicrobianos, en este estudio, únicamente pudieron presentarse de manera descriptiva según EUCAST (2024), lo que limita su interpretación clínica.
En conclusión, se aislaron e identificaron los géneros Bacillus spp. y Sthapylococcus spp., en quirófanos veterinarios, Aunque no hubo diferencias significativas entre superficies ni momentos del acto quirúrgico, si las hubo en la carga microbiana entre las diferentes clínicas. Respecto al perfil de susceptibilidad antibiótica, Bacillus spp. presentó resistencia a ciprofloxacina y norfloxacina, mientras que, Staphylococcus spp. mostró resistencia a rifampicina y un comportamiento variable frente a ciprofloxacina y trimetoprim sulfametoxazol. Estos hallazgos evidencian la necesidad urgente de reforzar y estandarizar los protocolos de limpieza, antisepsia y desinfección para mitigar la diseminación de bacterias multirresistentes y reducir el riesgo de infecciones del sitio quirúrgico en las clínicas veterinarias.
Contribución de los autores. GPMC: realizó los experimentos, procesó los datos experimentales y redactó el artículo con la colaboración de todos los autores. GTIN: contribuyó al muestreo y colaboró en la ejecución de los experimentos. G.C: preparó las muestras. VTA: apoyó con recursos y análisis formal de los datos. JHDA: aportó con revisión, edición y supervisión.
Declaración de conflictos de intereses. Los autores declaran no tener conflictos de intereses financieros ni relaciones personales conocidas que pudieran haber influido en el trabajo presentado en este artículo.
Disponibilidad de datos. Los datos estarán disponibles previa solicitud.