Revista Veterinaria. 2026; 37(1)
https://doi.org/10.30972/vet.3719154
Artículo Original




1 Universidad politécnica estatal del Carchi- Medicina veterinaria, Tulcán, Ecuador.
2 Universidad Politécnica Nacional, Ecuador.
3 Universidad Nacional de Loja, Loja, Ecuador.
 pamilaro20@gmail.com
pamilaro20@gmail.com
Resumen
El virus de la fiebre aftosa (FMDV, por sus siglas en inglés) es un patógeno extremadamente contagioso que afecta a los animales de pezuña hendida y representa una amenaza considerable tanto para la salud animal como para la economía ganadera a nivel global. Este artículo de revisión se centra en la caracterización molecular del FMDV, poniendo especial atención en la estructura del virión, modo de transmisión, el genoma viral y la variabilidad genética, vacunas y distribución del virus en Ecuador. La variabilidad genética otorgada por la proteína viral VP1, y a la falta de mecanismos de corrección de la polimerasa durante la replicación del ARN viral facilita la aparición de cuasi-especies lo cual complica los esfuerzos de control a través de vacunas para la erradicación del virus. También se examinan los principales métodos moleculares utilizados para el diagnóstico y la vigilancia epidemiológica, como la RT-PCR, RT-qPCR y la secuenciación de nueva generación (NGS), que permiten identificar serotipos, linajes y patrones de dispersión geográfica. Por último, es de gran importancia actualizar las estrategias de vacunación y fortalecer los sistemas de monitoreo genético para contener de manera efectiva los brotes y mejorar la inmunogenicidad de las vacunas actuales.
Palabras clave: Patógeno, MDV, variabilidad genética, VP1, salud animal, vacunas.
Abstract. Foot-and-mouth disease virus (FMDV) is a highly contagious pathogen that affects cloven-hoofed animals and represents a major threat to both animal health and the global livestock economy. This review focuses on the molecular characterization of FMDV, with particular emphasis on virion structure, transmission routes, viral genome organization, genetic variability, vaccination strategies, and virus distribution in Ecuador. The high genetic variability of FMVD- mainly associated with the VP1 capsid protein and the lack of proofreading activity of the viral RNA polymerase during replication- favors the emergence of quasispecies, complicating vaccine-based control and hindering virus eradication efforts. Additionally, this review discusses the main molecular tools used for diagnosis and epidemiological surveillance, including RT-PCR, RT-qPCR, and next-generation sequencing (NGS), which enable the identification of serotypes, lineages, and geographic distribution patterns. Finally, the importance of updating vaccination strategies and strengthening genetic surveillance systems is highlighted to improve outbreak containment and enhance the immunogenicity of current vaccines.
Key words: Pathogen, FMDV, genetic variability, VP1, animal health, vaccines.
La fiebre aftosa causada por un virus es muy contagiosa, afecta a animales de pezuña hendida, como los bovinos, porcinos, ovinos y caprinos. Esta enfermedad viral tiene un impacto significativo en la salud pública, animal y también en el desarrollo económico a nivel mundial causando pérdidas considerables en la producción ganadera, ya que reduce la cantidad de carne y leche, genera restricciones comerciales lo cual directamente afecta la económica del país (Sangucho et al. 2024). Además, en zonas ganaderas esto vendría a ser un problema debido a los costos relacionados con la prevención, control y erradicación de la fiebre aftosa.
El virus de la fiebre aftosa (FMDV, por sus siglas en inglés) perteneciente al género Aphthovirus de la familia Picornaviridae, tiene siete serotipos los cuales se encuentran principalmente en regiones endémicas de Asia, África y América del Sur. Este virus puede afectar a una amplia gama de especies susceptibles como bovinos y porcinos, lo que complica su control y vigilancia epidemiológica (Elrashedy et al. 2025a). La capacidad del virus para infectar a múltiples huéspedes y su rápida propagación aumentan el riesgo de brotes que pueden desencadenar crisis sanitarias y económicas tanto a nivel regional como global.
A nivel molecular este virus tiene genoma es de ARN y tiene una alta tasa de mutación por no tener una polimerasa corregidora de errores, el FMDV presenta una notable variabilidad genética (Mohamadin et al. 2025), esto le confiere la capacidad de generar botes e infectar varias especies. La caracterización molecular y el análisis de esta variabilidad son esenciales para comprender la evolución del virus, mejorar la vigilancia epidemiológica y crear medidas de prevención adaptadas a los serotipos y linajes que están circulando (Gubbins et al. 2022).
En consecuencia, si bien el desarrollo de vacunas contra la fiebre aftosa ha representado históricamente un reto debido a la diversidad de serotipos virales y la limitada inmunidad cruzada entre ellos (Lu et al. 2022), las vacunas inactivadas formuladas con adyuvantes acuosos u oleosos se han consolidado como un biológico altamente estable, capaz de inducir una respuesta inmune protectora (Jiao y Wu 2024) y de mayor duración cuando se aplica conforme a los esquemas de vacunación recomendados (Miraglia et al. 2024). No obstante, el desarrollo de nuevas vacunas basadas en tecnologías innovadoras como las vacunas recombinantes continúa siendo un desafío, ya que su eficacia depende de la capacidad de generar protección específica frente a los serotipos circulantes o, idealmente, de inducir inmunidad cruzada frente a múltiples serotipos del virus.
Esta revisión tuvo como objetivo examinar las principales características biológicas y moleculares del virus de la fiebre aftosa, analizar los mecanismos que generan su variabilidad genética y discutir las implicaciones de este virus para el diagnóstico, la vacunación y el control sanitario.
Diseño del estudio. Se realizó una revisión sistemática de la literatura con el objetivo de evaluar la estructura del virus, síntomas, transmisibilidad variabilidad, efectividad de las vacunas, los mecanismos inmunológicos, las plataformas tecnológicas y las implicaciones económicas de las vacunas contra la fiebre aftosa, así como su relevancia en los programas de control y erradicación de la enfermedad.
Fuentes de información y estrategia de búsqueda. La búsqueda bibliográfica se efectuó en las bases de datos PubMed/MEDLINE, Scopus, Web of Science y ScienceDirect, Google scholar, complementada con literatura gris proveniente de organismos internacionales como la Organización Mundial de Sanidad Animal (WOAH 2023) y la Organización Panamericana de la Salud (OPS/PANAFTOSA 2022).
Se utilizaron combinaciones de términos MeSH y palabras clave libres, incluyendo: “foot-and-mouth disease”, “Variability”, “virion struture” “FMD vaccine”, “vaccine efficacy”, “immunological response”, “vaccination programs”, “eradication” y “economic impact”, unidos mediante los operadores booleanos AND y OR. El periodo de búsqueda comprendió desde el año 2020 hasta 2025, sin restricciones geográficas.
Criterios de elegibilidad. Se incluyeron estudios que cumplieran con los siguientes criterios:
Artículos originales, revisiones sistemáticas y metaanálisis revisados por pares.
Artículos sobre la estructura viral de Fiebre aftosa, serotipos prevalentes, variabilidad del virus, y métodos de detección viral.
Estudios que evaluaron vacunas contra la fiebre aftosa en especies susceptibles.
Publicaciones que analizaron aspectos de eficacia vacunal, respuesta inmunológica, tecnologías emergentes y/o impacto económico.
Artículos publicados en inglés o español.
Tesis de un autor ecuatoriano debido a la relevancia con respecto al serotipo que circula en dicho país.
Se excluyeron:
Estudios duplicados.
Reportes de casos, cartas al editor y resúmenes de congresos.
Publicaciones sin acceso al texto completo.
Estudios que no abordan directamente los objetivos de la revisión.
Proceso de selección de estudios. La selección de los estudios se realizó en cuatro fases: identificación, cribado, elegibilidad e inclusión. Inicialmente, se evaluaron de manera independiente los títulos y resúmenes. Posteriormente, los artículos potencialmente elegibles fueron analizados a texto completo. Las discrepancias se resolvieron por consenso.
Extracción y análisis de los datos. De cada estudio incluido se extrajeron datos relacionados con estructura viral, mecanismos de variabilidad genética, tipos de vacuna, plataforma tecnológica, serotipos incluidos, esquemas de vacunación, indicadores de respuesta inmunológica, eficacia protectora, impacto económico y aplicación en programas de erradicación. La síntesis de los resultados se realizó de forma cualitativa y comparativa, destacando similitudes y diferencias entre plataformas vacunales y regiones geográficas.
Evaluación del riesgo de sesgo. La calidad metodológica de los estudios incluidos se evaluó mediante herramientas validadas según el diseño del estudio, considerando aspectos como la claridad de los objetivos, la metodología empleada y la consistencia de los resultados reportados.
El agente etiológico de esta enfermedad es el virus de la fiebre aftosa, perteneciente al género Aphthovirus de la familia Picornaviridae. Es un virus no envuelto con una cápside icosaédrica de aproximadamente 25 a 30 nanómetros de diámetro (Elrashedy et al. 2025b). Esta cápside está compuesta por 60 copias de cada una de las cuatro proteínas estructurales: VP1, VP2, VP3 (expuestas en la superficie) y VP4 (interna), las cuales forman la envoltura proteica que protege el genoma viral (Kabir et al. 2024). El genoma del FMDV es un ARN monocatenario de sentido positivo no segmentado y no envuelto, tiene 8.500 nucleótidos, contiene un solo marco de lectura abierto (ORF) que codifica una poliproteína de 7.000 nucleótidos (Elrashedy et al. 2025a). El ORF está flanqueado por una región no traducida (UTR) 5′ de aproximadamente 1.300 nucleótidos y una UTR 3′ más corta de unos 90 nucleótidos, seguida de una cola de poli(A) (Gizaw et al. 2020, Medina et al. 2020). La poliproteína es escindida por las proteasas codificadas por el virus (L y 3C), lo que resulta en su separación en tres segmentos: P1, P2 y P3. Este proceso produce un total de 15 proteínas virales maduras, entre ellas las estructurales y las no estructurales que median la replicación, ensamblaje y evasión inmune del virus (Raoof 2024).
El segmento P1 codifica la proteasa líder (Lpro) y las proteínas estructurales VP1 (1D), VP2 (1B), VP3 (1C) y VP4 (1A) (Zhu et al. 2023). El segmento P2 codifica las proteínas no estructurales 2A, 2B y 2C, mientras que el segmento P3 codifica 3A, 3B, la proteína viral del genoma (VPg) (1B, 2B y 3B), la proteasa 3C y la polimerasa 3D (Wubshet et al. 2024). Las proteínas no estructurales (NSPs) desempeñan principalmente funciones en la síntesis de proteínas, la replicación del ARN y la evasión del sistema inmunológico (Jumaa et al. 2021, Dong et al. 2022).
Una característica molecular importante del FMDV es la presencia del péptido 2A, que facilita la “auto escisión” de la poliproteína durante la traducción, mecanismo crucial para la producción de proteínas funcionales (Li et al. 2023). La cápside viral es altamente sensible a condiciones de pH ácido, lo que desencadena su desensamblaje y la liberación del genoma en la célula huésped, aspecto clave en el ciclo infeccioso del virus. Debido a que es un virus ARN, no tiene un sistema de corrección de errores durante la replicación, es decir ADN polimerasa (Wubshet et al. 2024), los Picornavirus generan una población viral heterogénea conocida como cuasiespecies (Jumaa et al. 2021). Esta diversidad genética constante permite que el virus experimente mutaciones continuas, lo que favorece su evolución y adaptación al medio, haciéndolo más resistente tanto a la respuesta inmunitaria del hospedero como a las terapias antivirales disponibles (Elrashedy et al. 2025a). En el caso del FMDV, las modificaciones en la secuencia consenso del genoma se producen de forma progresiva, con una tasa estimada de cambio de entre 0,5 y 1% anual, lo que equivale a uno o dos nucleótidos por semana. Esta variabilidad genética y estructura viral altamente organizada explica la gran capacidad del virus para adaptarse, replicarse rápidamente y evadir respuestas inmunitarias, lo que representa un desafío para el desarrollo de vacunas estables y eficaces.
El virus de la FMDV se transmite por contacto directo con animales infectados o por contacto indirecto con secreciones o excreciones (incluido el semen y la leche) de animales infectados o por vectores mecánicos (Homo sapiens, Equus ferus caballus, Canis lupus familiaris, Felis catus, Classis Aves, vehículos y materiales contaminados); diseminación del virus por aerosol, las partículas en suspensión son transportadas desde un sitio infectado por las corrientes de aire; liberación accidental del virus de un laboratorio; y en algunos caso muy extremos el uso de vacunas que contienen el virus activo debido a errores de producción o almacenamiento de la misma vacuna (Lu et al. 2022).
En los bovinos, los signos más comunes incluyen fiebre elevada (hasta 40 °C), salivación excesiva, anorexia, depresión y la aparición de vesículas dolorosas en la lengua, encías, labios, paladar, banda coronaria, espacio interdigital y pezones; además, las vacas pueden presentar una marcada disminución en la producción láctea y abortos en casos graves (Belsham 2021). Los porcinos, por su parte, desarrollan lesiones vesiculares en el hocico, lengua y especialmente en las patas, lo que provoca cojeras severas y postración, junto con pérdida de apetito y fiebre. En ovinos y caprinos, los signos pueden ser más sutiles o incluso subclínicos, aunque también pueden presentar fiebre, vesículas orales e interdigitales y cojeras. En corderos, es común la muerte súbita por miocarditis viral (Wang et al. 2022). La enfermedad tiene un periodo de incubación de 2 a 14 días y, aunque las lesiones suelen sanar en una semana, pueden complicarse con infecciones secundarias (Le et al. 2024). Debido a la presencia del virus en todas las secreciones y excreciones de los animales infectados, su transmisión es sumamente rápida, lo que convierte a la fiebre aftosa en una amenaza constante para la sanidad animal a nivel mundial (WOAH 2021).
El FMDV es un virus de ARN monocatenario de sentido positivo que pertenece al género Aphthovirus de la familia Picornaviridae. Al ser un virus con genoma ARN, se replica exclusivamente en el citoplasma de las células infectadas. El ciclo de replicación comienza cuando el virus se adhiere a receptores específicos en la superficie celular, principalmente integrinas, lo que facilita su entrada a través de un proceso llamado endocitosis mediada por receptor (Yang et al. 2022). Una vez dentro del endosoma, un cambio en el pH provoca la liberación del genoma viral al citoplasma, donde actúa como ARN mensajero para la producción de una poliproteína viral (ScienceDirect 2024). Esta poliproteína se corta luego por proteasas virales, especialmente la 3C proteasa, para dar como resultado proteínas estructurales que formarán parte de la cápside y no estructurales las cuales son esenciales para la replicación (Gong et al. 2024). La replicación del genoma se lleva a cabo a través de un intermediario de ARN de cadena negativa, que sirve como plantilla para crear nuevas copias de ARN positivo (Sarry et al. 2022). Las cadenas positivas de ARN actúan como ARNm adicionales para la síntesis de la proteína viral o se integran a los viriones de la progenie. Finalmente, las nuevas partículas virales se ensamblan en el citoplasma con la ayuda de algunos organelos de la célula infectada, luego se liberan mediante lisis celular, lo que causa el daño tisular característico de la enfermedad (Li et al. 2024).
Los Picornavirus son únicos entre los virus ARN en el sentido de que cuando una célula se infecta doblemente con dos cepas indistinguibles de la misma especie de virus, los genomas de los virus pueden experimentar una recombinación intermolecular, una característica demostrada tanto con el virus de la fiebre aftosa como con el Poliovirus (Li et al. 2021). Esta recombinación genética genera varias variantes que pueden evadir el reconocimiento por parte del sistema inmune, aumentando su virulencia y patogenicidad.
Serotipos del virus. Con respecto a los distintos serotipos del virus de la fiebre aftosa, existen siete serotipos inmunológicamente distintos: O, A, C, Asia 1, SAT 1, SAT 2 y SAT 3, cada uno con múltiples subtipos y linajes genéticos (Hassanein et al. 2024). Particularmente el serotipo O se destaca por su amplia distribución a nivel mundial, aunque no es el más diverso desde el punto de vista antigénico. El serotipo más antigénico es el tipo A, el cual presenta una mayor variabilidad. Además, según un estudio realizado en Egipto el serotipo más prevalente es el A, con un 67% y se asoció a la región africana y se vinculó a regiones como Etiopía, Kenia y Sudán (El-Ansary et al. 2023, Hassanein et al. 2024). La similitud en la secuencia de aminoácidos entre ambos serotipos es de aproximadamente un 86%. En cuanto a su estructura, las proteínas VP1, VP2 y VP3 se encuentran en la superficie del virus, donde conforman una estructura conocida como barril β de ocho hebras, mientras que la proteína VP4 se sitúa internamente, con una estructura secundaria poco definida (Yang et al. 2020). El serotipo A y C son prevalentes en África, Asia, Europa, y Sudamérica. El serotipo SAT-1 se encuentra en África y Asia. El serotipo SAT-2 y SAT-3 son limitados en África y Asia (Yang et al. 2020, Ismael et al. 2021).
Mecanismos de variabilidad. La región genética correspondiente a VP1 es la que exhibe mayor variabilidad, con diferencias del 30% al 50% entre serotipos, lo que la convierte en un marcador clave para su diferenciación, esto tendría gran relevancia a la hora de hacer una vacuna (Yang et al. 2022). Los epítopos antigénicos más relevantes están localizados en diversas asas estructurales de las proteínas virales, entre ellas la N-terminal, y las asas B-C, E-F, F-G, G-H, así como el extremo C-terminal (Chen et al. 2025). Un aspecto importante es que la proteína VP1 contiene motivos RGD (arginina-glicina-ácido aspártico) altamente conservados (Belsham et al. 2020) y regiones hipervariables dentro del asa G-H, fundamentales para que el virus pueda unirse a las integrinas del hospedador y así ingresar a las células, induciendo una fuerte respuesta inmune (Ekanayaka et al. 2020, Raoof 2021). Esta exposición a la respuesta inmune genera una fuerte presión selectiva, favoreciendo mutaciones que permiten al virus evadir los anticuerpos y adaptarse a diferentes hospedadores (Li et al. 2023, Elrashedy et al. 2025b). Además, como FMDV es un virus de ARN cuya polimerasa carece de actividad correctora, presenta una alta tasa de mutación, lo que facilita la rápida aparición de variantes y linajes distintos dentro de un mismo serotipo (Li et al. 2023, Dinana et al. 2024). La hipervariabilidad de VP1 tiene implicaciones importantes para el control de la enfermedad, ya que puede disminuir la eficacia de las vacunas y exige una vigilancia molecular constante para actualizar estrategias de prevención y control (Hassan et al. 2021, Elrashedy et al. 2025b). Sin embargo, las vacunas inactivadas con adyuvantes oleosos continúan siendo la herramienta más eficaz para los programas de control y erradicación de la fiebre aftosa.
Se identificó una mutación en la posición 83 de la proteína VP1, donde el ácido glutámico (E) se reemplaza por lisina (K) en el virus adaptado a cultivo celular (Belsham et al. 2020). Esta mutación (VP1 E83K) reduce la capacidad del virus para suprimir la señalización de IFN-β, lo que resulta en una atenuación del virus (Tesfaye et al. 2020, Keck et al. 2022). Por otro lado, la forma salvaje de VP1 (E83) interactúa específicamente con el sitio de unión de TRAF3 en la proteína MAVS, inhibiendo la unión de TRAF3 a MAVS e inhibiendo así la respuesta inmune mediada por IFN-β (Ekanayaka et al. 2020, Murienthaisong et al. 2021).
Estos hallazgos sugieren que la mutación E83K en VP1 compromete la capacidad del virus para bloquear la señalización de IFN-β, lo que podría tener implicaciones en la virulencia y la propagación del FMDV (Muenthaisong et al. 2021).
Finalmente, en consecuencia, el estudio detallado de la estructura molecular del FMDV ha sido esencial para comprender su patogénesis y orientar estrategias de prevención y control de brotes a nivel global (Belsham 2021). Esta estructura genética y proteica confiere al FMDV una notable capacidad de mutación y adaptación, lo que complica su control y erradicación (Kim et al. 2024). Por lo tanto, la comprensión de la variabilidad genética del FMDV es esencial para el desarrollo de estrategias de control más efectivas, incluyendo el diseño de vacunas que puedan ofrecer una protección más amplia y duradera contra las diversas cepas del virus.
Vacunas de la fiebre aftosa. Las vacunas contra la fiebre aftosa se basan principalmente en formulaciones de virus completo inactivado, generalmente con adyuvantes para favorecer la respuesta inmune como emulsiones oleosas. Estas alternativas vacunales constituyen el pilar de los programas de control y erradicación de la enfermedad a nivel mundial debido a su elevada eficacia, estabilidad y capacidad para inducir una respuesta inmune protectora sostenida en las especies susceptibles (WOAH 2023). Si bien las vacunas inactivadas oleosas, inducen una robusta respuesta inmune la capacidad de neutralización cruzada depende significativamente del esquema de vacunación aplicado y del grado de similitud antigénica entre la cepa vacunal y el virus circulante. Diversos estudios experimentales, revisiones sistemáticas y metaanálisis han demostrado que estas vacunas inducen altos títulos de anticuerpos neutralizantes y reducen significativamente la severidad clínica y la excreción viral, superando en eficacia a otras plataformas vacunales actualmente en desarrollo (Jiao y Wu 2024, Miraglia et al. 2024). No obstante, la protección conferida es serotipo-específica y depende del grado de concordancia antigénica entre las cepas vacunales y los virus circulantes, lo que obliga a una actualización periódica de las formulaciones y a la aplicación de esquemas de revacunación. Estos esquemas de vacunación de refuerzos y combinaciones antigénicas apropiadas mejoran la amplitud de la respuesta inmune neutralizante frente a cepas heterólogas del mismo serotipo (Miraglia et al. 2024). En paralelo, se han desarrollado nuevas tecnologías, vacunas basadas en mRNA, proteínas recombinantes, sistemas de expresión en plantas, vectores virales, vacunas sintéticas y de ADN (Jiao y Wu 2024), las cuales muestran potencial para mejorar aspectos como la inmunidad cruzada, la seguridad biológica; sin embargo, su aplicación a gran escala aún enfrenta limitaciones inmunológicas, productivas y económicas, por lo que actualmente complementan, pero no sustituyen, a las vacunas inactivadas en los programas oficiales de control de la fiebre aftosa. No obstante, el análisis reconoce que estas tecnologías emergentes presentan ventajas potenciales en términos de innovación, bioseguridad y flexibilidad de diseño, por lo que su desarrollo podría complementar las estrategias vacunales tradicionales en el futuro (Rodríguez et al. 2024). Finalmente, desde una perspectiva inmunológica y de eficacia global, las vacunas inactivadas siguen siendo la herramienta más confiable y eficaz para el control de la fiebre aftosa.
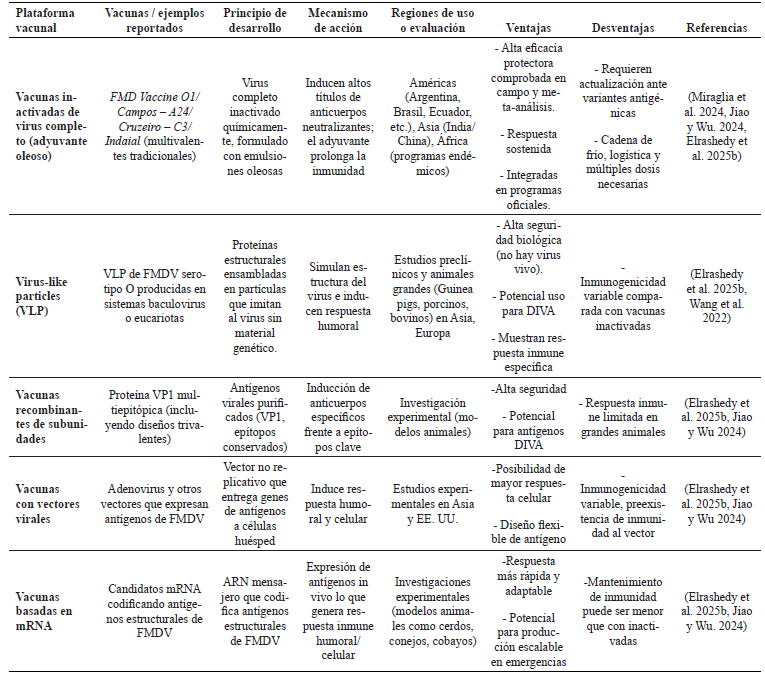
En conjunto, la evidencia científica reciente sintetizada en la Tabla 1 menciona que las vacunas inactivadas de virus completo continúan siendo la mejor estrategia vacunal contra la fiebre aftosa a nivel mundial, sin embargo, estas presentan limitaciones, como la necesidad de alta bioseguridad en su producción y la menor eficacia frente a variantes antigénicas emergentes. La mayoría de las vacunas tiene la capacidad de inducir altos títulos de anticuerpos neutralizantes, una protección robusta, lo que favorece las estrategias de control y erradicación de la enfermedad (Jemberu et al. 2020, Samy Abousenna et al. 2021). En contraste, las tecnologías vacunales emergentes incluyendo vacunas basadas en partículas similares a virus (VLP), vectores virales y plataformas de mRNA presentan ventajas potenciales en términos de seguridad biológica, flexibilidad de diseño antigénico; sin embargo, como se evidencia en la Tabla 1, estas plataformas aún muestran limitaciones inmunológicas, productivas y operativas que condicionan su aplicación a gran escala. Consecuentemente, las VLP, que no contienen material genético, retienen la conformación espacial de los antígenos virales y han demostrado estimular células presentadoras de antígeno (como dendríticas) de manera similar a las vacunas inactivadas, promoviendo así respuestas humorales significativas. En contraste, Lu et al. (2022) y Wang et al. (2022), destacan el potencial inmunológico de plataformas como VLP, vectores virales y vacunas de ácidos nucleicos para inducir respuestas humorales y celulares más equilibradas y mejorar aspectos de seguridad biológica; sin embargo, estos autores coinciden en que los resultados experimentales aún no superan la consistencia y eficacia observadas con las vacunas inactivadas en programas de vacunación a gran escala. En este contexto, y a la luz de la evidencia actual, dichas tecnologías deben considerarse como herramientas complementarias en desarrollo, más que como sustitutos inmediatos de las vacunas inactivadas tradicionales dentro de los programas oficiales de control y erradicación de la fiebre aftosa.
Desde una perspectiva inmunológica, de acuerdo con el artículo de Wubshet et al. (2024) se muestra que la vacunación contra la fiebre aftosa genera una respuesta protectora efectiva, principalmente a través de anticuerpos neutralizantes, que son considerados el principal indicador inmunológico de protección contra el virus de la fiebre aftosa (Wubshet et al. 2024). Los estudios de campo realizados en África revelaron que los animales vacunados tienen aproximadamente un 69% menor de riesgo de infección en comparación con aquellos que no han sido vacunados, lo que confirma que una respuesta humoral adecuada puede limitar la infección, la replicación viral y la transmisión (Jiao y Wu 2024). Esto confirma que, en condiciones reales, las vacunas inactivadas generan una respuesta humoral lo suficientemente fuerte como para disminuir la circulación del virus. Estos hallazgos son consistentes con los reportados por Miraglia et al. (2024), quienes notaron que los esquemas de vacunación optimizados con formulaciones oleosas no solo logran altos niveles de anticuerpos neutralizantes, sino que también prolongan la duración de la inmunidad y mejoran la capacidad de neutralización frente a cepas heterólogas dentro del serotipo O, aunque no logran una protección cruzada completa entre serotipos. Además, la duración de esta respuesta inmune depende de factores clave, como la concordancia antigénica entre las cepas de la vacuna y los serotipos que circulan, así como del cumplimiento de los esquemas de vacunación adecuados. En particular, es necesario aplicar esquemas primarios que incluyan al menos dos dosis iniciales, seguidas de revacunaciones periódicas, lo que ayuda a mantener niveles protectores de anticuerpos neutralizantes en la población. La falta o la aplicación irregular de estas dosis se relaciona con respuestas inmunes subóptimas y una disminución significativa de la eficacia de la vacuna observada en el campo.
Finalmente, todas estas plataformas vacunales se apoyan en la inducción de anticuerpos neutralizantes específicos y en la activación de células T colaboradoras para promover memoria inmunológica, cruciales para una protección sostenida frente a la fiebre aftosa, aunque la respuesta cruzada entre serotipos sigue siendo un reto debido a la alta variabilidad genética de FMDV (Lu et al. 2022, Hu et al. 2024). En conjunto, los avances descritos en la literatura reflejan un creciente esfuerzo por diseñar vacunas que no solo generen altos títulos de anticuerpos neutralizantes, sino que también potencie la respuesta inmune celular y genere memoria inmunológica de larga duración, adaptándose a las demandas de control epidemiológico (Fang y Liu 2022).
Desde una perspectiva comparativa, el análisis económico que presentan Lu et al. (2022) se alinea con la evidencia de estudios recientes que examinan la efectividad y aplicabilidad de diversas plataformas de vacunas contra la fiebre aftosa. Los autores señalan que las vacunas de virus completo inactivado conllevan mayores costos de producción, debido a los estrictos requisitos de bioseguridad y la necesidad de revacunaciones periódicas. Sin embargo, los estudios de eficacia en campo y los metaanálisis respaldan que esta inversión se traduce en una protección inmunológica más robusta y en una reducción significativa del riesgo de infección, lo que justifica su costo-efectividad en programas de control y erradicación (Miraglia et al. 2024, Wubshet et al. 2024). Por otro lado, las revisiones que se enfocan en plataformas emergentes, como las vacunas basadas en VLP, vectores virales y tecnologías de ácidos nucleicos, coinciden en que estas alternativas ofrecen ventajas potenciales en términos de seguridad biológica y simplificación de los procesos de producción, lo que podría ayudar a reducir costos operativos a largo plazo. Sin embargo, también enfatizan que los altos costos iniciales de investigación, desarrollo y escalamiento industrial, junto con una eficacia inmunológica que aún es variable, limitan su competitividad económica frente a las vacunas inactivadas tradicionales (Lu et al. 2022, Wang et al. 2022). Aunque las nuevas plataformas de vacunas representan una inversión estratégica con un potencial futuro, las vacunas inactivadas siguen siendo la opción más costo-efectiva y viable para su implementación inmediata en programas nacionales y regionales de control de la fiebre aftosa, especialmente en contextos donde la erradicación depende de mantener altas y sostenidas coberturas vacunales (Chathuranga et al. 2022, Ren et al. 2024). En conjunto, la discusión y análisis entre artículos sugiere que las discrepancias entre plataformas vacunales no radican únicamente en su capacidad inmunogénica, sino en la interacción entre eficacia, viabilidad operativa y costos, lo que explica por qué las vacunas inactivadas continúan siendo el estándar de referencia, mientras que las tecnologías emergentes se perfilan como complementos prometedores para el futuro de los programas de erradicación.
Métodos de caracterización molecular. La caracterización molecular del virus de la fiebre aftosa utiliza una variedad de técnicas que nos permiten explorar la variabilidad genética, establecer relaciones filogenéticas entre diferentes cepas virales y evaluar su impacto epidemiológico en distintas regiones (Medina y Díaz-San Segundo 2024). Uno de los métodos más comunes es la reacción en cadena de la polimerasa con transcriptasa reversa (RT-PCR), que facilita la amplificación de segmentos específicos del genoma viral, como la región que codifica la proteína estructural VP1. Esta proteína es altamente variable y resulta muy útil para diferenciar entre serotipos y linajes (Wang et al. 2022).
Después de esto, la secuenciación del gen VP1, junto con análisis filogenéticos, nos ayuda a formar agrupaciones genéticas y a rastrear cómo se disemina el virus en distintas regiones (Li et al. 2023). También se utilizan técnicas como la RT-qPCR para cuantificar el virus, y la RT-PCR en tiempo real multiplex, que es ideal para detectar varios serotipos al mismo tiempo. En un estudio realizado en Egipto, los autores realizaron una RT-qPCR utilizando nuevos conjuntos de cebadores y sondas diseñados en regiones conservadas dentro de la secuencia codificante de VP1, para la detección específica de los serotipos SAT 2 y O del FMDV los cuales son endémicos de esta región. Otros enfoques más avanzados incluyen la secuenciación del genoma completo a través de plataformas de alto rendimiento (NGS), que nos brindan información detallada sobre mutaciones, recombinación y evolución viral (Wang et al. 2022). Estas herramientas moleculares son esenciales para diseñar vacunas efectivas y para fortalecer los programas de vigilancia epidemiológica.
Ecuador ha enfrentado varios brotes de fiebre aftosa (FMD, por sus siglas en inglés), especialmente en la última década del siglo XX y los primeros años del XXI, siendo el serotipo O el más común. La falta de una buena implementación de las campañas de vacunación y el escaso control sobre el movimiento de animales facilitaron la propagación del virus en el país (Rivera et al. 2023). Después de la epidemia de 2009-2010, la intervención técnica de PANAFTOSA 2025 llevó a una reestructuración del programa nacional de control, lo que mejoró la cobertura de vacunación, el monitoreo y la trazabilidad del ganado, complementado con buenas prácticas de vacunación y gestión del registro de fincas, lo que resultó en una disminución rápida de la incidencia de la enfermedad. Además, la literatura científica reconoce que la combinación de vigilancia sólida, campañas nacionales de vacunación y medidas de bioseguridad son estrategias esenciales para reducir la incidencia de la fiebre aftosa y avanzar hacia estatus libre de enfermedad (Byamukama 2025). De acuerdo a un artículo realizado sobre la fiebre aftosa, el serotipo más prevalente en Ecuador es el O durante los brotes de fiebre aftosa entre los años 2009 y 2010 (Rivera et al. 2023) Se caracterizaron cepas del virus serotipo O y se determinó que presentaron diferencias genéticas y antigénicas aproximadamente de 10% con respecto a la cepa vacunal específicamente en la región VP1. De acuerdo a investigaciones la alta variación antigénica del virus de la fiebre aftosa serotipo O contribuye a que las vacunas diseñadas con cepas antiguas no proporcionen una protección adecuada frente a variantes circulantes, lo cual puede explicar por qué la vacuna utilizada alrededor de 2010 no fue completamente efectiva frente a las variantes de serotipo O presentes en Ecuador en ese momento (Rivera et al. 2023, Wang et al. 2024). Las cepas del virus fiebre aftosa circulantes en Ecuador mostraban cambios genéticos y antigénicos suficientes para disminuir la eficacia y eficiencia de las vacunas que en ese momento se estaban administrando (OPS/PANAFTOSA 2022). Esto sugiere que el movimiento de los animales y la variabilidad del virus contribuyen a una rápida dispersión del virus además de conferir ciertas capacidades para evadir los anticuerpos generados a través de las vacunas (Onodera et al. 2023). Por este motivo, es recomendable actualizar las vacunas, cumplir con el esquema de vacunación completo (Dabasa y Abunna 2021, García et al. 2025) y realizar análisis más exhaustivos sobre la estructura del virus debido a que constantemente está cambiando, también revisar la formulación de la vacuna para mejorar la protección frente a las variantes emergentes de esta manera asegurar una protección duradera.
En Ecuador, los programas de erradicación de la fiebre aftosa han sido implementados de manera sostenida y coordinada bajo la conducción de la autoridad veterinaria nacional, AGROCALIDAD, en alineación con las estrategias regionales del Programa Hemisférico para la Erradicación de la Fiebre Aftosa (PHEFA). Como resultado de la aplicación sistemática de campañas de vacunación obligatoria, vigilancia epidemiológica activa y pasiva, control de movilización animal y fortalecimiento de las capacidades de diagnóstico y respuesta. Ecuador obtuvo el estatus de libre de fiebre aftosa con vacunación en 2015 para la región continental, y sin vacunación en las Islas Galápagos (Maradei et al. 2014). La evidencia reciente destaca que Ecuador no ha registrado casos de fiebre aftosa desde 2011, lo que refleja la efectividad del enfoque integral adoptado, que combina inmunización estratégica, monitoreo serológico postvacunal, simulacros de emergencia sanitaria y capacitación continua del personal veterinario (Quezada Morocho 2018). Estas acciones no solo han permitido preservar el estatus sanitario alcanzado, sino que también posicionan al país en una fase avanzada del proceso de erradicación, con el objetivo a mediano plazo de transitar hacia un escenario libre de fiebre aftosa sin vacunación en el territorio continental, en concordancia con las metas regionales establecidas por el PHEFA (OPS/PANAFTOSA 2022, AGROCALIDAD 2023, WOAH 2023).
A nivel mundial, la lucha contra la fiebre aftosa se ha llevado a cabo a través de iniciativas coordinadas que combinan el control sanitario, la vigilancia epidemiológica, el fortalecimiento de los servicios veterinarios y la cooperación internacional. Un elemento clave en este esfuerzo es la Estrategia Global para el Control de la Fiebre Aftosa, promovida por la Organización de las Naciones Unidas para la Alimentación y la Agricultura (FAO) y la WOAH. Esta estrategia utiliza herramientas como el Progressive Control Pathway for Foot-and-Mouth Disease (PCP-FMD) y la evaluación de los servicios veterinarios a través del Performance of Veterinary Services (PVS), ayudando a los países a seguir un proceso escalonado para mitigar riesgos y avanzar hacia el estatus de libre de enfermedad, ya sea con o sin vacunación (FAO 2023, OPS/PANAFTOSA 2022). En el ámbito regional, el Programa Hemisférico para la Erradicación de la Fiebre Aftosa (PHEFA), coordinado por el Centro Panamericano de Fiebre Aftosa y Salud Pública Veterinaria (PANAFTOSA/PAHO/WHO), ha sido un ejemplo destacado de cooperación intergubernamental desde 1988. Con planes de acción sucesivos (2021-2025 y 2026-2030), se ha logrado que más del 80% de la población bovina de las Américas esté en zonas libres de fiebre aftosa sin necesidad de vacunación, y países como Bolivia y Brasil han consolidado este estatus, contribuyendo significativamente al avance hacia la erradicación en la región (PAHO/WHO 2025). Estos programas demuestran tanto la viabilidad técnica de erradicar la enfermedad como la importancia de contar con estrategias armonizadas que incluyan una vacunación adecuada, vigilancia continua, preparación ante emergencias y un fortalecimiento institucional, todos pilares fundamentales para eliminar de manera definitiva esta enfermedad que tiene un impacto sanitario, económico y social significativo.
El FMDV es un problema constante para la salud de los animales en todo el mundo. Esto se debe a que se contagia fácilmente, causa problemas económicos y tiene mucha variabilidad genética. Entender cómo está estructurada la molécula, especialmente las proteínas estructurales como VP1, ha ayudado a determinar la capacidad de causar enfermedades que se propagan rápidamente. Además, la transmisibilidad del virus y la forma en que el virus entra, como el motivo RGD en el lazo GH. Esta información ha sido fundamental para crear vacunas más precisas y efectivas. La falta de un sistema para corregir errores mientras el virus se replica hace que surjan diferentes versiones del virus, conocidas como cuasi-especies. Esto dificulta el trabajo para controlar y prevenir el virus, ya que puede escapar de la defensa natural del cuerpo y de la protección que ofrecen las vacunas. La diferencia entre los serotipos y cepas no solo influye en cuán efectivas son las vacunas que tenemos ahora, sino que también requiere que estemos siempre vigilantes y actualicemos las vacunas que usamos en el campo. Si bien las vacunas actuales no generan inmunidad cruzada completa, su optimización mediante esquemas de vacunación adecuados permite ampliar la protección dentro de un mismo serotipo, lo cual es epidemiológicamente relevante para regiones donde circulan variantes del serotipo O. En conjunto, los hallazgos respaldan el uso continuo de vacunas inactivadas como pilar de los programas de control y erradicación de la fiebre aftosa, al tiempo que resaltan la importancia de ajustar tanto la composición antigénica como los esquemas de aplicación para maximizar la eficacia vacunal frente a la diversidad viral existente.
Es importante seguir haciendo investigaciones que combinen estudios sobre genes, enfermedades y el sistema inmunológico. También se debe fomentar la vacunación utilizando vacunas inactivadas con los esquemas de vacunación adecuados. Solo con un enfoque que combine diferentes disciplinas y esté al día, podremos crear estrategias de control que sean sostenibles y efectivas contra este patógeno que afecta a varios países.