Revista Veterinaria. 2026; 37(1)
https://doi.org/10.30972/vet.3719218
Revisión Bibliográfica




1Laboratorio de Inmunoparasitología, FCV-UNLP, La Plata (CP1900), Buenos Aires, Argentina.
2Consejo Nacional de Investigaciones Científicas y Técnicas (CONICET), La Plata (CP1900), Buenos Aires, Argentina.
3Instituto de Parasitología, Facultad de Veterinaria, Universidad de Berna, Langgassstrasse 122, Berna 3012, Suiza.
Recibido: 01 octubre 2025 / Aceptado: 22 febrero 2026
Resumen
La toxoplasmosis y la neosporosis representan importantes desafíos sanitarios en la producción caprina, ocasionando pérdidas reproductivas significativas y riesgos para la salud pública. Este trabajo analiza los aspectos biológicos, mecanismos de transmisión, manifestaciones clínicas, diagnóstico, impacto productivo y estrategias de prevención de Toxoplasma gondii y Neospora caninum en caprinos, con especial énfasis en la situación epidemiológica en Argentina. Bajo un enfoque de "Una Salud", se destaca la necesidad de implementar medidas de control integradas para mitigar las pérdidas económicas y reducir los riesgos zoonóticos, priorizando acciones de vigilancia epidemiológica y bioseguridad en los sistemas de producción caprina.
Palabras claves:Toxoplasma gondii, Neospora caninum, seroprevalencia, abortos, cabras, salud pública.
Abstract. Toxoplasmosis and neosporosis represent major health challenges in goat production, causing significant reproductive losses and posing risks to public health. This study/review analyzes/addresses the biological characteristics, transmission mechanisms, clinical manifestations, diagnostic approaches, impact on production, and prevention strategies related to Toxoplasma gondii and Neospora caninum infections in goats, with special emphasis on the epidemiological situation in Argentina. Within a One Health framework, the need for integrated control measures to mitigate economic losses and reduce zoonotic risks is emphasized, prioritizing epidemiological surveillance and biosecurity practices in goat production systems.
Key words: Toxoplasma gondii, Neospora caninum, seroprevalence, abortions, goats, public health.
La producción de cabras domésticas (Capra aegagrus hircus), es una actividad de profunda relevancia socioeconómica en numerosas comunidades rurales a nivel global, que se ve constantemente amenazada por desafíos sanitarios que comprometen directamente la productividad y rentabilidad. Entre estos, las enfermedades parasitarias causadas por protozoos intracelulares obligados como Toxoplasma gondii y Neospora caninum revisten importancia en la sanidad animal y particularmente T. gondii en la salud pública. Estos protozoos, distribuidos ampliamente a nivel mundial, tienen como principal manifestación clínica en caprinos la ocurrencia de abortos mediante infección transplacentaria, generando importantes pérdidas reproductivas y económicas. Además, ambas infecciones pueden cursar con cuadros subclínicos, mortalidad perinatal, fallos reproductivos como retorno al celo o infertilidad y persistencia intracelular de estos parásitos durante toda la vida de los animales (Lindsay y Dubey 2020, Dubey 2022).
La complejidad de la epidemiología de la toxoplasmosis y la neosporosis en caprinos se ve acentuada por sus ciclos de vida indirectos facultativos, donde felinos y caninos actúan como hospedadores definitivos (HD), respectivamente, liberando ooquistes que contaminan el ambiente. Los gatos y perros jóvenes o animales adultos inmunocomprometidos no controlados en los establecimientos constituyen los principales diseminadores de ooquistes en el ambiente.
La transmisión horizontal y vertical o también denominada transplacentaria (ya sea por infección exógena o endógena) contribuye a la persistencia de estas infecciones en los hatos o rebaños. A la par de su impacto productivo, la toxoplasmosis reviste una particular importancia zoonótica, siendo una preocupación de salud pública global, especialmente por el riesgo de transmisión a través del consumo de carne cruda o mal cocida y productos lácteos caprinos no pasteurizados. En contraste, la neosporosis, aunque no es una zoonosis, genera abortos recurrentes que afectan directamente la rentabilidad de los establecimientos. A nivel mundial, la seroprevalencia varía según la región, el tipo de sistema de producción y la presencia del HD (Rodrigues et al. 2021, Celi et al. 2022). La situación en Argentina y América del Sur es particularmente relevante, donde la seroprevalencia de ambas infecciones es considerable y la diversidad genética de T. gondii presenta linajes no canónicos, lo que añade complejidad a su dinámica epidemiológica (Ragozo et al. 2010, Clementino Andrade et al. 2013, Shwab et al. 2014).
El presente trabajo tiene como objetivo principal analizar en profundidad las características generales de la toxoplasmosis y la neosporosis caprina, incluyendo sus agentes etiológicos, ciclos biológicos, mecanismos de transmisión, patogenia en cabras, y las manifestaciones clínicas y lesiones asociadas. Se buscará consolidar el conocimiento existente sobre su prevalencia en Argentina y América del Sur, evaluar su impacto en la producción caprina y su relevancia en la salud pública bajo el enfoque de "Una Salud". Finalmente, se abordarán y promoverán estrategias actualizadas y eficaces de diagnóstico, control y prevención para ambas parasitosis en el contexto de la producción caprina.
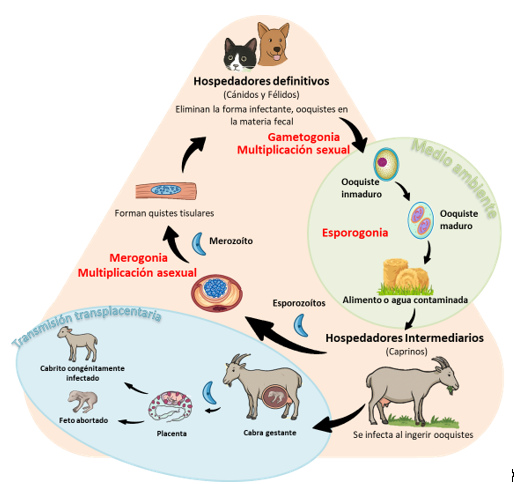
Agentes etiológicos y ciclo biológico. Ambos parásitos, T. gondii y N. caninum, poseen un ciclo indirecto facultativo, donde los felinos y caninos son los HD respectivamente, y numerosas especies de aves y mamíferos, incluidas las cabras, son los hospedadores intermediarios (HI) (Lindsay y Dubey 2020). Se reconocen tres formas infectantes en su ciclo: taquizoítos, bradizoítos y ooquistes. Los taquizoítos y bradizoítos se encuentran en los tejidos de los HI, mientras que los ooquistes, que se eliminan en las heces del HD, se encuentran en el ambiente.
Las cabras pueden infectarse con T. gondii y/o N. caninum por vía horizontal, ingiriendo los ooquistes que están presentes en el alimento y/o agua de bebida o por vía transplacentaria por pasaje de taquizoítos a través de la placenta. En las cabras u otros HI se produce un ciclo exclusivamente extraintestinal y de multiplicación asexual. Las formas infectantes penetran en distintas células nucleadas del hospedador y se multiplican como taquizoítos (estadios de multiplicación asexual rápida). Luego de un tiempo, los parásitos forman quistes tisulares, que contienen las formas parasitarias denominadas bradizoítos (estadios de multiplicación lenta), ubicados principalmente en el sistema nervioso central y tejido muscular. De esta manera, las cabras permanecen infectadas de forma crónica durante toda su vida (Figura 1). Los HD carnívoros (felinos o caninos) adquieren la infección ingiriendo quistes en el tejido de los HI, y en su intestino los parásitos se reproducen sexualmente eliminando en las heces ooquistes que se diseminan en el ambiente contaminando el alimento y/o agua de los caprinos. Además, T. gondii puede transmitirse entre HI (en ausencia de HD) por consumo de quistes tisulares, así como entre HD (en ausencia de HI) por ingestión de ooquistes (Lindsay y Dubey 2020, Dubey 2022).
Signos clínicos y lesiones en cabras. La toxoplasmosis y la neosporosis son enfermedades parasitarias de importancia en la sanidad caprina, como consecuencia de pérdidas reproductivas, viabilidad de los fetos y manifestaciones clinicopatológicas, incluso la muerte en cabras adultas (Dubey et al. 2020, Rodrigues et al. 2020, 2021, Nayeri et al. 2022).
En el contexto de aborto en caprinos, aquellos de tipo infecciosos representan una de las principales causas de pérdidas económicas en la producción caprina a nivel mundial. La etiología es compleja y multifactorial, con agentes bacterianos, virales y parasitarios involucrados. Dentro de estos últimos, T. gondii y N. caninum son protozoos intracelulares obligados capaces de inducir abortos mediante infección transplacentaria, por ingestión de ooquistes esporulados excretados por felinos o recrudescencia ante cambios inmunológicos u hormonales respectivamente.
Toxoplasmosis caprina. El signo clínico más característico de la infección por T. gondii es el aborto cuando afecta a hembras preñadas, aunque depende del momento de la gestación en la que se produce la infección y el daño a la placenta o a los tejidos fetales, como también la virulencia de la cepa de T. gondii. Durante la infección aguda los signos clínicos son variados e inespecíficos debido a la multiplicación rápida de los protozoos en diversos tejidos, sin embargo, la severidad depende del estado del sistema inmunitario. Es crucial considerar que, períodos fisiológicos como la gestación, parto y el pico de lactancia son sumamente estresantes y pueden comprometer la inmunidad, y consecuentemente permitirían la reactivación de infecciones crónicas por T. gondii. Esto aumentaría la probabilidad de fallas reproductivas y de transmisión de taquizoítos con eventual aparición en el calostro y leche (Steffen et al. 2024). Específicamente, en cabras gestantes, la multiplicación de T. gondii en los cotiledones placentarios produce daño local directo y necrosis progresiva de los mismos originando la muerte fetal por insuficiente provisión de oxígeno y nutrientes. En un reporte de caso en Paraná, Brasil se notificó durante el año 2013 un brote de toxoplasmosis clínica en cabras lecheras de raza Saanen. Los signos clínicos observados fueron linfadenopatía, diarrea y pérdida de peso en 33 de las 179 cabras del establecimiento. Seis hembras abortaron o tuvieron cabritos débiles al final de la gestación. Tres cabras adultas murieron y alrededor del 60% presentaron trastornos reproductivos (Neto et al. 2018, Dubey 2022). En cuanto a infecciones experimentales en cabras, la sintomatología varía según la dosis de ooquistes ingeridos, incluyendo hipertermia, letargia, inapetencia y disnea. La exposición de hembras preñadas resulta en abortos o el nacimiento de crías infectadas. El aborto más precoz se registró a los nueve días p.i. con parasitemia detectable entre los cuatro y ocho días p.i. que duró entre tres y diez días. Se ha documentado la presencia de quistes de T. gondii en órganos como el hígado, músculos, cerebro y corazón, persistiendo hasta por 441 días p.i. (Dubey 2022). Además, en cabritos infectados congénitamente, el parásito ha sido aislado en diversos tejidos, incluyendo músculos, cerebro, corazón, pulmones y médula espinal (Dubey et al. 2020, Dubey 2022).
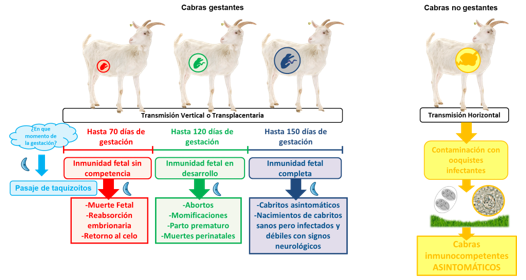
Cabras gestantes. Dependiendo de la etapa de la gestación en que se produce la infección, sumado al daño en placenta o tejidos fetales, el parásito producirá desde muerte embrionaria y reabsorción fetal, hasta el nacimiento de cabritos débiles o clínicamente normales pero infectados (Dubey et al. 2020). Si la infección transplacentaria ocurre en la gestación temprana (menos de 50 días), se produce la muerte embrionaria y reabsorción fetal, debido a que el sistema inmune del feto es rudimentario y por lo tanto no es capaz de generar una respuesta eficaz para controlar la multiplicación del parásito, por lo que las cabras pueden retornar al servicio (AbouZeid et al. 2010, Lindsay y Dubey 2020). En etapas de gestación más avanzada, los efectos de la infección dependerán de la eficacia de la respuesta inmune del feto para lograr vencerla, así puede ocurrir muerte fetal, con aborto y momificación, más frecuentemente cuando la infección ocurre a la mitad de la gestación (70-90 días) y el nacimiento de cabritos muertos, cabritos débiles o cabritos sanos pero congénitamente infectados en la gestación tardía (más de 110 días) (Figura 2) (AbouZeid et al. 2010, Lindsay y Dubey 2020, de Oliveira et al. 2022). Estas lesiones pueden ocurrir de manera recurrente debido a la reactivación de infecciones latentes o crónicas ante cambios inmunológicos y hormonales (Lindsay y Dubey 2020, Dubey et al. 2020).
Cabras no gestantes (vacías). La infección natural en cabras no gestantes es generalmente asintomática, aunque las cabras a veces pueden presentar fiebre, pérdida de apetito, diarrea, dificultad respiratoria y hasta signos nerviosos (Neto et al. 2018, Dubey et al. 2020).
Cabritos o recría. En cabritos afectados, la leucomalacia focal en la sustancia blanca del cerebro provocada por el parásito es común, originando debilidad generalizada con dificultad para alimentarse por falta de succión o flacidez para pararse y muerte en 48 horas (AbouZeid et al. 2010, Lindsay y Dubey 2020). También es frecuente observar en gestaciones múltiples, el nacimiento de cabritos muertos acompañado por el nacimiento del otro débil o del feto momificado. Por otro lado, se ha informado en establecimientos con alta prevalencia y título de anticuerpos anti-T. gondii altos asociación con muertes perinatales (Steffen et al. 2021).
Machos. La infección natural en machos suele cursar de manera asintomática. No obstante, tras la inoculación experimental con taquizoítos u ooquistes maduros, se ha observado como principal signo clínico hipertermia (40,6 °C) alrededor del quinto día post-inoculación (p.i.). Además, se han reportado episodios de anorexia y letargo entre los tres y siete días p.i. en todos los animales inoculados (Santana et al. 2010, Dubey 2022). Aunque el aparato reproductor masculino no constituye un órgano blanco primario de T. gondii, distintos estudios han evidenciado la presencia de ADN de T. gondii en muestras seminales de machos sometidos a inoculación experimental (Santana et al. 2010, Lopes et al. 2013, Dubey 2022). Asimismo, se ha documentado la transmisión del parásito a hembras caprinas y ovinas a través del semen, ya sea por apareamiento con machos infectados de forma experimental (Lopes et al. 2013) o mediante inseminación artificial con semen contaminado con taquizoítos de T. gondii (Wanderley et al. 2013). No obstante, algunos autores sugieren que esta vía de transmisión podría tener una relevancia epidemiológica limitada (Lindsay y Dubey 2020, Dubey 2022).
Avances en el desarrollo de vacunas frente a T. gondii. La búsqueda de una vacuna efectiva contra la toxoplasmosis es un objetivo crucial, tanto por su impacto en la salud pública dada la inocuidad de los productos de origen caprino, como en la producción ganadera. Es importante destacar que, aunque la investigación avanza con nuevas tecnologías, hasta el momento no se dispone de vacunas aprobadas para su uso en humanos, ni en caprinos. Actualmente, la única vacuna comercial disponible es Ovilis Toxovax®, una vacuna viva atenuada (cepa S48) autorizada solamente en Reino Unido, Francia y Nueva Zelanda. Su aplicación en ovejas antes del servicio reduce significativamente los abortos y aumenta la viabilidad de los corderos, con efecto protector por hasta 18 meses, aunque, el costo, su corta vida útil y la posibilidad de reversión a la virulencia de esta vacuna, y el riesgo de infección para los humanos que la manipulan limita su uso.
Las investigaciones sobre estrategias de inmunización contra la toxoplasmosis en caprinos han explorado diversos enfoques experimentales, incluyendo vacunas vivas atenuadas derivadas del propio protozoo T. gondii y como así también la inmunización con parásitos estrechamente relacionados del género Hammondia, utilizando la posible inmunidad cruzada entre estos agentes. En estudios de inmunización cruzada en caprinos, la vacunación con 106 ooquistes de H. hammondi ha demostrado ser efectiva. De un grupo de seis cabras vacunadas antes del servicio, cinco parieron crías sanas, a diferencia de las cabras no vacunadas que abortaron y sufrieron retención de placenta. Aunque se observó una baja producción de anticuerpos, todas las cabras inmunizadas sobrevivieron al desafío con T. gondii, lo que sugiere que la protección es principalmente de tipo celular. Por otro lado, la vacunación con H. heydorni resultó en una protección limitada, con solo una de cada cuatro cabras sobreviviendo al desafío y sin generar una respuesta de anticuerpos protectores. Estos resultados limitan su potencial como candidato vacunal (Dubey 2022, Hasan y Nishikawa 2022). Además, también se probó experimentalmente en cabras la vacuna viva atenuada basada en la cepa S48 (Ovilis Toxovax®), aprobada en ovejas. Observaron que las cabras inmunizadas un mes antes del servicio mostraron una menor tasa de abortos tras la infección con 104 ooquistes de T. gondii a los 90 días de gestación. Este resultado indica que la cepa S48 puede conferir protección contra la infección transplacentaria en caprinos, aunque su uso sigue siendo experimental (Hasan y Nishikawa 2022).
En este contexto, un estudio reciente en Argentina, realizado en corderos, comparó dos sistemas de producción de vacunas de nueva generación: una vacuna recombinante convencional expresada en E. coli (NbHsp90.3-SAG1HC) y otra desarrollada a en una plataforma vegetal, (Arabidopsis thaliana - AtHsp81.2-SAG1HC). La vacuna recombinante indujo una fuerte respuesta de anticuerpos (humoral), mientras que la vacuna basada en plataforma vegetal generó una respuesta de tipo celular. Este último tipo de respuesta resultó ser particularmente efectivo, ya que demostró una reducción estadísticamente significativa de aproximadamente el 80% de las lesiones histopatológicas en los corderos desafiados experimentalmente con T. gondii. Por lo tanto, estos resultados indican que, a pesar de las distintas vías de protección, la vacuna a partir de una plataforma vegetal ofrece una defensa robusta contra el daño tisular causado por infección de este parásito (Campero et al. 2025).
La disponibilidad de una vacuna efectiva en nuestro país es, sin duda, promisoria. Estos resultados son alentadores y abren nuevas vías para el desarrollo de estrategias de inmunización contra la toxoplasmosis. Sin embargo, para capitalizar plenamente estos avances, es fundamental que los entes nacionales regulen y estandaricen los métodos de diagnóstico, y establezcan una política sanitaria clara para el control de esta enfermedad. Un desafío pendiente radica en la ausencia de pruebas serológicas capaces de diferenciar los anticuerpos generados por la vacunación de aquellos producidos en respuesta a infecciones naturales, lo que actualmente obstaculiza las medidas de control basadas en la identificación y eliminación de animales seropositivos. Resolver esta limitación será clave para una implementación exitosa y una gestión efectiva de la enfermedad. La integración de estas tecnologías podría ser clave para el control efectivo de esta zoonosis, protegiendo tanto al ganado como a la salud pública.
Diversidad genética y distribución de T. gondii. La detección y caracterización de T. gondii se realiza principalmente mediante PCR, una técnica molecular que identifica y amplifica selectivamente segmentos de ADN del parásito. Diversos genes se utilizan como blancos de amplificación, incluyendo genes únicos como P30 o genes repetidos como el gen B1, la secuencia TGRIE, el ADNr 18s y los loci SAG1 y SAG2. Dentro de las variantes de PCR, la PCR anidada (nPCR) puede aumentar la sensibilidad de detección, además, la PCR en tiempo real (qPCR) ofrece la ventaja de cuantificar el ADN del parásito, siendo un método muy sensible y específico (capaz de detectar el ADN de 1 taquizoíto). Estos métodos de detección indican la presencia del agente en el tejido (Bernstein et al. 2018, Lindsay y Dubey 2020, Dubey 2022).
La estructura poblacional de T. gondii es altamente diversa y exhibe variaciones significativas entre diferentes regiones geográficas. Para una mayor caracterización genética, particularmente mediante técnicas de nPCR-RFLP (Fragmentos de Restricción de Longitud Polimórfica amplificados por nPCR) que emplea 10 marcadores genéticos, incluidos SAG1, SAG2, SAG3, BTUB, GRA6, c22-8, c29-2, 358, PK1 y Apico, las cepas de T. gondii se han clasificado en tres genotipos canónicos: Tipo I, Tipo II y Tipo III (Howe y Sibley 1995, Howe et al. 1997, Bernstein et al. 2018, Dubey 2022). Estos genotipos difieren en su virulencia y patrones de distribución, siendo prevalentes tanto en América como en Europa.
Los genotipos Tipo II y Tipo III se asocian con infecciones menos virulentas, caracterizadas por una alta capacidad para inducir infecciones crónicas. En contraste, el genotipo Tipo I es altamente virulento, con una dosis infectiva letal muy baja en modelos murinos, no propenso a establecer infecciones crónicas, y está más frecuentemente implicado en casos de toxoplasmosis congénita en humanos. El genotipo Tipo II es el más prevalente en infecciones humanas, especialmente en individuos inmunocomprometidos, como aquellos con síndrome de inmunodeficiencia adquirida (SIDA). Por su parte, el genotipo Tipo III se aísla con mayor frecuencia en animales (VanWormer et al. 2014).
En regiones de América del Sur, particularmente en Brasil y Argentina, la población de T. gondii muestra una estructura genética aún más compleja, dominada por linajes no canónicos. Estos linajes representan una mayor diversidad genética, lo que refleja patrones evolutivos distintos y probablemente una mayor adaptación a hospedadores y ambientes locales (Shwab et al. 2014, Ajzenberg 2015).
La mayoría de los trabajos que realizan caracterización molecular de T. gondii en cabras son a partir de muestras en frigorífico, encontrándose también que los genotipos II y III son los más frecuentes en cabras de Europa, Estados Unidos y en África (Dubey et al. 2011, Gebremedhin et al. 2014, Paştiu et al. 2015). Sin embargo, aislamientos de T. gondii realizados en Brasil, Argentina y Estados Unidos demostraron que también existe una diversidad genética importante de este parásito en las cabras de esas regiones, con predominio de genotipos no clonales. La mayoría de estos estudios fueron también realizados a partir de tejidos de cabras destinados a consumo humano (Ragozo et al. 2010, Clementino Andrade et al. 2013, Rêgo et al. 2017), aunque también se han descripto en algunos pocos casos de abortos en cabras infectadas naturalmente (Silva Filho et al. 2008, de Oliveira et al. 2018), incluso en nuestro país (Unzaga et al. 2014). Es interesante realizar más estudios sobre los genotipos de T. gondii que circulan en las cabras de nuestra región debido a que podrían tener un comportamiento biológico y/o patogenia particular en esta especie.
La neosporosis, causada por N. caninum también induce abortos y malformaciones fetales en cabras y nacimientos de cabritos débiles (Dubey et al. 2017, Rodrigues et al. 2021, Nayeri et al. 2022), demostrándose que las cabras seropositivas tienen 3 veces más probabilidades de abortar que las seronegativas (Rodrigues et al. 2020). En Argentina, se ha reportado la presencia de anticuerpos contra N. caninum en fetos de caprinos abortados, con una seroprevalencia del 20% en suero (Unzaga et al. 2014), y se ha identificado mediante una revisión utilizando metaanálisis que la infección a nivel global fue del 7% en fetos abortados utilizando métodos moleculares (Nayeri et al. 2022). A pesar de su menor prevalencia en comparación con bovinos y ovinos, el impacto de N. caninum en la producción caprina sigue siendo un aspecto relevante que requiere mayor investigación para comprender sus implicaciones sanitarias y económicas en el país debido a que no se conoce la relación entre estas seroprevalencias con la frecuencia en la aparición de abortos en cabras.
Se han descrito lesiones como hidrocefalia, hipoplasia cerebelosa y porencefalia, además de infiltrados inflamatorios mononucleares en cerebro, pulmón, riñón y corazón de fetos abortados (Moreno et al. 2012, Costa et al. 2014). La encefalitis multifocal con necrosis e inflamación es común en estudios histopatológicos, y es acompañada de gliosis focal o difusa con presencia de quistes tisulares menores de 20 μm en tejido nervioso de fetos abortados (Moreno et al. 2012, Costa et al. 2014, González-Warleta et al. 2018). Por lo tanto, el tejido nervioso, en particular el cerebro constituye el tejido más adecuado para el diagnóstico de neosporosis en fetos caprinos abortados. Sin embargo, la identificación puede resultar compleja debido a la inespecificidad de los signos clinicopatológicos, la similitud con infecciones por T. gondii y la baja carga tisular del parásito en los tejidos afectados. La distinción entre N. caninum y otros protozoos, particularmente T. gondii, puede lograrse mediante inmunohistoquímica (IHC) o técnicas de detección molecular de ADN parasitario (PCR) (Moreno et al. 2012, Costa et al. 2014, Dubey et al. 2017, González-Warleta et al. 2018). En este contexto, la prevalencia informada de infección por N. caninum en fetos caprinos abortados se ha estimado en un 5,4% mediante hallazgos histopatológicos y en un 19,51% mediante IHC, lo que resalta la utilidad de esta última en el diagnóstico etiológico (Nayeri et al. 2022). En Argentina, Unzaga et al. (2014) estimaron la seroprevalencia de la infección por N. caninum en fetos de cabra abortados y observaron que el 20% de los animales fueron seropositivos para este parásito. A su vez, Campero et al. (2018) reportaron la primera detección y caracterización molecular de N. caninum en un feto caprino. En Brasil, Mesquita et al. (2013) evidenciaron que la transmisión transplacentaria de N. caninum ocurre con mayor frecuencia en cabras con títulos elevados de anticuerpos (≥200), especialmente a partir de la segunda mitad de la gestación, afectando a 9 de 13 animales (69,2%). La infección congénita genera respuesta serológica persistente en los cabritos durante toda la vida, mientras que las infecciones adquiridas postnatales muestran una respuesta transitoria con picos serológicos ante nuevas exposiciones al parásito mostrando mayor probabilidad de transmisión transplacentaria (Mesquita et al. 2013, Dubey et al. 2017). Es decir, que la presencia de títulos altos de este protozoo durante la gestación puede indicar infección activa, ya sea por reactivación del protozoo o por infección exógena. En estudios experimentales, las cabras infectadas gestantes desarrollaron títulos de hasta 25.600 en la primera gestación, mientras que, en la segunda gestación, sin re-inoculación, los valores oscilaron entre 400 y 3.200 (Lindsay et al. 1995, Dubey et al. 2017).
La presencia de ADN de N. caninum en tejido nervioso y muscular de rumiantes ha sido demostrada mediante PCR. Si bien los reportes son más frecuentes en bovinos y ovinos, la detección en caprinos ha sido confirmada, aunque los estudios son escasos (Dubey et al. 2017, Amdouni et al. 2018, Qian et al. 2020). En China, un estudio analizó muestras de sistema nervioso de cabras sacrificadas en frigorífico revelando una prevalencia del 2,8 % (12/422) de N. caninum, sin diferencias en relación con la edad, el sexo o la región de los animales (Qian et al. 2020). En el norte de África, se detectó una prevalencia molecular global del 19 % (23/121) en muestras de carne de cabras adultas obtenidas en frigorífico. En este estudio la prevalencia más alta se observó en cabras de 1 a 4 años, aunque sin diferencias según la localidad o la raza de los animales (Amdouni et al. 2018). En Brasil, un estudio reveló un 1,96% (2/102) de muestras positivas por PCR en tejido nervioso de cabras de frigorífico (Silva et al. 2009). En otro estudio realizado también en Brasil (Nakagaki et al. 2016) examinó a ocho cabras adultas infectadas naturalmente con N. caninum, detectado por PCR ADN del parásito en el 37% (133/359) de las muestras de varios tejidos, con excepción de piel. El sistema nervioso y muscular esquelético (cleidooccipital, tríceps braquial y semimembranoso) fueron los que presentaron el mayor porcentaje de positividad (44,4%; 28/63 y 42,8%; 72/168, respectivamente). Estos hallazgos sugieren la importancia de incluir el análisis de estos tejidos en el diagnóstico de la infección por N. caninum mediante PCR. Nakagaki et al. (2016) encontraron correlación entre los títulos de anticuerpos y la edad de los animales, y los cortes histológicos no revelaron la presencia de quistes de N. caninum en los tejidos analizados. Esta ausencia de quistes tisulares en infecciones naturales en caprinos, así como en modelos experimentales, tanto en ratas y jerbos, ha sido sugerida por otras investigaciones (Vonlaufen et al. 2002, Costa et al. 2018).
En conclusión, la toxoplasmosis y la neosporosis representan amenazas significativas para la reproducción y producción caprina, con manifestaciones clínicas y lesiones similares, pero con diferencias clave en el diagnóstico y transmisión. La identificación precisa mediante análisis histopatológicos, inmunohistoquímicos, serológicos y moleculares es esencial para el control y manejo de estas enfermedades en explotaciones caprinas (Dubey et al. 2017).
Avances en el desarrollo de vacunas y control frente a N. caninum. Aunque la vacunación es una alternativa más sostenible y costo-beneficio efectiva que los programas de eliminación del ganado, actualmente no existe una vacuna comercial disponible contra la neosporosis en rumiantes.
La única vacuna inactivada disponible (C548 NeoGuard™, Intervet) fue retirada en 2009 por su baja eficacia y resultados inconsistentes (Hemphill et al. 2016). En términos de eficacia, el diseño de vacunas exitosas requiere bloquear las etapas del ciclo de vida, como la invasión celular, replicación intracelular y simular la respuesta inmunitaria natural de los hospedadores. Las vacunas inactivadas y de subunidades han demostrado ser seguras, pero no generan una respuesta inmunitaria protectora adecuada frente al aborto o la transmisión transplacentaria. Por su parte, las vacunas vivas atenuadas han mostrado la mejor protección inmunitaria, aunque presentan riesgos de seguridad, como la posible reversión a la virulencia durante la gestación (Goodswen et al. 2013, Hemphill et al. 2016, Dubey et al. 2017). En este sentido, se investigan cepas de baja virulencia, tanto naturales como inducidas, y se exploran nuevas generaciones de vacunas basadas en proteínas recombinantes, ADN o vectores virales. Estas buscan bloquear procesos fundamentales del ciclo biológico, como la adhesión, invasión y formación de la vacuola parasitófora del taquizoíto, mediante la inducción de respuestas inmunitarias dirigidas contra proteínas de superficie o secretadas por organelas especializadas (micronemas, roptrias y gránulos densos) (Hemphill et al. 2016). Aunque se han evaluado diversas proteínas candidatas con resultados variables, el desarrollo de vacunas seguras y eficaces continúa siendo una necesidad prioritaria. Cabe señalar que la gran mayoría de estos avances tienen como foco los bovinos, especie en la cual el impacto productivo y económico de la neosporosis es mayor, mientras tanto, en caprinos la investigación en estrategias vacunales o quimioterapéuticas es escasa y los progresos prácticamente nulos, lo que refleja una brecha importante en el conocimiento y en el desarrollo de medidas específicas para pequeños rumiantes.
Diagnóstico de T. gondii y N. caninum en caprinos . El diagnóstico de la infección por T. gondii y N. caninum en caprinos, debe abordarse desde una perspectiva integral, tanto a nivel individual como de rebaño (Figura 3). A nivel individual, se requiere diferenciar infección activa, aguda, crónica o transplacentaria. A nivel poblacional, es fundamental caracterizar la circulación del agente en la explotación para orientar las estrategias de control (Dubey et al. 2017, Dubey 2022).
El diagnóstico de infección por estos protozoarios en caprinos combina métodos directos (detección del agente o de su ADN en tejidos o fluidos corporales) e indirectos (detección de anticuerpos específicos), en diferentes líquidos corporales como suero sanguíneo, líquidos fetales y leche, a través del uso de distintas pruebas inmunoserológicas. La integración de técnicas serológicas, moleculares e histopatológicas es esencial para establecer un diagnóstico etiológico certero, especialmente en casos de aborto. Las muestras recomendadas para arribar a un diagnóstico son fetos completos, placenta completa, suero de la madre (pareado), y líquidos fetales.
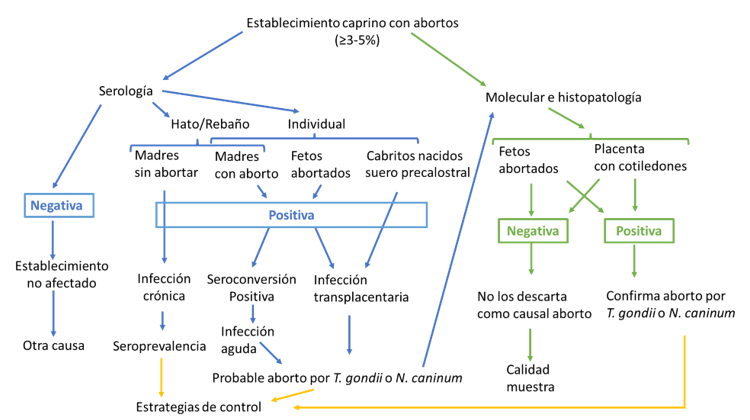
Métodos diagnósticos directos . El diagnóstico definitivo de aborto asociado a T. gondii o N. caninum requiere la detección directa del agente en tejidos fetales o placentarios (Dubey et al. 2020, Dubey 2022).
Se recomienda tomar muestras de:
Encéfalo fetal (que incluye el cerebro, el cerebelo y el tronco encefálico).
Pulmón, hígado, corazón y lengua.
Placenta completa, con especial atención a los cotiledones.
La PCR constituye la técnica de referencia para la identificación de ADN parasitario en tejidos, mientras que la histopatología e IHC la complementan al permitir la valoración de lesiones compatibles, como encefalitis necrotizante no supurativa, hepatitis, miocarditis, y la visualización directa de quistes tisulares o taquizoítos. El hallazgo de ADN parasitario en tejido fetal confirma infección congénita; sin embargo, la correlación causal con el aborto debe apoyarse en la presencia de lesiones histopatológicas específicas. La detección de ADN de T. gondii o N. caninum en tejidos fetales o placentarios confirma la infección transplacentaria, pero la atribución causal del aborto debe apoyarse en hallazgos histopatológicos característicos, y siempre que sea posible, con serología materna para interpretar adecuadamente los resultados.
Métodos diagnósticos indirectos . Las pruebas inmunoserológicas constituyen una herramienta fundamental para el diagnóstico y la vigilancia epidemiológica de enfermedades infecciosas en animales vivos. Estas pruebas permiten detectar la presencia de anticuerpos específicos contra un agente, lo que indica que el animal ha estado en contacto con dicho agente en algún momento de su vida. Por ello, si bien son ampliamente utilizadas para el estudio de la enfermedad en poblaciones animales, es importante considerar que la detección de anticuerpos refleja exposición previa y no necesariamente infección activa. Entre las pruebas serológicas más empleadas se destacan, la inmunofluorescencia indirecta (IFI) y el ensayo inmunoenzimático (ELISA). Ambas metodologías han sido validadas extensamente para su uso en pequeños rumiantes, demostrando alta sensibilidad y especificidad, permitiendo cuantificar el nivel de anticuerpos. Estas técnicas pueden aplicarse sobre diferentes tipos de muestras biológicas, tales como suero sanguíneo, líquido pleural y leche, lo que amplía su aplicabilidad en diferentes contextos de muestreo y vigilancia sanitaria (Dubey et al. 2020, Dubey 2022).
Serología materna. El análisis serológico en madres permite caracterizar el estado inmunológico y orientar el diagnóstico epidemiológico:
En los hatos caprinos que se registren abortos y se sospeche de toxoplasmosis o neosporosis, se recomienda el sangrado para la obtención de suero de todas o bien de una cantidad representativa de cabras que abortan y de la misma cantidad de cabras preñadas que no hayan abortado, para poder detectar asociaciones entre la presencia de abortos y los títulos de anticuerpos específicos.
Una única determinación positiva no permite establecer causalidad cuando ese animal tuvo un aborto, debido a la posible presencia de infecciones crónicas pasadas.
Se recomienda la recolección de muestras pareadas: una en el momento del aborto y otra a las 3-4 semanas posteriores. La seroconversión (incremento significativo de títulos) es indicativa de infección reciente, compatible con un rol etiológico en el aborto.
Serología fetal. La utilidad de esta técnica depende de la edad gestacional, ya que la producción de anticuerpos fetales sólo es detectable a partir de la segunda mitad de la gestación.
La detección de anticuerpos en líquidos fetales (especialmente líquido pleural) indica infección transplacentaria, sin embargo, para confirmar que estos parásitos causaron el aborto, es necesario asociarla a la lesión histopatológica característica.
Una serología fetal negativa no excluye infección (dado que depende del desarrollo del sistema inmune o edad fetal).
Serología precalostral en cabritos nacidos .
Los cabritos infectados por vía transplacentaria presentan anticuerpos detectables antes de la ingestión del calostro.
Los cabritos nacidos de madres seropositivas, pero no infectados no presentan anticuerpos precalostrales, lo que permite diferenciar inmunidad pasiva de infección congénita.
Lesiones clínicas y hallazgos patológicos sugerentes . En los brotes de toxoplasmosis y neosporosis caprina, el examen clínico y anatomopatológico proporciona información preliminar valiosa. Entre ellas se describen, reabsorciones embrionarias en hembras previamente diagnosticadas como gestantes por ultrasonografía, fetos momificados y placentas maceradas o de aspecto achocolatado, lesiones placentarias típicas: Necrosis multifocal en cotiledones con o sin calcificaciones (puntillado blanquecino). Ausencia de exudado purulento o fibrinoso y de engrosamiento coriónico intercotiledonario (lesiones características de otras enfermedades como Chlamydia abortus o Coxiella burnetii), sugieren que podría deberse a toxoplasmosis o neosporosis.
Sin embargo, las lesiones macroscópicas de N. caninum son indistinguibles de las de T. gondii, lo que subraya la necesidad de confirmar mediante técnicas moleculares específicas (Ortega-Mora et al. 2007).
Como mencionamos anteriormente los abortos pueden presentarse en todos los en todos los estadios gestacionales, incluyendo fases tempranas (Figura 4).

Seroprevalencia de T. gondii y N. caninum. Estudios previos han evidenciado la presencia de anticuerpos contra T. gondii y N. caninum en cabras. A nivel global, la seroprevalencia de T. gondii en caprinos se estima en 27,5%, con los valores más altos en América Central (62,2%) y Sudamérica (29,7%) (Dubey et al. 2020, Rodrigues et al. 2022). En Argentina, las seroprevalencias oscilan entre 16,2% y 63%, dependiendo de la región y del sistema productivo (Venturini et al. 1993, Martínez et al. 2013, Gos et al. 2017, Dodero et al. 2019, Basset et al. 2024). Los principales factores de riesgo asociados incluyen la presencia de felinos domésticos en los establecimientos, la edad de los animales, estado fisiológico y el tipo de sistema de producción (Iovu et al. 2012, Tzanidakis et al. 2012, Gos et al. 2017, Dubey et al. 2020, Rodrigues et al. 2022, Steffen et al. 2024). En Argentina, se identificó que el tipo de sistema y la composición racial predisponen a una mayor seropositividad (Gos et al. 2017, Steffen et al. 2021, 2024). En estudios realizados en la provincia de Buenos Aires, se detectaron anticuerpos contra T. gondii en el 63% de los caprinos de sistemas intensivos, a diferencia de los sistemas extensivos donde se encontró una seroprevalencia del 32,7% (Gos et al. 2017), siendo también menor en las cabras predominantemente Criollas y mayor en las cabras predominantemente Saanen (Steffen et al. 2021). Las cabras con altos títulos (≥1600) de anticuerpos anti-T. gondii no se asociaron con la ocurrencia de abortos, pero sí con las muertes perinatales en establecimientos con alta prevalencia y pérdidas reproductivas (Steffen et al. 2021).
Por su parte, N. caninum presenta una distribución mundial en caprinos con una seroprevalencia media del 5,99%, variando entre 0,47% y 26,65%, con una mayor proporción de animales seropositivos en América (Utuk y Eski 2019, Rodrigues et al. 2020). En Argentina, se han reportado prevalencias que van del 4,2% al 64%, con estudios realizados en provincias como La Rioja, Córdoba, Buenos Aires, San Luis y Salta (Moore et al. 2007, Gos et al. 2014, 2017, Suarez et al. 2023, Basset et al. 2024). La seropositividad ha sido relacionada con la presencia de perros en los establecimientos, los fallos reproductivos y el tipo de manejo productivo, siendo más frecuente en sistemas semi-intensivos con suplementación (Gos et al. 2017, Suárez et al. 2023).
Ambas infecciones tienen un impacto significativo en la producción caprina, especialmente por su relación con problemas reproductivos como el aborto. Sin embargo, aún existen vacíos de conocimiento sobre su rol en los sistemas de producción locales y su impacto en la sanidad animal y la seguridad alimentaria. Por ello, es fundamental continuar con estudios epidemiológicos y monitoreos regulares de los animales infectados que permitan una mejor comprensión de su dinámica de transmisión y la implementación de estrategias de control eficaces.
A nivel mundial, se estima una población de aproximadamente 1.100 millones de cabras domésticas, con un incremento del 21,1% en la última década (FAOSTAT 2023). Esta producción se concentra principalmente en países en desarrollo, donde representa una alternativa viable ante condiciones ambientales desfavorables para otras formas de ganadería. En este contexto, la producción caprina suele estar vinculada a sistemas de subsistencia o producción familiar, orientados al autoconsumo y la venta local. Asia y África concentran el 93,1% del stock mundial, mientras que América representa solo el 4,3%, con Brasil, México y Argentina como principales productores. Argentina ocupa la posición 34 a nivel mundial en términos de relevancia productiva (Martínez y Suárez 2018). En los últimos 10 años, mientras que las poblaciones de bovinos y ovinos disminuyeron un 7% y 10,5% respectivamente, la población caprina aumentó un 7% (FAOSTAT 2023). En el país, el 59% del stock caprino se concentra en las provincias de Neuquén, Mendoza, Chaco y Santiago del Estero, principalmente en establecimientos con menos de 500 animales (Steffen et al. 2021). Aunque presentes en todo el territorio, en regiones como el Noroeste Argentino, la producción caprina reviste particular importancia dentro de la agricultura familiar y campesina, enfocada en la cría de cabras criollas para producción de carne (cabritos), leche, fibra y cuero. En la Patagonia, en cambio, predomina la cabra Angora, orientada a la obtención de fibra mohair, concentrando el 25,2% del stock nacional (Steffen et al. 2021). No obstante, diversos factores de manejo limitan la eficiencia productiva, entre ellos las infecciones parasitarias, que afectan negativamente la productividad, reproducción por abortos o muerte perinatal y el bienestar animal (Martínez y Suárez 2018, Steffen et al. 2021).
Impacto de T. gondii y N. caninum en la producción caprina. Hasta el momento, la mayoría de los estudios sobre T. gondii y N. caninum en caprinos se han centrado en determinar la seroprevalencia y las pérdidas económicas vinculadas a las pérdidas reproductivas, sin abordar su impacto en la sanidad animal y la seguridad alimentaria como en la producción de leche y carne. En cuanto a T. gondii, aunque los animales infectados raramente presentan lesiones macroscópicas en mataderos, algunos estudios han detectado una alta carga de quistes tisulares viables en cabras sacrificadas para consumo humano, lo que refuerza el papel de la carne caprina en la transmisión de la toxoplasmosis (Zdolec y Kiš 2021, Batista et al. 2022). Se ha determinado que incluso pequeñas cantidades de carne cruda o poco cocida pueden ser suficientes para la infección en humanos y animales carnívoros (Rani et al. 2020). La mayoría de los estudios concuerdan que las explotaciones lecheras con manejos intensivos registran seroprevalencias significativamente mayores en comparación con explotaciones con un sistema de producción extensivo para el ganado caprino (Gos et al. 2017, Dubey et al. 2020, Dubey 2022, Rodrigues et al. 2022). Además, la leche de cabra representa otra fuente de infección, registrándose una elevada prevalencia de anticuerpos anti-T. gondii (70%) y ADN del parásito (65%) en muestras de leche, incluso se ha registrado en queso, lo que subraya la necesidad de realizar vigilancia epidemiológica en establecimientos lecheros, particularmente en aquellos que venden o utilizan leche de cabra no pasteurizada (Dubey et al. 2014, Sroka et al. 2017). Por otro lado, los pocos estudios sobre N. caninum en producción lechera se han realizado en bovinos, evidenciando impactos económicos significativos debido a abortos, aumento del período interparto, aumento de la tasa de refugo y, posiblemente, la reducción de la producción de leche, aunque su magnitud sigue en debate (González-Warleta et al. 2011, Reichel et al. 2013, Demir et al. 2020). Incluso en el ganado bovino de carne también se ha reportado una disminución de la ganancia diaria de peso (Barling et al. 2000, Moré et al. 2010). En Argentina, se han estimado pérdidas de hasta US$87,4 millones anuales debido a la neosporosis en bovinos (Reichel et al. 2013), pero existen pocos datos sobre su impacto en los caprinos. Dada la alta prevalencia de estos protozoos en cabras y su potencial efecto en la producción, es crucial realizar estudios poblacionales que evalúen su influencia en la rentabilidad y seguridad alimentaria del sector caprino.
En este sentido, un estudio reciente realizado en Buenos Aires, Argentina tuvo como propósito estimar la seroprevalencia de N. caninum, Sarcocystis spp. y T. gondii en cabras lecheras de raza Saanen, y su posible relación con la producción de leche. Se evaluaron 336 cabras en producción de dos establecimientos comerciales semi-intensivos mediante IFI, observándose una seroprevalencia global de 81,8 % (275/336) para N. caninum, 85,1 % (286/336) para Sarcocystis spp. y 66,7 % (224/336) para T. gondii. El análisis de la información productiva evidenció una asociación débil entre la seropositividad y la producción láctea caprina. No obstante, se observó que las cabras con títulos serológicos elevados frente a N. caninum presentaron una menor producción respecto de aquellas con títulos bajos. Estos hallazgos sugieren que, a pesar de la elevada frecuencia de las infecciones estudiadas, su impacto global sobre la producción lechera resulta limitado, por lo tanto, incitan a realizar investigaciones adicionales en poblaciones con menor prevalencia, permitiendo evaluar con mayor precisión la magnitud de posibles efectos subclínicos y favorecer el desarrollo de estrategias sanitarias orientadas a optimizar la productividad en sistemas caprinos lecheros (Steffen et al. 2025).
Implicancia en “Una Salud”. La toxoplasmosis constituye una zoonosis de alta relevancia sanitaria a nivel mundial y afecta a un tercio de la población mundial total (Gazzonis et al. 2019, Dubey et al. 2020). Es una preocupación importante para las personas con sistemas inmunitarios debilitados y mujeres embarazadas (Dubey 2022). Entre las principales vías de transmisión al ser humano se destacan la ingestión de ooquistes presentes en el agua de bebida o las verduras, el consumo de carne cruda o insuficientemente cocida, así como la ingesta de productos lácteos no pasteurizados derivados de animales infectados. También reviste importancia la transmisión transplacentaria, de la madre al feto dado que T. gondii puede atravesar la barrera maternofetal, como también otras barreras hematoencefálicas y hematoocular, provocando encefalitis, aborto espontáneo, parto prematuro o importantes secuelas neurológicas y oculares (Dubey 2022, Khan et al. 2023). Por lo tanto, para un abordaje integral se requiere un enfoque interdisciplinario como el propuesto por la iniciativa “Una Salud”, entre instituciones, productores y promotores de salud situados.
En países como Argentina, donde los productos caprinos poseen un fuerte arraigo cultural y representan una fuente nutricional y económica clave para pequeños y medianos productores, es fundamental considerar el riesgo de transmisión de T. gondii a través de la carne y la leche o sus derivados. La carne caprina reviste importancia como fuente de proteína y como potencial responsable en la transmisión de T. gondii a los humanos.
El consumo de carne cruda o poco cocida es uno de los principales factores de riesgo y puede ser responsable del 50 % o más de los casos de toxoplasmosis humana (Hamilton et al. 2015, Belluco et al. 2016). La identificación del parásito en la carne es compleja y desafiante, ya que los quistes tisulares son microscópicos y no se detectan durante inspecciones rutinarias (Yousefvand et al. 2021). Esto subraya la importancia de intensificar la búsqueda de este parásito e implementarlo como una prioridad en las inspecciones cárnicas en establecimientos y frigoríficos, dado que, la ingestión de tan solo 5-10 gramos de carne con quistes tisulares puede transmitir T. gondii (Rani et al. 2020). Aunque la serología en caprinos es valiosa para el monitoreo poblacional, la detección directa del parásito en tejidos es crucial para evaluar el riesgo de transmisión alimentaria, especialmente donde es una práctica cultural habitual el consumo de carne cruda o poco cocida (Gazzonis et al. 2020). La prevalencia de T. gondii en cabras es variable a nivel mundial, con detecciones en diversos tejidos musculares y órganos mediante PCR y nPCR (Belluco et al. 2016). Si bien la nPCR ha mostrado variabilidad en la sensibilidad, la elección de tejidos como el diafragma y el músculo cardíaco ha resultado más efectiva debido a la distribución preferencial de los quistes (Gazzonis et al. 2020). La tipificación genotípica del parásito es fundamental, ya que existen diferentes genotipos específicos (Gazzonis et al. 2020).
La leche cruda y los quesos frescos de cabras elaborados artesanalmente han sido señalados como posibles formas de infección, tanto para humanos como para otros animales (Dubey et al. 2014, Gazzonis et al. 2019, Dubey 2022, Khan et al. 2023). La excreción de T. gondii en leche de cabra ha sido documentada tanto en contextos de infección natural como experimental (Dubey et al. 2014, Saad et al. 2018, Gazzonis et al. 2019, Dubey 2022). En animales infectados naturalmente, se ha detectado ADN del parásito en muestras de leche (Saad et al. 2018, Gazzonis et al. 2019), mientras que en estudios experimentales se ha observado una excreción intermitente del mismo tras la inoculación oral con ooquistes (Dubey 2022). La viabilidad del parásito en estas secreciones ha sido confirmada mediante bioensayos en modelos animales, como ratones y gatos (Dehkordi et al. 2013, Dubey 2022). Asimismo, se ha demostrado que T. gondii puede sobrevivir en queso fresco producido mediante tratamiento enzimático en frío, lo cual subraya el riesgo asociado al consumo de productos lácteos (queso y quesillo) sin pasteurizar (Dubey et al. 2014, Dubey 2022, Khan et al. 2023). Sin embargo, a pesar de la evidencia experimental y molecular, la relevancia epidemiológica de esta vía de transmisión continúa siendo motivo de controversia, y su impacto real en la diseminación de la toxoplasmosis aún no ha sido claramente establecido (Dubey et al. 2014, Dubey 2022).
Desde una perspectiva de “Una Salud”, se recomienda la correcta manipulación y cocción de la carne y leche caprina, dado que T. gondii puede permanecer viable en los tejidos musculares o en la leche. A diferencia de la toxoplasmosis, la neosporosis no representa un riesgo zoonótico, pero puede causar abortos recurrentes en el ganado caprino. Es importante el lavado adecuado de manos tras la manipulación de carne cruda (faena) y la higienización de frutas y verduras con agua segura para contribuir a la reducción del riesgo de infección (Durlach et al. 2021, Dubey 2022).
Las formas infectantes de T. gondii mueren por la cocción y el contacto con agua hirviendo (100 °C), por lo tanto, se debe lavar los utensilios de cocina (tablas de cortar, cuchillos y otros elementos) utilizando agua hirviendo luego del contacto con carne cruda. En la preparación de los alimentos, utilizar una tabla y utensilios diferentes para cortar las carnes y los vegetales crudos y mantener los alimentos separados en la heladera. Los quistes tisulares en la carne se eliminan o inactivan al cocinarse hasta los 66 °C por 10 minutos antes de su consumo, y se debe evitar probarla cruda mientras se cocina o condimenta. Sin embargo, los tiempos de cocción varían según el grosor y el tipo de corte de carne. La cocción en microondas no es segura para eliminar T. gondii. Otra forma de eliminarlos es por congelación, se ha observado que la mayoría de los quistes presentes en la carne se destruyen a −12 °C de temperatura interna. Congelarla durante la noche en un congelador doméstico es eficaz para eliminar la mayoría de los quistes tisulares (Lindsay y Dubey 2020, Durlach et al. 2021, Dubey 2022).
El Consenso Argentino de Toxoplasmosis Congénita (Durlach et al. 2021), recomienda que las mujeres embarazadas eviten el contacto con la arena de los gatos y la tierra. Asimismo, se establece la necesidad de asegurar la cocción de la carne consumida y a las verduras cuando no es posible conocer si fueron correctamente lavadas. No consumir embutidos. Se recomienda alimentar a los gatos domésticos con alimentos balanceados o secos, enlatados o cocinados. La caja de arena o litera del gato debe vaciarse diariamente ya que los ooquistes se vuelven infecciosos entre 1 a 5 días luego de la eliminación en las heces y lavarse con agua a alta temperatura. En la medida que se pueda dicha tarea no debería realizarla las mujeres embarazadas, o en su defecto tomando los recaudos necesarios como el uso de guantes de látex. También debería usarse guantes mientras se realizan trabajos de jardinería.
Recomendaciones para la prevención y control de toxoplasmosis y neosporosis caprina. La prevención, detección temprana y control adecuado de la toxoplasmosis y la neosporosis son claves para minimizar el impacto productivo y reproductivo en los hatos caprinos, garantizando la salud del hato y la rentabilidad de la producción, dado que hasta el momento no existe tratamiento ni vacuna disponible. Para lograrlo se han sugerido diferentes medidas; como la aplicación de protocolos de bioseguridad, medidas higiénicas y prácticas de gestión en los establecimientos, y medidas sobre los HD (félidos y cánidos) para evitar la continuidad del ciclo biológico de los parásitos, y también sobre los caprinos. Sin embargo, estas medidas se deben utilizar combinadas para obtener una estrategia óptima de prevención y control como así también deberían adecuarse a la situación particular en cada caso, como por ejemplo el tipo de explotación, posibilidad de controlar fuentes de infección horizontal o posnatal, prevalencia de la enfermedad y el costo-beneficio de implementar medidas sanitarias de prevención y control. Debido a la endemicidad de estas enfermedades en la mayoría de los establecimientos, es muy común encontrar cabras seropositivas sin que ello esté necesariamente vinculado a la presentación de abortos o fallas reproductiva, por ello, es fundamental registrar los eventos reproductivos para identificar problemas de manera temprana.
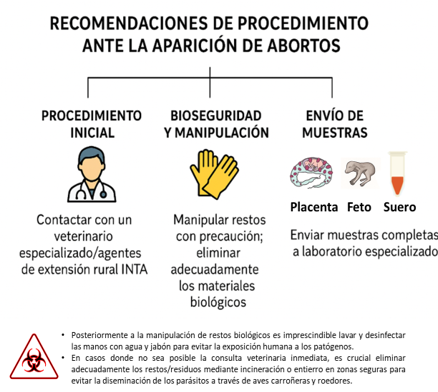
En el caso de la toxoplasmosis, T. gondii utiliza a los felinos como HD, mientras que, en la neosporosis, N. caninum se transmite a través de perros. Para minimizar los riesgos, es fundamental restringir el acceso de gatos y perros a los corrales, especialmente a los que albergan cabras preñadas como así también el acceso a las pasturas, silos y galpones donde se guarda el alimento y al suministro de agua, dado que estos podrían eliminar ooquistes en sus heces contaminando el medio ambiente. También es importante evitar que los perros y gatos consuman placentas, fetos abortados o carne cruda de cabras infectadas y en lo posible controlar el número de gatos o perros en los establecimientos y evitar el incremento de animales jóvenes mediante la castración, ya que se ha visto que existe mayor riesgo de eliminación de ooquistes en ellos. La correcta disposición de restos biológicos (placentas o materiales fetales o abortos y animales muertos) y el mantenimiento de una higiene estricta en las instalaciones/corrales o camas son esenciales para reducir la propagación de ambos parásitos (Figura 5).
Asimismo, se recomienda identificar a las cabras portadoras/seropositivas mediante serología y registrar los eventos reproductivos de estas. Evitar introducir cabras infectadas al hato/rebaño (realizar serología a todo animal nuevo que ingrese) y que la reposición sea con cabrillas/cabritas seronegativas. También dentro de las prácticas reproductivas utilizadas para el control, se recomiendan utilizar hembras receptoras y machos dadores seronegativos en los establecimientos que realicen transferencia embrionaria o inseminación artificial. Por último, establecer el control de roedores.
En este contexto, la implementación de estrategias de prevención y control orientadas a la educación sanitaria de productores, trabajadores rurales y profesionales de la salud constituye un pilar estratégico. La capacitación en buenas prácticas de manejo, higiene en instalaciones, eliminación adecuada de restos biológicos (placentas, fetos abortados, animales muertos) y control responsable de perros y gatos contribuye a interrumpir los ciclos de transmisión de estas parasitosis. La educación sanitaria, además, promueve el bienestar animal al concientizar sobre la importancia de mantener a los caprinos en buen estado de salud y reducir los factores predisponentes a la inmunosupresión. Asimismo, fomentar hábitos seguros en la manipulación y consumo de productos caprinos, como la correcta cocción de la carne y la pasteurización de la leche, resulta esencial para disminuir el riesgo zoonótico de la toxoplasmosis bajo una perspectiva integral de “Una Salud”.
La toxoplasmosis y la neosporosis representan causas relevantes de pérdidas reproductivas en caprinos, con implicancias directas en la productividad y en el caso de T. gondii, en salud pública. La información disponible evidencia la necesidad de aplicar un enfoque integral que combine vigilancia epidemiológica, medidas de bioseguridad, diagnóstico diferencial oportuno y estrategias de manejo orientadas a mantener a los animales en buen estado sanitario y de bienestar, a fin de reducir la incidencia y el impacto de estas parasitosis. Es fundamental para establecer la etiología de los abortos y diseñar estrategias de control eficaces un diagnóstico certero, para lo cual se combinen herramientas serológicas, moleculares e histopatológicas. Si bien se han desarrollado avances en herramientas diagnósticas y en propuestas vacunales, hasta el momento no existe en el mercado vacunas comerciales disponibles, por lo que resulta necesario continuar investigando estas parasitosis y su impacto productivo y epidemiológico en caprinos, a fin de optimizar las prácticas de prevención y control en el marco del concepto “Una Salud”. Bajo este marco, la articulación entre productores, veterinarios e instituciones sanitarias y de educación es esencial para mitigar los riesgos zoonóticos, promover el bienestar y la salud de los animales y mejorar la productividad en regiones donde la producción caprina constituye un recurso estratégico para la seguridad alimentaria y el desarrollo local.
Contribución de los autores. SKD: Conceptualización, Metodología, Investigación, Análisis formal, Redacción del borrador original, Redacción, revisión y edición. GML: Investigación, Metodología, Redacción, revisión y edición. BCM: Investigación, Metodología, Redacción del borrador original. PL: Redacción, revisión y edición, Supervisión. VMC: Supervisión, Obtención de financiación. MG: Investigación, Redacción, revisión y edición, Supervisión, Obtención de financiación.
Declaración de conflictos de intereses. Los autores declaran no tener conflictos de intereses financieros ni relaciones personales conocidas que pudieran haber influido en el trabajo presentado en este artículo.