Revista Veterinaria. 2026; 37(1)
https://doi.org/10.30972/vet.3719220
Revisión Bibliográfica




1Especialización en Salud Pública Veterinaria (ESPV), Fundación Universitaria Agraria de Colombia (Uniagraria), Bogotá, Colombia.
2Universidad Nacional de Colombia, Departamento de Ciencia Animal, sede Palmira.
3Asociación Nacional de Médicos Veterinarios de Colombia (AMEVEC), Bogotá, Colombia.
4Comité de Medicina Tropical, Zoonosis y Medicina del Viajero de la Asociación Colombiana de Infectología (ACIN), Bogotá, Colombia.
5Grupo de Investigación de Producción y Salud en Medicina Veterinaria y Zootecnia (PROSAVEZ), Facultad de Medicina Veterinaria y Zootecnia, Fundación Universitaria San Martín (FUSM), Bogotá, Colombia.
Recibido: 30 octubre 2025 / Aceptado: 01 marzo 2026
Resumen
Las zoonosis como la brucelosis y leptospirosis son enfermedades que se transmiten y comparten de forma natural entre animales vertebrados y seres humanos siendo de distribución mundial. De igual manera, actualmente no existe una ruta clara para el abordaje integral de la leptospirosis y brucelosis en el perro. El objetivo general de este trabajo fue describir el impacto en salud pública de Brucelosis y Leptospirosis. Se realizó una revisión sistemática de literatura, donde se van a seleccionar artículos científicos originales publicados en revistas científicas con un rango de búsqueda de 2018 a 2023. Se consultaron las bases de datos: Scielo, PubMed, Google Scholar y la Biblioteca Virtual en Salud (BVS). Adicionalmente se realizó la búsqueda de información de instituciones gubernamentales y organizaciones no gubernamentales involucradas en la vigilancia de brucelosis y leptospirosis. Para Leptospira, los roedores son el principal reservorio, y un posible factor de riesgo es el consumo de agua no tratada. Para Brucelosis, los perros que deambulan por la calle representan un factor de riesgo, además de ser reservorios y fuente de contaminación. El período de incubación de ambas patologías es muy variable, de días hasta varios meses. En ambos casos los animales pueden ser portadores asintomáticos, y aun estando en tratamiento, excretar el agente al medio ambiente. Se describió el impacto en salud pública de brucelosis y leptospirosis y el papel que desempeña el perro en ambas enfermedades.
Palabras clave: leptospirosis canina, brucelosis canina, costo de la enfermedad, carga de la enfermedad, factores de riesgo.
Abstract. Zoonoses such as brucellosis and leptospirosis are diseases naturally transmitted and shared between vertebrate animals and humans, with worldwide distribution. Similarly, there is currently no clear pathway for the comprehensive management of leptospirosis and brucellosis in dogs. The general objective of this study was to describe the public health impact of brucellosis and leptospirosis. A systematic literature review was conducted, selecting original scientific articles published in peer-reviewed journals from 2018 to 2023. The databases consulted included Scielo, PubMed, Google Scholar, and the Virtual Health Library (BVS). Additionally, information was gathered from governmental and non-governmental institutions involved in the surveillance of brucellosis and leptospirosis. For leptospirosis, rodents are the main reservoir, with untreated water being the most likely source of contamination. For brucellosis, stray dogs represent a risk factor, as they function as reservoirs and sources of infection. The incubation period of both diseases is highly variable, ranging from days to several months. In both cases, animals may remain asymptomatic carriers and, even under treatment, can excrete the pathogen into the environment. The public health impact of brucellosis and leptospirosis and the role of dogs in both diseases were described.
Key words: canine leptospirosis, canine brucellosis, cost of illness, disease burden, risk factors.
Las zoonosis son enfermedades que se transmiten y comparten de forma natural entre animales vertebrados y seres humanos, que son de distribución mundial. Los datos evidencian en Estados Unidos que cada año cerca de cuatro millones de personas presentan una de estas enfermedades, lo que ocasiona un grave problema de salud pública y un alto costo en salud para los sistemas sanitarios (Estepa et al. 2022), sin embargo, muchas de estas enfermedades no se diagnostican, no se informan a nivel nacional y se pueden transmitir a partir de fuentes distintas a los animales de compañía (el perro). Teniendo en cuenta estas limitaciones, la revisión de los datos nacionales de vigilancia de enfermedades y la literatura publicada sugiere un posible subdiagnóstico o subregistro lo cual hace difícil estimar los costos de atención en salud. Estos costos incluyen los de atención médica directa durante la enfermedad aguda, atención de apoyo o soporte (enfermedad crónica) y prevención de la enfermedad (por ejemplo, la rabia), pero no se ha estimado la pérdida de vida o calidad de vida (Stehr-Green y Schantz 1987).
Brucella spp. es una bacteria que puede afectar tanto a animales como a humanos, la trasmisión a animales suele darse por medio de la monta, aerosoles o por contacto directo de mucosas o piel lesionada con material contaminado con el agente patógeno, los fluidos vaginales luego de un aborto y el semen de animales infectados son una de las fuentes más comunes de contagio para otros animales (caninos, por ejemplo) y para las personas, dada la elevada concentración de bacterias presentes en este tipo de secreciones. Sin embargo, para el caso de B. canis esta puede persistir en secreciones vaginales no asociadas con el periodo de estro y en órganos diferentes a los reproductivos, el patógeno puede diseminarse de manera intermitente y en bajas concentraciones en orina, saliva y secreciones nasales (Laverde et al. 2021).
Un estudio realizado por Carreño et al. (2017), sugiere que la leptospirosis es una zoonosis reemergente endémica distribuida a nivel mundial. La presencia de esta enfermedad implica problemas de tipo epidemiológico, económico y social. En Colombia la enfermedad es subdiagnosticada probablemente debido a la falta de conocimiento, a la ausencia de métodos de diagnóstico o al acceso a las pruebas confirmatorias. Las prevalencias reportadas en ese estudio evidencian que van del 6% al 35% en humanos, 41% y 60,9% en bovinos, 10,3% en porcinos, 12% y 47,14% en caninos, 23,07% para primates no humanos y entre el 25% y el 82,7 % en roedores (las más elevadas), siendo Icterohaemorrhagiae, Grippotyphosa y Canicola los serovares de mayor circulación en el país (Carreño et al. 2017).
Perdomo-Medina et al. (2021) realizaron un trabajo acerca de la percepción de los médicos, enfermeros y médicos veterinarios sobre las enfermedades zoonóticas encontrando que existe desconocimiento de la prevención de estas por parte de los implicados, y falta de educación médica para afrontar las enfermedades zoonóticas, debilidades o barreras en el diálogo interprofesional entre las 3 profesiones, ausencia de práctica colaborativa entre los profesionales de la salud y los médicos veterinarios, desconocimiento de las medidas y adopción de estas para la prevención de las zoonosis, donde se demuestran las fallas y vacíos en el sistema vigilancia de las enfermedades, y los partícipes reportan un evidente subregistro de los casos.
En Colombia se realiza la vigilancia del evento mediante la notificación obligatoria de las enfermedades zoonóticas según el decreto 780 de 2016 (Ministerio de Salud y Protección Social 2016). El centro para el control y prevención de enfermedades (CDC) priorizó a la brucelosis y leptospirosis dentro de los seis primeros lugares, en unas mesas de trabajo con diversas instituciones del país (CDC 2023). Para el caso de brucelosis las prevalencias reportadas oscilan en humanos hacia el 3,8%, en animales entre 2,8 y 6,1% (Avila-Granados et al. 2019). En otro estudio se reporta una prevalencia en humanos entre 0,4 y 10,4%) (López Guarnizo 2014). Para Leptospira, las prevalencias en el país oscilan entre el 6 y el 25% (Carreño et al. 2017) El estudio de Calderón-Sierra et al. (2019) para leptospirosis, desde el año 2012 hasta el 2016 evidencia una notificación al SIVIGILA un total de 10.435 casos; el año en el cual se informó el mayor número de casos fue 2014 con 2.305 casos (22,08%, n = 2305); seguido de 2016 con 2.197 casos (21,1%); 2015 con un total de 2007 casos (19,23%); 2012 con 1.986 casos (19%) y finalmente 2013 con 1.940 casos (18,6%). Estos casos se dividen acorde con la clasificación que tiene el país: casos notificados, casos sospechosos, confirmados por laboratorio y confirmados por nexo epidemiológico.
En animales de compañía los reportes se realizan mediante el Sistema de Vigilancia en Salud Pública (SIVIGILA), para el Distrito Capital de los 602 reportes realizados entre agosto del 2014 y diciembre del 2021, el 44,4% (n = 267) corresponde a leptospirosis, seguido de brucelosis 35,2% (n = 212) (Estepa et al. 2022). Para el año 2023, por ejemplo, se registraron 299 en la estrategia de vigilancia centinela de B. canis en Bogotá, de los cuales 268 fueron muestreados según el algoritmo diagnóstico recomendado por la Secretaría de Salud de Bogotá en donde al realizar la primera prueba serológica (PRAP 2-Mercaptoetanol) permitió evidenciar una seroprevalencia inicial de 1,9% (5 animales) (Daza y Estepa 2024). Asimismo, para el caso de leptospirosis, en Bogotá en el año 2022, se realizó el registro de 86 reportes de diagnóstico de leptospirosis en caninos, donde las localidades que más reportaron fueron Antonio Nariño y Puente Aranda, lo cual sugiere la necesidad de fortalecer la capacidad del diagnóstico y la investigación en este tipo de eventos de interés en salud pública (Estepa et al. 2023). El objetivo general de esta revisión fue describir el impacto en salud pública de Brucelosis y Leptospirosis.
Se llevó a cabo una revisión sistemática de literatura siguiendo la metodología de Sakamoto-Trujillo et al. (2022) y Barrera Cepeda et al. (2023). Esta revisión se realizó a partir de artículos originales publicados en revistas científicas. Se consultaron las bases de datos: Scielo, PubMed, Google Scholar y la Biblioteca Virtual en Salud (BVS). Adicionalmente se realizó la búsqueda de información de instituciones gubernamentales y organizaciones no gubernamentales involucradas en la vigilancia de brucelosis y leptospirosis canina. En general una revisión de literatura se define como una estrategia de recopilación de evidencias acerca de una intervención o un tema específico. El propósito de una revisión es dar respuesta a una pregunta o problema de investigación, consolidar los hallazgos de la literatura existente en un período de tiempo, identificar vacíos en el conocimiento, aclarar o reforzar conceptos, informar acerca de los tipos de estudios o reunir la literatura existente de un tema. En general, una revisión sistemática se compone de cinco fases para el desarrollo, las cuales son: elaboración de la pregunta de investigación o definición del problema, establecimiento de los criterios de inclusión/exclusión, revisión y selección de estudios (literatura), extracción de los datos y análisis de los resultados (Fernández-Sánchez et al. 2020). Las palabras claves se definirán por medio de DeCS y MeSH: canine leptospirosis, leptospirosis/veterinary, canine brucelosis, brucelosis/veterinary, leptospirosis/economics, brucellosis/economics
Los artículos se consideraron elegibles si cumplían con los siguientes criterios de inclusión:
Artículos originales de revistas científicas, publicados a partir del año 2018 a 2023.
Idioma español e inglés.
Artículos con resultados donde se evidencie el impacto en salud pública de brucelosis y leptospirosis en caninos.
No se incluyeron otras revisiones de literatura, artículos sin relevancia o las palabras claves en el título, estudios en los que no evalúe o evidencie el impacto en salud pública de brucelosis y leptospirosis, documentos que traten temas en animales de producción, investigaciones con metodología que no reporten datos claros o inexactos, documentos anteriores al año 2018 y que no cumplieran los criterios de calidad científica.
Para la selección de los artículos científicos, se realizó una lectura crítica de los artículos con relevancia en títulos, resumen y palabras claves, a fin de seleccionar los estudios que cumplieron los criterios de inclusión, una vez seleccionados los documentos se registraron los datos en una tabla en Microsoft Excel®, con los siguientes encabezados, para el objetivo 1: reservorios, fuentes de contaminación-infección, período de incubación, período de transmisibilidad, posibilidad de tratamiento, medidas de bioseguridad en caso de manejar animales positivos, eutanasia humanitaria, costos en salud (Humana), discapacidad (en humanos), medidas de prevención y control, factores de riesgo. Para el objetivo 2: prueba tamiz, pruebas confirmatorias, signos y síntomas de animales sospechosos.
Los estudios incluidos en general fueron heterogéneos, en los métodos y resultados, y muchos reportaron diferentes tipos de variables, lo cual no permitió un análisis estadístico, por lo cual se realizó una síntesis narrativa y el reporte de porcentajes de frecuencia de presentación de algunas variables. Dada la naturaleza del estudio, no requiere aval del comité de bioética, sin embargo, contó con aval del comité de investigación de la Fundación Universitaria Agraria de Colombia (Uniagraria).
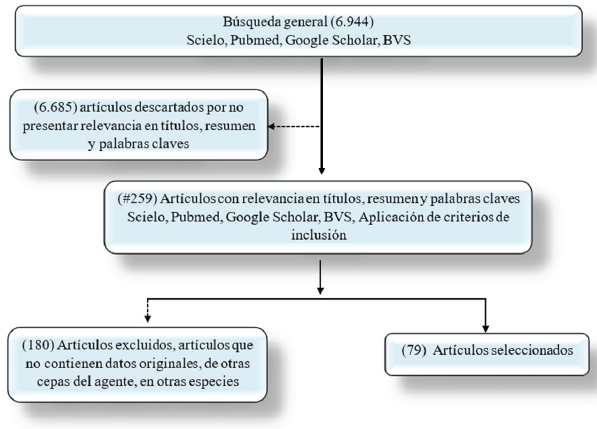
El proceso de búsqueda y selección de artículos se resume en el organigrama de búsqueda y selección de los artículos (Figura 1).
Variables asociadas a la enfermedad, costos en salud y discapacidad, medidas de prevención y control. De los 31 documentos consultados, el 48% menciona a los roedores como el principal reservorio, en segundo y tercer lugar los animales silvestres y de compañía 19,3% (Castrillón-Salazar et al. 2019, Felix et al. 2020, Molina et al. 2020, Bernardino et al. 2021, Berra et al. 2021, Kusumaratna et al. 2021, Taylor et al. 2021; Gong et al. 2022, Griebsch et al. 2022, Perez-Garcia et al. 2022, Stull et al. 2022, Belaz et al. 2023, Klosowski y Bohn 2023, Lu et al. 2023, Senthilkumar et al. 2023a, Sohn-Hausner et al. 2023, Sykes et al. 2023).
En cuanto a las fuentes de contaminación un factor de riesgo es el consumo de agua no tratada 24,4%, seguido por el suelo 15,5% y la fauna silvestre 9% (Castrillón-Salazar et al. 2019, Hernández-Ramírez et al. 2020, Murcia et al. 2020, Saeki y Tanaka 2021, Bernardino et al. 2021, Griebsch et al. 2022, Belaz et al. 2023, Garcia-Lopez et al. 2023, Klosowski y Bohn 2023, Lu et al. 2023, Sykes et al. 2023). El período de incubación de la enfermedad varía de 7 a 14 días en general en los animales, y en humanos puede llegar a ser de 3 a 30 días (Klosowski y Bohn 2023, Sykes et al. 2023). El período de transmisibilidad es variable, en animales puede ser de 2 semanas por la orina hasta 128 días, incluso varios años (Castrillón-Salazar et al. 2019, Iverson et al. 2021, Klosowski y Bohn 2023). En cuanto al posible tratamiento, según reporta la literatura en un 12% se aborda mediante la medicación con doxiciclina y penicilinas tales como: Amoxicilina, Amoxicilina/Ácido clavulánico, Ampicilina/Sulbactam 12%; Penicilina/Estreptomicina 3% y otros antibióticos 3%, sin embargo, se evidencia que el tratamiento incluso de 14 días con doxiciclina puede no eliminar la leptospiruria (infección en túbulos renales, lo cual genera un estado de portador). En un estudio se determinó que existe una variación con respecto a la posología de la doxiciclina por vía oral, con duraciones de tratamiento que oscilan entre 14 y 49 días. Sin embargo, no está establecida una dosificación estandarizada en casos de la enfermedad en caninos. Los perros que viven con otros perros infectados deben recibir igualmente doxiciclina cada 24 horas por lo menos durante 14 días (Iverson et al. 2021, Koscinczuk et al. 2021, Griebsch et al. 2022, Sykes et al. 2023).
De igual manera, se ha demostrado en perros que la eficacia del tratamiento es variable. La doxiciclina puede mejorar los parámetros clínicos y bioquímicos, pero no logra eliminar la excreción urinaria de leptospiras. Otros datos muestran que a dosis de 5 mg kg-1 durante diferentes periodos de tratamiento puede haber resolución clínica después de 21 días, mientras que en otros casos el paciente puede resultar siendo negativo por PCR en orina durante el tratamiento. Sin embargo, en algunos casos, la ineficacia del tratamiento puede ser tan severa que posiblemente sea necesario recurrir a la eutanasia debido a la ausencia de mejoría clínica y a las consideraciones asociadas al bienestar del paciente (Mendes et al. 2025).
Las evidencias acerca de las medidas de bioseguridad en caso de tener animales positivos sugieren que el manejo del perro durante y después del tratamiento tiene implicaciones importantes porque el perro puede contaminar el ambiente, a las personas y otros perros (desde los 4 hasta los 128 días desde que se diagnostica positivo y se instaura el tratamiento, lo que los convertiría en portadores asintomáticos), por cual se deben utilizar elementos de protección personal (EPP), tales como guantes, gafas protectoras; incluso el aislamiento de los animales y protocolos de limpieza y desinfección adecuados (Murcia et al. 2020, Iverson et al. 2021, Griebsch et al. 2022, Sykes et al. 2023).
Los costos que esta enfermedad acarrea en salud debido a la ausencia de la persona enferma en el cargo, lo cual puede llegar a los 4,4 millones de dólares anuales, con datos de pérdidas en un año de hasta 29 billones de dólares. Un tercio (1/3) de los casos requieren internación en unidad de cuidado intensivo (UCI). La productividad global anual perdida debido a la leptospirosis en un año puede ser hasta de 29,3 dólares por caso, lo cual afecta el producto interno bruto (PIB) del país. Incluso, se ha calculado que las pérdidas por enfermedad asociadas a la leptospirosis pueden llegar a 1.568 euros por paciente. El diagnóstico influye en este valor ya que se calcula que un paciente sin diagnóstico confirmado representa un costo de 10.000 dólares, y con diagnóstico (PCR y pruebas de seguimiento) 16.000 dólares (Sanhueza et al. 2020, Aslan y Lenhart 2020, Agampodi et al. 2023, Gómez-Martín et al. 2023, Parra et al. 2023). En cuanto a discapacidad hay estudios donde se evidencia, por ejemplo, que de 512 pacientes, 136 requirieron hospitalización prolongada. Alrededor de un tercio de los casos mortales tuvo hospitalización de más de 7 días. La tasa de mortalidad es del 6,4%. La discapacidad se puede medir por años de vida ajustados por discapacidad (AVAD), o por sus siglas en inglés (DALYs, disability-adjusted life years) que para el caso de leptospirosis es de 2,9.
Otros estudios evidencian que los DALYs son de 0,42 por cada 100.000 personas y 15,82 por cada 100.000 personas que trabajan en ocupaciones que tienen algún factor de riesgo (38 veces más alto). De hecho, la leptospirosis representa el 2% de las muertes prematuras cada año en Colombia. Además, la enfermedad es responsable de pérdidas económicas significativas, ya que se estima que un máximo de 648 años de trabajo perdidos (dato del año 2012), 46 años en promedio potenciales de vida perdidos (APVP), por sus siglas en inglés (YLPP, Years of Life Potentially Lost) atribuibles a muerte prematura, dado que se estima que alrededor de 2 años de vida potencialmente se pierden por cada 100.000 habitantes, para Colombia. Esto representa una pérdida económica considerable, asumiendo que esta última probablemente esté subestimada debido a la poca notificación y/o confirmación de los casos. En cuanto a los años de trabajo perdidos, por sus siglas en inglés (WYL, years of work lost), los cuales cuantifican el tiempo de trabajo perdido debido a la muerte antes o durante la edad productiva, en la enfermedad en promedio son de 27 años (Sanhueza et al. 2020, Al Hariri et al. 2022, Agampodi et al. 2023, Arboleda et al. 2023).
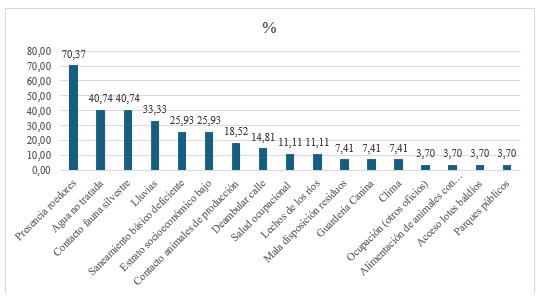
Por otra parte, con referencia a las medidas preventivas el 42% de los autores coinciden en que la vacunación de los animales es la más importante, 10% en realizar acciones de vigilancia epidemiológica y vigilancia activa y otras acciones como el control de roedores 9% y disminución en el contacto con las fuentes de infección (6%) (Castrillón-Salazar et al. 2019, Felix et al. 2020, Molina et al. 2020, Murcia et al. 2020, Sanhueza et al. 2020, Iverson et al. 2021, Kusumaratna et al. 2021, Saeki y Tanaka 2021, Taylor et al. 2021, Gong et al. 2022, Griebsch et al. 2022, Perez-Garcia et al. 2022, Sant’Anna et al. 2022, Stull et al. 2022, Engida et al. 2023, Garcia-Lopez et al. 2023, Klosowski y Bohn 2023, Lu et al. 2023, Senthilkumar et al. 2023a, Sohn-Hausner et al. 2023, Sykes et al. 2023). Los factores de riesgo para la enfermedad en caninos reportados se agruparon en 17 categorías, tales como: presencia de roedores como el más importante con 70,4%; contacto con fauna silvestre 40,7%, consumo de agua no tratada 40,7%; 33,3% precipitaciones, 25,9% saneamiento básico deficiente, entre otros (Figura 2) (Castrillón-Salazar et al. 2019, Smith et al. 2019, Felix et al. 2020, Hernández-Ramírez et al. 2020, Molina et al. 2020, Murcia et al. 2020, Sanhueza et al. 2020, Serrano-Martínez et al. 2020, Bernardino et al. 2021, Berra et al. 2021, Iverson et al. 2021, Koscinczuk et al. 2021, Kusumaratna et al. 2021, Saeki y Tanaka 2021, Taylor et al. 2021, Al Hariri et al. 2022, Gong et al. 2022, Griebsch et al. 2022, Perez-Garcia et al. 2022, Stull et al. 2022, Belaz et al. 2023, Garcia-Lopez et al. 2023, Klosowski y Bohn 2023, Lu et al. 2023, Parra et al. 2023, Senthilkumar et al. 2023b, Sohn-Hausner et al. 2023, Sykes et al. 2023).
Prueba tamiz, pruebas confirmatorias y signos y síntomas de animales sospechosos de leptospirosis. En cuanto al diagnóstico, se realizó una revisión de 36 documentos, en donde se evidencia que la prueba tamiz y además diagnóstica en un 83% es el MAT (prueba de aglutinación microscópica), seguida del PCR 5%, ELISA 5% y urocultivo 2%. Para la confirmación del diagnóstico se hace énfasis en el PCR 50%, seguido de la prueba ELISA 5%, Cultivo 5% y el MAT 2%. Los signos y síntomas se agruparon en 10 categorías, demostrando una mayor presentación clínica de síndrome renal 25%, síndrome hepático 25%, síndrome gastrointestinal 19%, Anorexia/Letargia 16%, hemorragias 11%, fiebre 11% y síndrome dermatológico, respiratorio, reproductivo y conjuntivitis con un 5% respectivamente (Miotto et al. 2018a, Barreto et al. 2019, Castrillón-Salazar et al. 2019, Smith et al. 2019, Aslan y Lenhart 2020, Desai et al. 2020, Felix et al. 2020, Hernández-Ramírez et al. 2020, Molina et al. 2020, Murcia et al. 2020, Serrano-Martínez et al. 2020, Bernardino et al. 2021, Berra et al. 2021, Iverson et al. 2021, Koscinczuk et al. 2021, Retnowati et al. 2021, Saeki y Tanaka 2021, Taylor et al. 2021, Gong et al. 2022, Griebsch et al. 2022, Martin et al. 2022, Perez-Garcia et al. 2022, Sant’Anna et al. 2022, Stull et al. 2022, Sulistiawati et al. 2022, Vojinovic et al. 2022, Arboleda et al. 2023, Garcia-Lopez et al. 2023, Gomes et al. 2023, Klosowski y Bohn 2023, Parra et al. 2023, Senthilkumar et al. 2023a, b, Sohn-Hausner et al. 2023, Sykes et al. 2023, Tintel et al. 2023).
El pronóstico de estos pacientes puede ser de reservado a malo, por lo que debe considerarse la eutanasia humanitaria cuando el paciente llega a condiciones que comprometan de forma grave la salud y afectan de forma grave el bienestar animal. La evidencia demuestra que la mortalidad por diversas complicaciones pulmonares, hepáticas o hemorrágicas, pueden avocar a tomar la decisión de eutanasia, al presentar signos tales como: dificultad respiratoria, insuficiencia renal aguda, cuadros hemorrágicos o finalmente por cuestiones económicas (imposibilidad de mantener el paciente en aislamiento-hospital, costo en tratamientos, medidas de prevención dispendiosas de implementar en los propietarios). Los datos demuestran que pueden existir hasta un 50% de pacientes que presentan estas complicaciones, aun vacunados, debido a que posiblemente la vacuna no contenía el serovar que infectó al animal (Miotto et al. 2018a, Iverson et al. 2021, Griebsch et al. 2022, Garcia-Lopez et al. 2023, Sykes et al. 2023). La literatura evidencia diversas opciones y opiniones con respecto al tratamiento debido a los tiempos prolongados de administración de antibióticos debido a que el agente puede permanecer en el perro por mucho tiempo y ser excretado por la orina por varios años (Castrillón-Salazar et al. 2019), por lo que el tratamiento con doxiciclina, por 14 días, como lo sugiere la literatura, puede no eliminar la leptospiruria (infección en túbulos renales, lo cual genera un estado de portador) (Sykes et al. 2023). De igual manera la evidencia demuestra que la mortalidad puede ocurrir por diversas complicaciones pulmonares, hepáticas o hemorrágicas que pueden desembocar en la decisión de la eutanasia terapéutica o con base en el bienestar animal (Ley 84 de 1989, para el caso de Colombia, capítulo V, art. 17), a la progresión de los signos clínicos, o complicaciones durante la hospitalización tales como vómito, anorexia, deshidratación, ictericia, trastornos hemorrágicos, diarrea, disuria, anuria, oliguria también, se presentan alteraciones en BUN, Creatinina, ALT, ALP, entre otros (Miotto et al. 2018b). Un estudio realizado en 20 pacientes demostró que 10 perros sobrevivieron tras recibir el tratamiento y en 10 casos ocurrió eutanasia o muerte. Trece perros no acudieron a los controles de seguimiento, por lo que no fue posible determinar información sobre el desenlace clínico (Miotto et al. 2018b). Un dato importante del estudio anterior es que la comparación entre perros con infección confirmada (18) y perros sintomáticos sin confirmación de infección leptospiral (15) no reveló diferencias significativas (p>0,05) en los niveles de BUN/CR, la actividad de ALT y ALP, el hematocrito, el recuento de leucocitos ni en el desenlace clínico. Otros datos de un estudio en 254 perros con leptospirosis aguda que la bilirrubina sérica a una concentración de al menos 10 μmol L-1 (0,6 mg dL-1) se asocia (odds ratio [OR], 16,4; p<0,001) con muerte o eutanasia. Así mismo el síndrome de hemorragia pulmonar leptospiral se ha asociado con una mortalidad de hasta el 70% aunque existen formas leves que pueden resolverse con tratamiento antimicrobiano (Schuller et al. 2015), la pregunta es cómo saber o detectar esas formas leves en la clínica diaria o cómo establecer un adecuado pronóstico, se torna en un complejo dilema que debe ser abordado por la medicina veterinaria incluyendo la evaluación de otras variables y factores desde el enfoque una salud. Otro estudio describió las características diagnósticas en 10 casos de leptospirosis canina aguda fatal con cambios renales y hepáticos mínimos al comienzo de la evaluación clínica. Sin embargo, la mayoría de los perros afectados tenía menos de 6 meses de edad y presentaba un perfil bioquímico compatible con disfunción hepatorrenal. Los signos clínicos incluyeron vómito, depresión, ictericia, deshidratación, diarrea y anorexia. Todos los perros murieron o fueron sometidos a eutanasia humanitaria entre 3 y 7 días después del inicio de la enfermedad clínica (Rissi y Brown 2014).
En relación con la seroprevalencia, se recopilaron 15 estudios evidenciando datos muy variables según el tiempo de estudio y el número de muestras. En Francia un estudio reporta 98% con 60 muestras, EE. UU. 61% con 88 muestras, Brasil 43% con 120 muestras, Colombia en el 2019 8% en 500 muestras, en 2020 57% con 92 muestras y en el 2022, 11% en 1.335 muestras. Para el año 2023, Colombia reporta 35% de 1824 muestras, con Bogotá y Antioquia como las zonas de mayor prevalencia (Castrillón-Salazar et al. 2019, Smith et al. 2019, Felix et al. 2020, Hernández-Ramírez et al. 2020, Murcia et al. 2020, Serrano-Martínez et al. 2020, Bernardino et al. 2021, Iverson et al. 2021, Taylor et al. 2021, Perez-Garcia et al. 2022, Stull et al. 2022, Vojinovic et al. 2022, Belaz et al. 2023, Garcia-Lopez et al. 2023, Senthilkumar et al. 2023a).
Variables asociadas a la enfermedad: reservorios, fuentes de contaminación-infección, medidas de prevención y control, medidas de prevención y control, factores de riesgo. En la búsqueda de evidencias para la brucelosis, en los 29 documentos consultados no hay datos suficientes para inferir cuales son los reservorios y fuentes de contaminación de B. canis, sin embargo, se sugiere al perro como reservorio y fuente de diseminación del agente, con énfasis en animales de calle o sin tenedor responsable (Palacios-Rodríguez et al. 2021, De Massis et al. 2022). El período de incubación es muy variable, con rango de 5 días hasta 4 años, aunque se existen datos desde 2 semanas hasta 3 meses, lo cual incluye que el período de transmisibilidad sea muy amplio, por ejemplo, en el semen de perros infectados, el agente puede permanecer hasta 6 a 8 semanas incluso con tratamiento (Cosford 2018, Long et al. 2022). Con respecto al tratamiento, todos los autores están de acuerdo con que la doxiciclina en unión con otro fármaco es el tratamiento de elección. El 20% sugiere adicionar al tratamiento aminoglucósidos, el 13% sugiere las quinolonas. Incluso en un caso se reporta el uso de doxiciclina y enrofloxacina oral y al mismo tiempo un esquema parenteral de 7 días de estreptomicina. Se hace necesario resaltar la realización de monitoreo de función renal y exámenes complementarios por la nefrotoxicidad de este esquema. El monitoreo debe ser durante varios meses. En el estudio de Seo et al. (2023) un animal positivo estuvo 15 meses con antibióticos y aun así mantenía niveles altos de anticuerpos, lo cual evidencia que probablemente la enfermedad no tenga cura, aunque se deben definir los criterios de negatividad. Todos los propietarios de pacientes positivos deben ser claramente informados acerca de los costos, la duración del tratamiento, la posibilidad de recaídas y del hecho de que aún con la terapia, el animal sigue eliminando el agente. Las evidencias anteriores sugieren hacer énfasis en el uso estricto de las medidas de bioseguridad tales como el uso de elementos de protección personal (EPP), lavado de manos, protocolos de limpieza y desinfección de rutina respetando la concentración y el tiempo de contacto de los desinfectantes (Cosford 2018, Egloff et al. 2018, Forbes et al. 2019, De Massis et al. 2022, Djokic et al. 2023, Guarino et al. 2023, Seo et al. 2023).
El manejo de los casos positivos debe ser discutido con el propietario. Según Boyden (2024), el tratamiento no se recomienda debido a la baja tasa de éxito, siendo la eutanasia el único medio definitivo para eliminar el patógeno. Si los propietarios optan por instaurar tratamiento, este debe incluir la esterilización del animal, el uso de antibióticos perioperatorios para reducir el riesgo de infección al personal veterinario, períodos prolongados de múltiples antibióticos, así como el monitoreo y manejo del estilo de vida (aislamiento y restricción). La eutanasia humanitaria (terapéutica) puede incluirse como una opción debido a que no se ha demostrado que al realizar el tratamiento el animal se vaya a curar, al contrario, existe un riesgo con otros animales, el hombre y la contaminación medio ambiental, ya que el animal positivo es posible fuente de infección.
La enfermedad no causa cuadros letales en los perros, pero por el “riesgo” de que el perro se convierta en fuente de infección podría considerarse la eutanasia la cual elimina el riesgo (Cosford 2018, De Massis et al. 2022). Santos et al. (2021) mencionan que la infección por B. canis, por ejemplo, provoca infertilidad en los perros y ha cobrado progresivamente mayor atención por parte de los criadores debido a las importantes pérdidas económicas asociadas, así como al riesgo para la salud pública. Desafortunadamente, no existe actualmente una vacuna comercial disponible para la prevención de la brucelosis canina. Por lo tanto, las medidas de control incluyen: (i) la realización de pruebas de tamizaje en perros y criaderos con sospecha de brucelosis, (ii) el tratamiento o la eutanasia de los animales infectados, y (iii) la eliminación de la bacteria del ambiente. Cuando existen diversos tipos de grupos o albergues de animales, los perros deben someterse a pruebas de tamizaje de forma anual o semestral; en caso de resultados positivos o inconclusos, los animales deben ser sometidos a cuarentena y a pruebas confirmatorias. Una vez confirmado el diagnóstico, debe considerarse la eutanasia. Siempre, los propietarios deben ser informados sobre los riesgos zoonóticos antes de optar por el tratamiento o la eutanasia. La orquiectomía o la ovariohisterectomía deben considerarse con el fin de eliminar el principal sitio de infección y disminuir el riesgo de transmisión. Además, los perros infectados deben recibir tratamiento, ya que el patógeno puede permanecer en los tejidos de animales castrados, a pesar de que el riesgo de transmisión sea menor. La elección del tratamiento en lugar de la eutanasia debe realizarse únicamente bajo la estricta supervisión de un médico veterinario; si se opta por el tratamiento, niños pequeños no deben tener contacto con el perro infectado. Los propietarios también deben ser conscientes de que, incluso bajo condiciones rigurosas, el tratamiento puede no lograr la curación, y podría requerir un segundo ciclo terapéutico, con los consecuentes efectos en la salud del animal. Los perros tratados deben someterse nuevamente a pruebas diagnósticas, y los resultados negativos mediante serología, PCR y aislamiento bacteriano pueden interpretarse como indicativos presuntivos de curación. Asimismo, deben implementarse medidas para el control de la contaminación ambiental en los hogares o lugares donde conviven otros animales.
Las medidas de prevención y control están dirigidas a disminuir la posibilidad de que los perros se infecten, por ejemplo, la esterilización quirúrgica de los animales de compañía, normas de bioseguridad e higiene, protocolos de limpieza y desinfección en guarderías, albergues, y demás establecimientos donde haya concentración de perros, cuarentena al ingreso de animales nuevo por mínimo 6 semanas y pruebas serológicas de ingreso. En caso de dar animales para adopción, estos deben tener pruebas serológicas antes de la entrega al tenedor responsable (Cosford 2018, Hensel et al. 2018, Galarce et al. 2020, De Massis et al. 2022, Djokic et al. 2023).
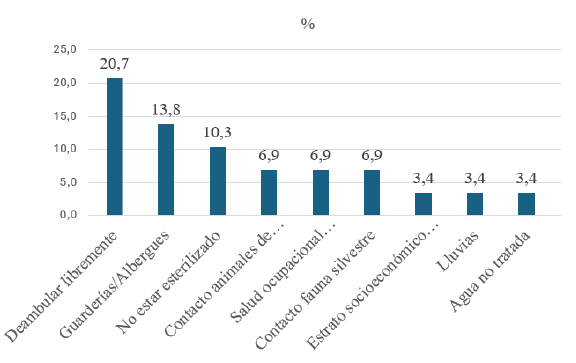
Se consolidaron 9 factores de riesgo siendo el de mayor importancia el hecho de que los animales deambulen en las calles o salga libremente a entornos callejeros o rurales 20,7%. En segundo lugar, los animales que permanecen o van de manera ocasional a guarderías o albergues 13,8% y en tercer lugar el hecho de no estar esterilizado 10,3%, ya que un animal infectado puede transmitir por el semen el agente en las primeras 8 semanas después de la infección hasta varios años después, de forma intermitente. En la Figura 3 se evidencian los factores de riesgo para B. canis en el perro (Colman et al. 2017, Hensel et al. 2018, Castrillón-Salazar et al. 2019, de Oliveira et al. 2019, Oosthuizen et al. 2019, Anyaoha et al. 2020, De Massis et al. 2022, Djokic et al. 2023, Ebani 2023).
Prueba tamiz, pruebas confirmatorias, signos y síntomas de animales sospechosos de B. canis. En cuanto al diagnóstico se realizó una revisión de 28 documentos, en donde llama la atención que la prueba tamiz predominante es la de 2β-Mercaptoetanol 32,1%, en segundo lugar la Prueba Rápida de Aglutinación (RSAT, por sus siglas en inglés) 21,4% seguido por la prueba de ELISA y la inmunodifusión en gel de agar (AGID, por sus siglas en inglés) con 17,8% respectivamente, con menos peso existen otras pruebas tales como inmunocromatografía, rosa de bengala, el PCR, Aglutinación en microplaca (MSAT, por sus siglas en inglés), fijación del complemento, Inmunofluorescencia (IFA), Antígeno de Brucella spp. buferado (BAPA), cultivo ya sea de orina o sangre y la electroforesis. Al contrario, en cuanto a las pruebas confirmatorias se consolida el PCR 34,7%, 2β-Mercaptoetanol 17,8%, la Prueba Rápida de Aglutinación (RSAT, por sus siglas en inglés) y la prueba de ELISA cada una con 10,7% (Cosford 2018, Hensel et al. 2018, Jung et al. 2018, Castrillón-Salazar et al. 2019, de Oliveira et al. 2019, Forbes et al. 2019, Oosthuizen et al. 2019, Whitten et al. 2019, Anyaoha et al. 2020, Galarce et al. 2020, Kamga et al. 2020, Mol et al. 2020, Sánchez-Jiménez et al. 2020, Weese et al. 2020, Borie et al. 2021, Laverde et al. 2021, Marami et al. 2021, Palacios-Rodríguez et al. 2021, Suárez-Esquivel et al. 2021, van Dijk et al. 2021, De Massis et al. 2022, Long et al. 2022, Djokic et al. 2023, Guarino et al. 2023, Hamdy et al. 2023, Perletta et al. 2023, Seo et al. 2023, He et al. 2024).
Los signos y síntomas más comunes reportados en 14 documentos están constituidos por los siguientes: discospondilitis-sacroilitis 64,2%, síndrome reproductivo en el macho (prostatitis, orquitis, epididimitis) 57,1%, aborto en las hembras infectadas 35,7%, y síndrome ocular (uveítis, corioretinitis) en un 21,4% (Cosford 2018, Egloff et al. 2018, Hensel et al. 2018, Forbes et al. 2019, Mol et al. 2020, Borie et al. 2021, Marami et al. 2021, van Dijk et al. 2021, De Massis et al. 2022, Long et al. 2022, Djokic et al. 2023, Ebani 2023, Guarino et al. 2023, Seo et al. 2023).
Como resultado del análisis de estudios de prevalencia en 13 estudios se demuestra que los datos son muy variables según el tipo de prueba y la selección de los pacientes (con o sin propietario, animales callejeros o con la presencia de otros factores de riesgo). Un estudio en Brasil evidencia una prevalencia del 45,5% en 167 muestras, en Nigeria 27,6% en 123 muestras y Canadá con 11,7% en 1.080 muestras. Del mismo modo para Colombia se reportan datos con prevalencias de 1,9% y 7,2%, con 51 y 500 muestras respectivamente. Un trabajo interesante y que evidencia la importancia del muestreo en albergues y/o guarderías, fue realizado en Canadá, donde se encontró una positividad del 36,5% en un muestreo de 663 albergues/guarderías (Colman et al. 2017, Jung et al. 2018, Castrillón-Salazar et al. 2019, de Oliveira et al. 2019, Oosthuizen et al. 2019, Whitten et al. 2019, Anyaoha et al. 2020, Galarce et al. 2020, Kamga et al. 2020, Weese et al. 2020, Laverde et al. 2021, Suárez-Esquivel et al. 2021, Hamdy et al. 2023).
Costos en salud/discapacidad por brucelosis. En diversos estudios las estimaciones de los costos asociados con las infecciones de brucelosis se limitan a países específicos, todos los datos sugieren que las pérdidas económicas a nivel mundial debido a la brucelosis son extensas, tanto en términos de salud y producción ganadera como en salud pública (costos de tratamiento y pérdida de productividad en humanos). Los costos asociados con brucelosis y atención en salud están relacionados con la atención ambulatoria y hospitalaria. Los costos directos, en un estudio en China, fueron de 688,6 dólares con un rango entre 333,4 a 1.563,5. Los costos médicos fueron significativamente altos con valores en promedio de 541,28 y 101,48 dólares respectivamente. Existen otros costos que asume el paciente, los denominados gastos indirectos (costo máximo del plan de salud en un año), que oscilan entre 202,9 a 939,4 dólares. Curiosamente, aunque los pacientes con un nivel socioeconómico más alto gastan más al acceder a medicamentos y otros gastos adicionales más elevados, los pacientes con un nivel económico más bajo reportan un mayor porcentaje de su salario gastado en la atención médica, lo cual denota la significativa carga financiera que enfrentan las personas de entornos socioeconómicos más bajos, incluso con gastos indirectos relativamente menores (Charypkhan et al. 2019, Dadar et al. 2021). Un trabajo realizado en Kazajistán demostró en un año más de 1.300 casos de brucelosis humana (incidencia de 7,6 casos por 100.000), lo que resulta en una carga de enfermedad de más de 700 años de vida ajustados por discapacidad (AVAD) por cada año en ese país (Charypkhan et al. 2019). En España, por ejemplo, en una recopilación de casos de brucelosis humana en 18 años se registraron 5.066 pacientes (en 5.598 hospitalizaciones), lo que representa un costo promedio por paciente hospitalizado de 3.091,5 euros ± 1.780,6 euros (a la fecha esto representa 3.460,3 ± 1.993,03 dólares) y la hospitalización en promedio fue de 11,4 días (Guerrero-Espejo y Muñoz-Parada 2021). Al contrario, en India, se estimó que las pérdidas anuales medianas debidas a la brucelosis humana eran de 10,46 millones de dólares estadounidenses, con una pérdida de 7,37 millones de dólares en adultos y 3,08 millones de dólares en los niños. La brucelosis humana en India causó una pérdida de 177,601 a una tasa de 0,15 AVAD por cada mil personas por año. Se encontró que los AVAD eran de 0,29 por cada mil personas por año en la población adulta ocupacional o clase trabajadora y de 0,13 en la población adulta no ocupacional (Singh et al. 2018).
Análisis Costos en salud/discapacidad. Los años de vida ajustados por discapacidad, AVAD o DALYs combinan los años potenciales de vida perdidos (APVP) más los años vividos con discapacidad (AVD) dentro del proceso salud enfermedad. Su principal utilidad se refiere a los estudios de carga de la enfermedad, los cuales se definen como un indicador que permite medir las pérdidas de salud que para una población representan la mortalidad prematura y la discapacidad asociada a las enfermedades. Un DALYs representa la pérdida de un año que equivale a un año de completa salud, o equivalente a la pérdida de un año 100% saludable. Los AVAD representan la carga de una enfermedad, expresada como la suma del número de años vividos sin salud, con una discapacidad y los años perdidos por una muerte prematura. Un AVAD se puede considerar "un año de vida con salud" perdido. Los AVAD consideran el impacto de los años vividos con discapacidad después del inicio de la enfermedad y los años de vida perdidos debido a la mortalidad prematura en comparación con una esperanza de vida estandarizada. El total de AVAD de una población también se puede considerar una medición de la diferencia entre el estado de salud actual de la población y una situación ideal en la que cada persona disfruta de una buena salud hasta la vejez (Alvis y Valenzuela 2010). Para el caso de brucelosis se reportaron 700 años de vida y para leptospirosis esto es muy variable con datos que van desde 2,9 hasta 15 (DALYs), este indicador estima la pérdida de vida plena o saludable que ocurre en una sociedad por la presencia de una enfermedad.
La leptospirosis causa efectos a largo plazo en el 30% de personas que experimentan cuadros agudos mientras que las que se ven afectadas de forma crónica pueden gastar una cantidad variable de tiempo incapaz de volver a su trabajo, y solo una proporción de ellos puede continuar trabajando en su ocupación habitual (Sanhueza et al. 2020). Algunos indicadores socioeconómicos y de salud sobre la leptospirosis en Colombia indican una disminución en la calidad de vida de las personas con esta enfermedad. De hecho, la leptospirosis representa el 2% de las muertes prematuras cada año en Colombia (Arboleda et al. 2023). Además, es responsable de pérdidas económicas, ya que se estima que un máximo de 648 años de trabajo fue perdido en 2012 y un mínimo de 46 años perdidos en 2020 son atribuibles a muertes prematuras, dado que se estima que se pierden alrededor de 2 años de vida potencialmente por cada 100.000 habitantes en Colombia. Esto representa pérdidas económicas considerables. Los reportes en el año 2020 (pandemia) fue donde se presentaron los mayores porcentajes para tasa de letalidad, lo que sugiere que los casos reportados al sistema de vigilancia fueron sólo aquellos que tuvieron condiciones graves, contribuyendo al subregistro de los casos en ese año. Adicionalmente las consecuencias de la enfermedad se traducen en días de hospitalización, días de incapacidad y años de trabajo perdidos por muertes prematuras, uso indiscriminado de antibióticos (resistencia antimicrobiana en pacientes que consultan por síndrome febril de etiología desconocida) (Arboleda et al. 2023). La enfermedad causa una pérdida anual de 2,9 millones de años de vida ajustados por discapacidad (DALYs) (Petakh et al. 2022). Estas enfermedades predominan en comunidades que viven en situaciones menos favorecidas, pobreza y dificultades para acceder a servicios básicos de salud, lo cual sitúa a la leptospirosis y la brucelosis en el contexto de enfermedades tropicales desatendidas (ETD), por lo que se deben resolver las dificultades de vulnerabilidad socioeconómica y ambiental (Belaz et al. 2023).
Otros datos reportan AVAD para brucelosis entre 3,1 y 4,5 años, sin embargo, este valor es muy variable de acuerdo con las evidencias recopiladas, los países donde se han hecho algunos estudios, con valores entre mínimo 0,1 y 1,69 (DALYs). La discapacidad causada por la enfermedad también es variable, incluso por definición. En el 2010 la estimación del consenso de carga global de enfermedades, concepto que se refiere a la cuantificación del impacto que las enfermedades, lesiones y factores de riesgo tienen sobre la salud de las poblaciones en todo el mundo, define la brucelosis como enfermedad infecciosa de episodio agudo, severo, con discapacidad clase II (Capacidad limitada para realizar la mayoría de las actividades, condición dolorosa que afecta la capacidad ocupacional incluso durante el período de remisión), sin embargo, ya existen reportes que consideran una de las formas de presentación de la brucelosis como crónica (Murray 1994, Murray et al. 2012, Di Bari et al. 2022). Estudios en España, demostraron que la enfermedad puede resultar en incapacidad hasta de 49,5 días con un costo cercano a los 51,496 dólares en un grupo de 380 enfermos por brucelosis en distintos campos laborales, incluyendo costos de tratamiento y hospitalización. Similar a lo anterior, en un estudio en China, se analizó la duración de la estancia hospitalaria y los costos totales entre diferentes grupos de personas. Los pacientes de mayor edad mostraron 4,6 veces más gastos hospitalarios (5.438 dólares) por la enfermedad que los más jóvenes. Pacientes provenientes de municipios evidenciaron una estancia hospitalaria más larga (13,9 días) con unos costos de 2.627 dólares, en donde un 25% de la población fueron pacientes críticos y el 30% requirieron cirugía con una estancia hospitalaria en promedio de 20 días y costos en promedio de 10.525 dólares. En el caso de infecciones localizadas por la brucelosis, el 64% mostraron infecciones en columna y articulaciones, con un promedio de estancia hospitalaria de 18,8 días y costos de 10.160 dólares (Rodríguez et al. 1990, Ma et al. 2024), cifras que no son nada despreciables en los sistemas de salud de América latina, donde se enfrenta actualmente una crisis hospitalaria, de insumos, medicamentos, diagnóstico de enfermedades infecciosas y donde se trata de evitar la incapacidad laboral.
Para la presentación de este tipo de enfermedades existen múltiples factores ambientales, económicos, incluyendo el cambio climático, los cuales pueden estar relacionados con la distribución y persistencia. En otros países, los sistemas de información geográfica (SIG) para caracterizar la ocurrencia de enfermedades infecciosas, zoonóticas y transmitidas por vectores es ampliamente utilizado y con efectos benéficos demostrables, sin embargo, en Colombia, al igual que en otros países de América Latina, se han utilizado en diferentes enfermedades infecciosas humanas y animales (dengue, chikungunya, Zika, rabia bovina, entre otras), sin embargo, aún no es utilizado para el caso de leptospirosis y brucelosis, este tipo de estrategias podrían apoyar en la vigilancia epidemiológica y estrategias de prevención y control (PyP) (Bonilla-Aldana et al. 2023). El enfoque de Una Salud debe ser tenido en cuenta para implementar estrategias de PyP, logrando articular las secretarías de salud, ambiente, desarrollo económico, educación, planeación, y demás actores involucrados mediante la EGI-ETV-Zoonosis (Estrategia de Gestión Integrada para las Enfermedades Transmitidas por Vectores y Zoonosis). Las zoonosis deben priorizarse de acuerdo con varios criterios: 1) severidad de la enfermedad en humanos, 2) proporción de la enfermedad humana atribuida a la exposición animal, 3) carga de la enfermedad en animales, 4) disponibilidad de intervenciones y 5) colaboración intersectorial existente, esto con el fin de articular las acciones, direccionar los recursos de forma adecuada, articular planes y programas y establecer acciones de atención primaria en salud acordes a las necesidades. La integración multidisciplinar y la colaboración multisectorial fortalecen el desarrollo del sistema de vigilancia de enfermedades en humanos y animales, mejoran la capacidad de los laboratorios y apoyan la implementación de estrategias de prevención y control. Este enfoque no se trata solo del discurso, se debe entender que las relaciones hombre-animales-ecosistema son bidireccionales, por lo que el sistema y entorno en el que nos desarrollamos debe actualizarse y adaptarse constantemente, procurar nuevas herramientas diagnósticas, actualización de las normas que regulan estas enfermedades, fortalecimiento de los sistemas de vigilancia epidemiológica, la transformación debe venir desde la base (la formación profesional, desde el aula), fortalecimiento de la investigación. Si esta transformación en el tiempo no se logra se perderá el gigantesco esfuerzo realizado por la implementación de este tipo de abordaje multidisciplinar. Una salud debe destacar el papel crucial del medio ambiente en la transmisión de enfermedades al mostrar cómo la deforestación, el cambio climático, la urbanización, y distintas actividades causadas por el hombre, provocan cambios en la dinámica de las enfermedades. Debe ser motivo de investigación y articulación entre los actores de distintos campos para que trabajen juntos, trascendiendo barreras entre disciplinas para entender mejor cómo se propagan las enfermedades, facilitando la implementación de herramientas para reducir el riesgo de transmisión, estrategias de educación, normatividad, protección de la vida silvestre y la salud animal. De igual manera, unir esfuerzos para mejorar el conocimiento de los ecosistemas, de las enfermedades zoonóticas, investigación en tratamientos nuevos y medidas preventivas más efectivas, incluyendo la creación de herramientas de diagnóstico, incluyendo el acceso a estas herramientas a la población menos favorecida. A medida que aumente el contacto entre humanos, animales y el medio ambiente, los agentes continúan adaptándose, por lo que es la oportunidad de que Una Salud emerja como una barrera crucial que puede proteger la salud global (Pieracci et al. 2016, Araya 2020, Chávez de Pop et al. 2020, Choudhary et al. 2024).
Para la leptospirosis en caninos el principal reservorio son los roedores sinantrópicos, la principal fuente de contaminación son las aguas no tratadas, la medida principal de prevención es la vacunación.
En cuanto a la brucelosis canina el principal factor de riesgo es deambular libremente, la principal medida de prevención y control está dirigida a disminuir la posibilidad de que los perros se infecten por montas no deseadas o deambulen sin control (esterilización).
El saneamiento básico juega un papel determinante como estrategia para mitigar enfermedades, como la leptospirosis, que se vehiculizan a través del agua no tratada, roedores o condiciones deficientes en el manejo de residuos.
El período de incubación de ambas enfermedades es muy variable, pasa por algunos días hasta varios meses e incluso años, lo cual dificulta la detección temprana y la implementación de estrategias de prevención y control, incluyendo la diseminación del agente en el ambiente y el riesgo de contaminación a los propietarios y otros animales.
Aunque existen protocolos de tratamiento, en ambos casos no hay cura de la enfermedad, existe el riesgo de recaídas y el agente puede ser excretado por un periodo de tiempo, lo cual se convierte en un factor de riesgo. Incluso, los tratamientos con varios antibióticos, por tiempos prolongados, pueden tener efectos colaterales en el sistema inmune y la microbiota intestinal, lo cual va a repercutir directamente en la homeostasis, la fisiopatología y la recuperación del animal.
La vacunación como medida preventiva para leptospirosis debe ser recomendada a los propietarios de los animales como vacuna esencial, sin embargo, se deben revisar los antígenos de las vacunas disponibles, ya que no todas las vacunas protegen contra todas las cepas, lo cual hace necesario el uso de otras medidas de prevención y control como educación, fortalecimiento del hospedero (nutrición adecuada, desparasitación regular, control de ectoparásitos) y normas de higiene.
La esterilización quirúrgica de los animales y evitar que deambulen libremente en entornos rurales, previene el posible contagio con ambas enfermedades, evita el consumo de agua no tratada y el contacto con fauna silvestre, son factores protectores.
En cuanto a las medidas de bioseguridad, se convierte en un reto complejo que propietarios de animales positivos sigan las medidas recomendadas y el uso de elementos de protección personal, protocolos de limpieza y desinfección, el aislamiento de los animales, la cuarentena, áreas de infecciosos en clínicas veterinarias, refugios y albergues; y demás recomendaciones que de fondo, no solucionan el problema, por el contrario, pueden convertirse en medidas dispendiosas para un animal de compañía al interior de una familia.
La comunicación con los propietarios o tenedores responsables de los animales de compañía debe ser clara en cuanto a los riesgos, la relación costo/beneficio del tratamiento, el uso de medidas de bioseguridad, los efectos colaterales del uso prolongado de los fármacos y el pronóstico del paciente en cada caso particular.
Se necesitan investigaciones locales que caractericen el curso de la enfermedad en medicina humana y así poder estimar las tasas de letalidad, indicadores de discapacidad, enfermedad y cronicidad de esta, lo cual puede influir a mediano plazo en las políticas de atención en salud.
Es de suma importancia generar políticas públicas donde se consideren medidas sanitarias en albergues/refugios/guarderías, protocolos de limpieza y desinfección, la posibilidad de muestrear animales antes del ingreso a esos establecimientos y las pruebas serológicas en programas de adopción.
Agradecimientos. A las autoridades sanitarias e investigadores que apoyaron este manuscrito con información acerca del tema de costos en salud y discapacidad de brucelosis y leptospirosis, Dr. Ignacio Moriyón (U. de Navarra, España), al Ministerio de Salud y Protección Social de Colombia, al Dr. Baldomero Molina Flores (PAHO), al Dr. José María Blasco Martínez (U. de Zaragoza).
Contribución de los autores. Conceptualización: LJCM, AMJ y VMAP. Análisis formal: LJCM, AMJ y VMAP. Investigación: LJCM, AMJ y VMAP. Redacción: LJCM, AMJ, LKSM y VMAP. Elaboración de gráficos: LJCM, AMJ y VMAP. Revisión crítica del artículo: LJCM, AMJ, LKSM, VMAP. Redacción-borrador original: LJCM, AMJ, LKSM y VMAP. Redacción-revisión y edición: LJCM, AMJ, LKSM y VMAP.
Declaración de conflictos de intereses. Los autores declaran no tener conflictos de intereses financieros ni relaciones personales conocidas que pudieran haber influido en el trabajo presentado en este artículo.