Revista Veterinaria. 2026; 37(1)
https://doi.org/10.30972/vet.3719221
Artículo Original




1Grupo de investigación en Farmacología Experimental y Medicina Interna – Élite, Programa de Medicina Veterinaria y Zootecnia, Facultad de Ciencias Agropecuarias y Recursos Naturales, Escuela de Ciencias Animales, Universidad de los Llanos, Villavicencio 1745, Meta, Colombia.
2Facultad de Ciencias Agropecuarias y Recursos Naturales, Escuela de Ciencias Animales, Laboratorio de Farmacología. Universidad de los Llanos, Villavicencio 1745, Meta, Colombia.
a  libnny.barajas@unillanos.edu.co
libnny.barajas@unillanos.edu.co
b maria.pinzon.pacheco@unillanos.edu.co
maria.pinzon.pacheco@unillanos.edu.co
c  valentina.zambrano@unillanos.edu.co
valentina.zambrano@unillanos.edu.co
d dumar.jaramillo@unillanos.edu.co
dumar.jaramillo@unillanos.edu.co
Recibido: 18 diciembre 2025 / Aceptado: 19 marzo 2026
Resumen
La transferencia de inmunidad pasiva (TPI) en neonatos bovinos proveniente del calostro, esta determina la supervivencia y el desempeño productivo. El objetivo de este estudio fue comparar la capacidad diagnóstica del inmunoensayo de absorción ligado a enzima (ELISA) frente a métodos indirectos como precipitación con sulfito de sodio (SST) y turbidez con sulfato de zinc (ZST), evaluando TPI en neonatos bovinos; para ello se recolectaron 49 muestras de suero de los neonatos bovinos una hora postnacimiento (precalostrado) y muestras pareadas a las 48 horas de nacido (postcalostrado); además, se realizó la toma de 49 muestras de calostro obtenidas una hora después del parto. Para determinar la calidad de calostro se usó refractometría de Brix. La capacidad diagnóstica de las pruebas y su relación con la calidad calostral se analizaron estadísticamente con curvas ROC, correlación de Pearson y concordancia Kappa. Los resultados de ELISA mostraron: 77,6% (38/49) de los neonatos presentó TPI adecuada y el 22,4% (11/49) falla TPI. Las pruebas SST y ZST presentaron alta sensibilidad (Se) (0,97 y 1,00, respectivamente), pero baja especificidad (Sp) (0,18 y 0,09, respectivamente) y área bajo la curva (AUC) de 0,578 y 0,545, respectivamente. Para el calostro la refractometría Brix mostró: 79,6% (39/49) buena calidad, 14,3% (7/49) calidad media y 6,1% (3/49) mala calidad. Se halló una correlación de Pearson leve positiva entre la calidad del calostro y TPI (r = 0,312; p=0,029). Por consiguiente, las pruebas SST y ZST debido a su limitada Sp no deben emplearse como pruebas confirmatorias de TPI. No obstante, su alta Se respalda su uso como pruebas de tamizaje en campo de TPI, siempre que los resultados sean confirmados mediante métodos directos de mayor precisión diagnóstica como el ELISA, por otro lado, la correlación entre la calidad calostral y TPI evidencia una correlación leve positiva significante para este estudio.
Palabras clave: inmunoensayo, métodos de cribado, inmunidad neonatal.
Abstract
Passive transfer of immunity (PTI) in neonatal calves through colostrum determines their survival and productive performance. The aim of this study was to compare the diagnostic performance of the enzyme-linked immunosorbent assay (ELISA) with indirect methods such as sodium sulfite precipitation (SST) and zinc sulfate turbidity (ZST) for evaluating PTI in neonatal calves. A total of 49 serum samples were collected from calves one-hour after birth (pre-colostrum) and paired samples were obtained 48 hours after birth (post-colostrum). Additionally, 49 colostrum samples were collected in one-hour pospartum. Colostrum quality was determined using Brix refractometry. The diagnostic performance of the tests and their relationship with colostrum quality were analyzed using ROC curves, Pearson correlation, and Kappa concordance. ELISA results showed that 77.6% (38/49) of the calves had adequate PTI, whereas 22.4% (11/49) presented failure of passive transfer. The SST and ZST tests showed high sensitivity (Se) (0.97 and 1.00, respectively) but low specificity (Sp) (0.18 and 0.09, respectively), with areas under the curve (AUC) of 0.578 and 0.545, respectively. Brix refractometry indicated good colostrum quality in 79.6% (39/49) of the samples, moderate quality in 14.3% (7/49), and poor quality in 6.1% (3/49). A weak positive Pearson correlation was observed between colostrum quality and PTI (r = 0.312; p=0.029). These results indicate that SST and ZST tests should not be used as confirmatory tests for PTI due to their limited specificity. However, their high sensitivity supports their use as field screening tests, provided that results are confirmed using more accurate diagnostic methods such as ELISA.
Key words: immunoassay, screening methods, neonatal immunity.
La transferencia de inmunidad pasiva (TPI) corresponde a la absorción de inmunoglobulinas (Ig) maternas a través del intestino delgado durante las primeras 24 horas de vida, proceso fundamental para la protección inmunológica del neonato, además provee anticuerpos y componentes inmunoestimulantes para el desarrollo y funcionalidad sistémica del organismo neonatal (Puppel et al. 2020, Turini et al. 2020). La principal Ig presente en el calostro bovino es la IgG, cuya concentración oscila entre 30 y 87 g L-1, representando aproximadamente el 80-90% del total de Ig. En contraste, otras clases como IgA, IgM, IgE e IgD, se encuentran en proporciones menores, desempeñando un papel complementario dentro del perfil inmunológico del calostro (Godden et al. 2019).
La TPI y los niveles séricos de IgG están altamente correlacionados con el total de Ig ingerida por los terneros (Yang et al. 2015). Los principales factores de riesgo que contribuyen a la falla TPI (FTPI) en terneros incluyen la administración de calostro de calidad deficiente o un volumen insuficiente de calostro durante las primeras 24 horas después del nacimiento (Turini et al. 2020). La concentración de IgG en el calostro ha sido ampliamente utilizada como criterio de referencia para definir su alta calidad a los niveles de IgG superiores a 50 g L-1 (Godden et al. 2019). Se ha demostrado que una alta calidad del calostro se correlaciona positivamente con el crecimiento del microbioma probiótico, pero esta influencia de la calidad del calostro no solo se limita únicamente a la conformación de la microflora intestinal, sino también a su condición de fuente primaria de anticuerpos y componentes inmunoestimulantes para el desarrollo y funcionalidad del neonato (Puppel et al. 2020).
La inmunodifusión radial (RID) es una técnica ampliamente reconocida como la prueba de referencia para evaluar la TPI, al proporcionar una medición directa y reproducible de IgG, utilizada para la validación de otros métodos. No obstante, el inmunoensayo ELISA se utiliza con frecuencia en estudios experimentales debido a su rapidez y viabilidad operativa, esta prueba directa ha demostrado una adecuada correlación con RID para la clasificación de TPI (Ahmann et al. 2021, Popescu et al. 2024). Para la evaluación de TPI de forma indirecta en muestras de suero sanguíneo existen dos técnicas: precipitación con sulfito de sodio (SST) y turbidez con sulfato de zinc (ZST), basadas en la formación de precipitación/turbidez como señal indirecta de la concentración de Ig (Hogan et al. 2016, Reyes-Castañeda et al. 2016). Para evaluar la calidad calostral, las pruebas más utilizadas son el refractómetro óptico, refractómetro digital Brix y el calostrómetro (Buczinski y Vandeweerd. 2016, Röder et al. 2023).
Los terneros nacen prácticamente desprovistos de anticuerpos, por ello, el manejo del calostro es uno de los factores cruciales que afectan la salud y supervivencia del ternero (Lora et al. 2018, Souza et al. 2021). En un estudio de metaanálisis, los terneros con FTPI tienen el doble de riesgo de morir, 1,8 veces más riesgo de desarrollar enfermedades respiratorias y 1,5 veces más riesgo de tener diarrea en comparación con los que no tienen FTPI (Uyama et al. 2022). Por lo tanto, se recomienda monitorear la eficiencia aparente de la absorción de Ig en los terneros para evaluar las prácticas generales de manejo del calostro (Lopez y Heinrichs. 2022). Los estudios enfocados en la absorción de Ig y en la concentración de sus componentes en el calostro permiten comprender su impacto sobre la TPI, así como sobre la salud y la supervivencia de los terneros (Souza et al. 2021).
El objetivo de este estudio fue comparar la capacidad diagnóstica del inmunoensayo ELISA frente a métodos indirectos como SST y ZST para evaluar la TPI en neonatos bovinos.
Ubicación. El estudio se llevó a cabo en un predio lechero bovino ubicado en el municipio de Cumaral, Meta, Colombia, con ordeño mecánico de aproximadamente 600 vacas al día y ciclo cerrado de raza Girolando, en su mayoría multíparas, con un promedio de producción de 35-40 Litros por día. Durante el periodo evaluado los bovinos se mantuvieron bajo supervisión médica veterinaria permanente y no presentaron alteraciones clínicas ni evidencia de enfermedad. Los bovinos recibieron dietas ajustadas a sus requerimientos nutricionales según su estado fisiológico y productivo. Las raciones fueron formuladas por un nutricionista y preparadas en la planta de alimentación del predio, asegurando la homogeneidad y la consistencia en el suministro. El muestreo se efectuó en época de verano, bajo las condiciones climáticas de temperatura promedio máxima de 30 °C, mínima de 20 °C y humedad relativa >42% (IDEAM 2025).
Tamaño de muestra y tipo de estudio: El estudio fue de tipo observacional, longitudinal-analítico, no probabilístico, con un enfoque semicuantitativo. El tamaño muestral estuvo determinado por la disponibilidad de partos que cumplieron con los criterios metodológicos del estudio durante el periodo de muestreo, así como por el acceso limitado al predio y a los sujetos experimentales. De un hato compuesto por aproximadamente 600 vacas en ordeño, se incluyeron 49 vacas paridas y sus respectivas crías hembras, correspondientes a partos eutócicos ocurridos bajo condiciones que permitieron la toma de muestras dentro de la primera hora de vida del neonato. Este intervalo fue crítico para garantizar la validez de las variables evaluadas. Todos los partos fueron no programados y ocurrieron durante el día, lo cual facilitó el acceso a los neonatos.
Toma de muestras y pruebas de laboratorio: En los neonatos se obtuvieron dos muestras sanguíneas de 3 mL por venopunción yugular utilizando agujas 21G (Vacuplast®, Nanchang, China) y tubos tapa roja sin coagulantes, previa antisepsia de la zona de punción. La primera muestra se tomó una hora después del nacimiento, previo al consumo de calostro (precalostrado), donde posteriormente se aseguró consumo de calostro dentro de las primeras 6 horas de vida. La segunda muestra fue a las 48 horas de nacido (postcalostrado). Las muestras fueron centrifugadas a 3.500 rpm durante 10 minutos; el suero obtenido se alicuotó en viales estériles y se almacenó a -25 °C hasta su procesamiento. Las muestras de calostro (5 mL) se recolectaron inmediatamente postparto, ya sea directamente de la madre (cuando el neonato consumía calostro directamente de la glándula mamaria) o del banco de calostro del predio (cuando el calostro materno presentaba baja calidad según la evaluación mediante refractometría digital Brix del predio), con esto se aseguró un manejo homogéneo en cuanto a la calidad del calostro suministrado y se garantizó condiciones comparables entre todos los neonatos incluidos. Todas las muestras fueron recolectadas por el personal responsable del área de partos del predio y fueron almacenadas en viales estériles, identificadas y mantenidas a -25 °C hasta su análisis, manteniendo el origen de cada muestra en condición ciega para el grupo investigador.
Para la evaluación de TPI en los sueros sanguíneos se utilizó el inmunoensayo ELISA (MonoScreen QuantELISA Immunoglobulin Easy - BIO K 420®, Bio-X Diagnostics, Bélgica) siguiendo las indicaciones del fabricante (manual del kit). La técnica se llevó a cabo con alícuotas de 100 µL de suero por pozo en placas previamente sensibilizadas con el antígeno específico. La lectura de absorbancia se efectuó en un lector de microplacas a 450 nm y los datos obtenidos fueron analizados mediante la plataforma AnalysiScreen® de Bio-X Diagnostics (plataforma AnalysiScreen®). La clasificación de TPI siguió los lineamientos de Fernandez-Novo et al. (2025), donde una excelente (E) TPI (ETPI) está ≥25,0 mg mL-1 de IgG, buena (B) TPI (BTPI) con 18,0-24,9 mg mL-1, regular (R) TPI (RTPI) con 10,0-17,9 mg mL-1 y falla (F) TPI (FTPI) en 10 mg mL-1.
Como métodos indirectos para la evaluación de TPI en los sueros sanguíneos se usaron las pruebas de SST y ZST. En la Prueba SST se prepararon soluciones al 14, 16 y 18% de sulfito de sodio, las cuales se mezclaron con 0,1 mL de suero sanguíneo de los neonatos en tubos de ensayo. La presencia o ausencia de precipitado a distintos tiempos permitió clasificar la concentración de IgG en tres rangos, si precipita en 14% es efectiva la TPI (> 15 mg IgG mL-1), en 16% es parcial la TPI % (5-15 mg IgG mL-1) y en 18% (≤ 5 mg IgG mL-1) hay FTPI, según la metodología descrita por García et al. (2006).
En la prueba ZST, se mezclaron 3 mL de solución de sulfato de zinc al 20,8% (d = 1,06 g mL-1) con 0,1 mL de suero sanguíneo del neonato, evaluando la reacción semicuantitativa de la turbidez generada tras 15 minutos de reacción, asimismo, la intensidad de la opacidad se interpretó visualmente, donde la ausencia de turbidez fue indicativa de FTPI, correspondiente a concentraciones séricas <10 mg IgG mL-1, de acuerdo con lo propuesto por Hogan et al. (2016).
Por otro lado, la calidad calostral se evaluó mediante refractometría óptica (%Brix) con un refractómetro portátil (Brixco Instruments, Alemania; rango 0-90% Brix). Se clasificó como calostro de buena calidad valores ≥22% Brix (≥50 g L-1 de IgG), calidad media o aceptable 18-21% Brix y calidad inaceptable <17% Brix, de acuerdo con Buczinski y Vandeweerd (2016).
Análisis estadístico. Los datos recolectados fueron tabulados y analizados utilizando estadística descriptiva, se estimó la media (x̅) y desviación estándar (±), para determinar la frecuencia de TPI en los neonatos y la calidad calostral. A los datos se les aplicó la prueba de normalidad de Shapiro-Wilk, donde no se evidenciaron diferencias significativas respecto a la distribución normal. Los resultados obtenidos en ELISA y en las pruebas SST y ZST se sometieron al análisis de la curva “Receiver operating characteristic” (ROC), con el fin de evaluar la TPI en neonatos bovinos, según lo descrito por Roy-García et al (2023) este análisis permitió establecer puntos de corte óptimos y evaluar la capacidad discriminatoria entre SST y ELISA, y ZST y ELISA. Los índices de rendimiento diagnóstico, incluyendo los valores predictivos positivos (PPV) y negativos (NPV), la proporción de falsos positivos (FP) y falsos negativos (FN), así como los índices de sensibilidad (Se), especificidad (Sp), significancia estadística (p) y área bajo la curva (AUC) comparando la prueba directa ELISA con las pruebas indirectas SST y ZST. Para la construcción de las tablas de contingencia se consideró como resultado positivo aquellos neonatos con ETPI y BTPI, y como resultado negativo a los individuos con RTPI y FTPI, aplicando este mismo criterio tanto a la prueba ELISA como a las pruebas SST y ZST. Por otro lado, la concordancia diagnóstica se evaluó mediante el índice Kappa de Cohen utilizando el software SPSS v.2025.27. Además, la correlación de Pearson se realizó utilizando el software R-studio v.2025.09.1 + 401. Se empleó el software Jamovi v.2.6.44 para hallar el área bajo la curva (AUC), siendo una medida global de la capacidad discriminatoria de la prueba diagnóstica, al evaluar su desempeño a lo largo de todos los puntos de corte posibles e integrar la relación entre Se y Sp, distinguiendo entre individuos con y sin la condición evaluada, independientemente del umbral seleccionado, lo que permite valorar su capacidad predictiva (Çorbacıoğlu y Aksel. 2023). En el presente estudio el AUC se utilizó para estimar la capacidad de las pruebas indirectas SST y ZST frente a ELISA, para discriminar entre neonatos bovinos con adecuada TPI y aquellos con FTPI comparándolas con la prueba ELISA, en este sentido, se indica un AUC <0,5 indica ausencia de poder discriminativo; valores entre 0,6-0,75 capacidad moderada; >0,75 buena capacidad discriminativa y >0,9 excelente precisión diagnóstica/discriminativa (Martínez y Pérez. 2023). Todos los análisis se calcularon los intervalos de confianza del 95% (IC95%) y se consideró un valor de p<0,05 como nivel de significancia estadística.
Consideraciones éticas. Todos los procedimientos realizados con los bovinos cuentan con el aval del Comité de Bioética de la Universidad de los Llanos, según Acta N° 15 de 13 de noviembre de 2025. Los animales relacionados a la investigación se manejaron asegurando su bienestar y siguiendo la normativa vigente para mantener su integridad según la Ley 84 de 1989 “Estatuto Nacional de Protección de los Animales” y la Resolución 8430 de 1993 del Ministerio de Salud. El nombre de la empresa vinculada en este estudio se mantuvo bajo la confidencialidad de la información en cumplimiento de la Ley 1581 de 2012 (protección de datos personales) y el Artículo 15 de la Constitución Política (hábeas data) de Colombia.
En ELISA, las muestras precalostrado presentaron concentraciones séricas de IgG entre 0 y 8,73 mg mL-1. En contraste, las muestras postcalostrado evidenciaron un incremento en la concentración de IgG, con valores que oscilaron entre 6,7 y 143,2 mg mL-1 (Figura 1). A partir de estas concentraciones, la clasificación de la TPI fue ETPI 57,1% (28/49), BTPI 20,4% (10/49), RTPI 16,3% (8/49) y FTPI 6,1% (3/49).
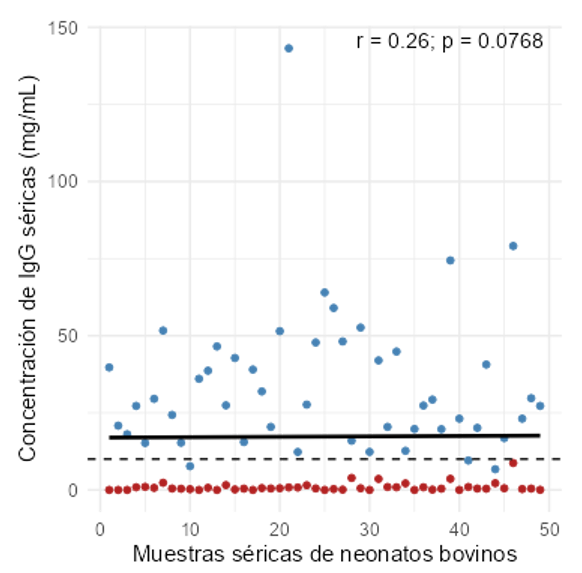
La prueba SST evidenció que en las muestras de suero sanguíneo de los neonatos bovinos en el precalostrado fueron negativas en todas las concentraciones evaluadas. Por otro lado, en las muestras postcalostrado se obtuvo precipitación en un 65,3% (32/49) a 14%; 28,5% (14/49) en 16% y 6,1% (3/49) al 18%.
En la prueba ZST, todas las muestras correspondientes a precalostrado mostraron ausencia de turbidez. Mientras tanto, en las muestras postcalostrado se observó turbidez en un 93,8% (46/49) y ausencia de turbidez en el 6,1% (3/49) de las muestras.
Por otro lado, con la refractometría de Brix se determinó que los calostros evaluados presentaron una buena calidad en el 79,6% (39/49), calidad media de 14,3% (7/49) y mala calidad de 6,1% (3/49). Encontrando valores comprendidos entre 11 y 36% Brix en el refractómetro óptico (x̅ 25,8 ± 5,68% Brix).
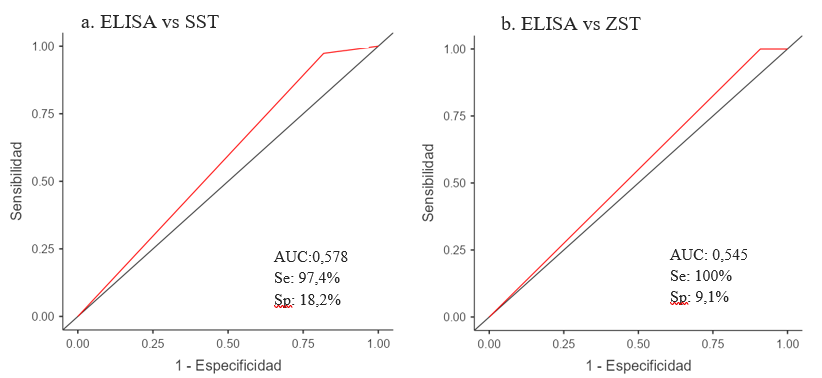
En la Tabla 1 se observa el comportamiento de las pruebas indirectas SST y ZST frente, con la prueba de referencia ELISA. El AUC de ELISA frente SST fue de 0,578 (Figura 2a) y el de ELISA frente ZST fue de 0,545 (Figura 2b).
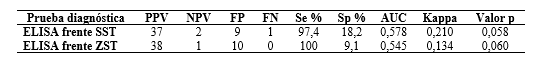
PPV: valor predictivo positivo. NPV: valor predictivo negativo. FP: falso positivo. FN: falso negativo. AUC: área bajo la curva. SST: precipitación con sulfito de sodio. ZST: turbidez con sulfato de zinc. ELISA: Ensayo de inmunoabsorción ligado a enzima. Se: sensibilidad. Sp: especificidad.
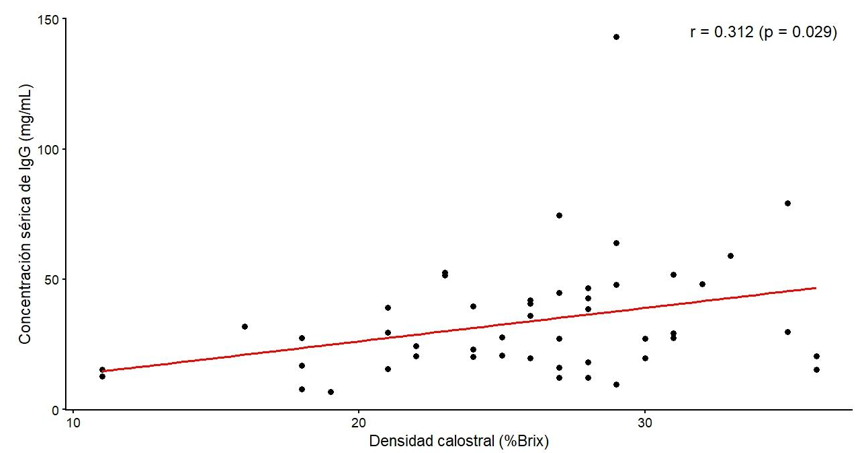
La correlación de Pearson entre la densidad del calostro (%Brix) y la concentración de Ig medidas en la muestra sérica postcalostrado en ELISA fue de r = 0,312 (p = 0,029) (Figura 3).
El inmunoensayo ELISA es una prueba directa aceptada para evaluar la TPI en neonatos bovinos, además los estudios de TPI en hatos bovinos demuestran una variación significativa entre poblaciones bovinas (Hampe et al. 2021, Michelsen et al. 2025). Este comportamiento puede estar bajo influencia de factores como el manejo, la calidad y el momento del suministro del calostro, así como condiciones sanitarias del sistema productivo (Lora et al. 2018, Godden et al. 2019).
En este estudio, la comparación de ELISA frente a las pruebas SST y ZST evidenciaron un desempeño diagnóstico limitado para la TPI en suero sanguíneo para ambas pruebas indirectas rápidas (Tabla 1). En este contexto, la alta Se de SST y ZST podría permitir la identificación inicial (tamizaje) de neonatos bovinos con FTPI. Por otro lado, la baja Sp, de estas mismas pruebas, compromete su utilidad como pruebas confirmatorias de TPI, restringiendo su aplicación a pruebas de tamizaje que deben complementarse con métodos de mayor precisión diagnóstica.
Las pruebas indirectas, como SST y ZST, son de bajo costo, pero presentan restricciones en su precisión diagnóstica (García et al. 2006, Souza et al. 2021). La refractometría Brix es una herramienta confiable para estimar la calidad del calostro; sin embargo, las pruebas de campo destinadas a esta evaluación pueden presentar variabilidad considerable en su desempeño diagnóstico, lo que sugiere que factores como el manejo de la muestra, las condiciones de la medición y la interpretación de los resultados influyen en su eficiencia (Röder et al. 2023, Sockett et al. 2023). En consecuencia, la elección de la prueba para evaluar la TPI no depende solo de la concentración calostral, sino del momento de evaluación, el objetivo diagnóstico y los recursos disponibles (Godden et al. 2019, Puppel et al. 2020, Turini et al. 2020).
Los hallazgos obtenidos en el rendimiento diagnóstico de ELISA frente SST en este estudio (Tabla 1, AUC = 0,578, Se 97,4% y Sp 18,2%) contrasta con los reportados por Lee et al. (2008), quienes concluyeron que SST en concentraciones 14%, 16% y 18% presentó AUC = 0,88, Se 76% y Sp 99%. Asimismo, García et al. (2006) documentaron valores de Se 89-94% y Sp 86-90% para esta prueba indirecta. En concordancia con los resultados obtenidos en este estudio, Souza et al. (2021) encontraron que la mayoría de los estudios de TPI medidos por pruebas indirectas, la SST alcanza Se 70-95%; por otro lado, existe disparidad con lo esperado en Sp 70-90% en esta misma prueba. Weaver et al. (2000) describen que las diluciones clásicas del SST (14% y 16%) requieren concentraciones de IgG inusualmente altas para generar turbidez, lo que conduce a una mayor probabilidad de clasificar incorrectamente a terneros con niveles fisiológicos normales de inmunoglobulinas como neonatos con FTPI.
La prueba SST para TPI es empleada en una proporción estandarizada de 0,1 mL de suero en 1,9 mL de solución, la cual favorece la precipitación temprana de IgG, por tanto, presenta alta Se para detectar terneros con FTPI (García et al. 2006, Male Here et al. 2026). No obstante, la baja Sp obtenida en este estudio, se puede atribuir a factores preanalíticos como deshidratación, procesos inflamatorios subclínicos y variaciones en el momento del muestreo postnacimiento, que incrementan la frecuencia de FP y reduce la Sp (Souza et al. 2021). En este sentido, Weaver et al. (2000) señalan que la priorización de la Se de esta prueba mediante determinados puntos de corte o diluciones del reactivo incrementa de manera sustancial la tasa de FP, comprometiendo la Sp diagnóstica de la prueba.
El rendimiento diagnóstico de ELISA frente ZST en este estudio (Tabla 1, AUC = 0,545, Se 100% y Sp 9,1%) difiere con lo reportado por Hogan et al. (2016), quienes hallaron AUC=0,875, Se 98% y Sp 30%. Estas discrepancias pueden atribuirse, en parte, dado que la precisión diagnóstica de ZST es susceptible a variaciones en la concentración, el tiempo de reacción y la presencia de hemólisis (Dunn et al. 2018, Souza et al. 2021). En concordancia, Hudgens et al. (1996) demostraron que una solución de ZnSO4 a 200 mg mL-1 presentó una Se 100% y Sp 25,5% y al incrementar la concentración de ZnSO4 a 350 mg mL-1 mejoró significativamente la Sp. Por otro lado, Dunn et al. (2018) halló que la lectura espectrofotométrica en comparación con la evaluación visual incrementa la Sp. Asimismo, Denholm et al. (2022) concluyeron que la reducción de los puntos de corte mejora el rendimiento diagnóstico de la prueba. Weaver et al. (2000) y Cuttance y Laven (2019) indicaron que ZST, al no ser específica para IgG, puede generar FP, reduciendo la Sp, por lo que debe considerarse únicamente como herramienta de tamizaje.
El análisis de correlación de Pearson en este estudio evidenció una asociación positiva leve significativa entre la calidad del calostro medida por refractometría de Brix y la concentración de Ig obtenida mediante inmunoensayo ELISA en neonatos bovinos (Figura 3, r = 0,312; p = 0,02). Al respecto, Fahim y Imbabi (2021) hallaron una correlación significativa entre buena calidad de calostro y TPI (r = 0,68; p<0,05). Asimismo, Michelsen et al. (2025) encontraron una alta correlación entre las mediciones de IgG sérica en TPI y %Brix del calostro (r = 0,88). Estas discrepancias podrían deberse al uso de refractometría Brix óptica en este trabajo, en contraste con la refractometría digital empleada en otros estudios. Sockett et al. (2023) encontraron que la refractometría digital tiene un nivel de precisión diagnóstica de Se 80,2% y Sp de 82,6% a ≥ 22%Brix. Elsohaby et al. (2015) hallaron que la refractometría de Brix digital muestra un mejor desempeño que la refractometría óptica, al obtener una Se del 85,5% frente al 80% reportado para el método óptico al medir calidad calostral.
Se concluye que, las pruebas SST y ZST debido a su limitada Sp no deben emplearse como pruebas confirmatorias de TPI. No obstante, su elevada Se podría respaldar su uso como pruebas de tamizaje en campo, siempre que los resultados sean confirmados mediante métodos directos de mayor precisión diagnóstica, como el inmunoensayo ELISA. Por otro lado, la correlación entre la calidad calostral y TPI para este estudio evidenció una correlación leve positiva significante.
Agradecimientos. Los autores agradecen a Santiago Gonzales por su colaboración en el registro de las fechas de nacimiento de los neonatos, así como en el almacenamiento y entrega de las muestras. Asimismo, expresan su agradecimiento a las médicas veterinarias Laura Ordoñez y Luisa Ospina por su valiosa participación en las actividades de recolección de muestras, cuyo apoyo fue fundamental para el desarrollo de la investigación.
Contribución de los autores. LGBH: Recolección de datos, análisis estadístico, redacción-borrador original, visualización, administración del proyecto. MFPP: Recolección de datos, análisis estadístico, redacción del borrador original del manuscrito. VZH: Redacción del borrador original del manuscrito. DAJH: Conceptualización, validación, recursos, redacción-revisión y edición, supervisión.
Declaración de conflictos de intereses. Los autores declaran no tener conflictos de intereses financieros ni relaciones personales conocidas que pudieran haber influido en el trabajo presentado en este artículo.
Disponibilidad de datos. Los datos estarán disponibles previa solicitud.