Revista Veterinaria. 2026; 37(1)
https://doi.org/10.30972/vet.3719223
Artículo Original




1Facultad de Ciencias Exactas Químicas y Naturales. Félix de Azara 1552 5to piso Laboratorio 22.
Recibido: 22 agosto 2025 / Aceptado: 18 marzo 2026Resumen
El parque Natural Municipal Gruta India está ubicado en el Municipio de Garuhapé, Misiones y tiene por finalidad la conservación de la biodiversidad de la Selva Paranaense y del patrimonio cultural del sitio. Un tramo del arroyo Tres de Mayo atraviesa el área protegida y fue estudiado con el objetivo de determinar la composición, estructura y el estado de conservación de la comunidad íctica. Se realizaron cuatro muestreos estacionales, entre los años 2022 y 2023, con redes de espera monofilamento de 2,5; 3; 4 y 5 cm entre nudos opuestos, y red de arrastre o copo en las zonas de menor profundidad con vegetación flotante o palustre. La diversidad específica estuvo representada por 43 especies pertenecientes a los Ordenes Characiformes, Siluriformes, Gymnotiformes, Cichliformes, Perciformes y Clupeiformes. La diversidad alfa (H') tuvo un valor de 3 y los estimadores no paramétricos Chao2 y Jackknife1, indicaron que aún restarían por registrar entre 12 y 17 especies. La distribución rango–abundancia evidenció diferencias en la estructura de la comunidad entre los sectores del arroyo, destacando la región potámica por presentar la mayor riqueza específica (33 especies) y abundancia (164 individuos). La similitud entre los puntos de muestreo fue de moderada a baja (2-32%). Siete especies fueron clasificadas como comunes o abundantes, mientras que 29 especies raras se registraron principalmente en sitios influenciados por el río. Se identificaron seis especies endémicas, entre ellas Rhamdella cainguae y Rineloricaria misionera clasificadas como vulnerables según las categorías y criterios de la Lista Roja de la UICN. Estos resultados indican que el arroyo funciona como un refugio importante para la ictiofauna endémica y amenazada, lo que resalta su alto valor ecológico y la necesidad de implementar estrategias de conservación específicas, a escala de cuenca, que aseguren su protección a largo plazo.
Palabras clave: ictiofauna, arroyos interiores, endemismo, conservación.
Abstract. The Gruta India Municipal Natural Park is located in the municipality of Garuhapé, Misiones Province, Argentina, and its main purpose is the conservation of the biodiversity of the Parana Rainforest and the cultural heritage of the site. A reach of the Tres de Mayo stream flows through the protected area and was studied to determine the composition, structure, and conservation status of the fish community. Four seasonal sampling events were conducted between 2022 and 2023 using monofilament gill nets with mesh sizes of 2.5, 3, 4, and 5 cm between opposite knots, and a seine net and hand net in shallow areas with floating or emergent (palustrine) vegetation. Species diversity comprised 43 species belonging to the orders Characiformes, Siluriformes, Gymnotiformes, Cichliformes, Perciformes, and Clupeiformes. Alpha diversity (H′) reached a value of 3, while the non-parametric richness estimators Chao2 and Jackknife1 suggested that an additional 12 to 17 species remain undetected. Rank–abundance patterns revealed marked differences in fish assemblage structure among stream reaches, with the potamic reach exhibiting the highest species richness (33 species) and abundance (164 individuals). Similarity among sampling sites ranged from low to moderate (2–32%). Seven species were classified as common or abundant, whereas 29 rare species were predominantly recorded at sites under direct river influence. Six endemic species were recorded, including Rhamdella cainguae and Rineloricaria misionera, which are categorized as Vulnerable according to the categories and criteria of the IUCN Red List. These findings indicate that the stream functions as an important refuge for endemic and threatened ichthyofauna, highlighting its high ecological value and the need to implement basin-scale conservation strategies to ensure its long-term protection.
Key words: ichthyofauna, inland streams, endemism, conservation.
Satisfacer las necesidades de la población mundial y conservar la biodiversidad implica articular entre preservación y uso sustentable de las especies y los ecosistemas. Esta compleja tarea involucra actores e intereses de índole económica, social, política, ambiental y cultural a veces contrapuestos. En la actualidad, las áreas protegidas son la herramienta más aceptada para la conservación de la biodiversidad y en la Cuenca del Plata se han creado 601 áreas que cubren el 7,2% de su superficie (Comité Intergubernamental Coordinador de los Países de la Cuenca del Plata 2017). La selva Atlántica, en la provincia de Misiones, es una de las áreas de mayor biodiversidad de Argentina y las áreas naturales juegan un rol fundamental en su conservación, a la vez que brindan valores y servicios a la humanidad. El 15,72% del territorio provincial (2.980,10 ha) compone un sistema de 71 áreas protegidas de diferente administración, 3 de orden nacional (área protegida de Parques Nacionales), 22 Parques Provinciales, 3 Reservas Provinciales, 2 Reservas de Usos Múltiples, 4 Paisajes Protegidos, 11 Reservas Municipales, 28 Reservas Privadas y 1 Parque Federal (Sistema Federal de Áreas Protegidas 2024). A pesar de este número, es un sistema con deficiencias ya que su diseño responde principalmente a aspectos de conservación de ecosistemas terrestres sin contemplar aspectos de la biodiversidad de ríos y arroyos de Misiones (Araya et al. 2021).
El Parque Natural Municipal Gruta India creado en el año 2020, por Ordenanza Municipal e incorporado al sistema provincial de áreas naturales protegidas (Resolución Ministerial 595/21), está ubicado en el Municipio de Garuhapé, Misiones. Uno de los objetivos del plan de manejo del Parque es la conservación de la biodiversidad de la Selva Paranaense y del patrimonio cultural, este último representado por un sitio arqueológico datado en aproximadamente 4.000 años de acuerdo con la cronología radiocarbónica (LP -1446: 3550 ± 60 AP). Se ha datado material lítico y cerámico, esqueletos humanos y numerosos restos faunísticos tanto de vertebrados como de invertebrados.
Una gran gruta, denominada Tres de Mayo, se ubica sobre la margen derecha del arroyo homónimo, en ella encontraron protección las comunidades altoparanaenses, que habitaron Sudamérica en el Paleolítico (Rizzo et al. 2006). Este paisaje, en el que se destaca el Salto Tres de Mayo, integra cultura, arqueología y naturaleza en un marco de gran diversidad volviéndolo un recurso de elevado valor turístico.
Los ecosistemas acuáticos de Misiones pertenecen a la Provincia de los Grandes Ríos (López et al. 2005), poseen una ictiofauna notablemente diversa. Se estima que más de 300 especies de peces habitan los cursos de agua de Misiones, lo que representa más del 60% de las 581 especies de peces continentales de la Argentina (Koerber et al. 2024). Se destaca el alto endemismo de la comunidad íctica de Misiones, contabilizando hasta el momento 80 especies de distribución restringida a arroyos y ríos de Misiones y la región (Mirande y Koeber 2020, Araya et al. 2021).
En los últimos años, con la identificación de nuevas especies realizadas por investigadores como Říčan et al. (2023), Alonso et al. (2024) y Benítez et al. (2024) entre otros, se ha avanzado en los inventarios de peces en Misiones, sin embargo, siguen siendo incompletos (Araya 2017).
El objetivo del presente estudio fue determinar la composición y estructura de la comunidad íctica, considerando el estado de conservación de las especies, en el tramo del arroyo Tres de Mayo que atraviesa el Parque Natural Municipal Gruta India. Se trata del primer relevamiento realizado con rigor científico en la zona, y proporcionará información de base esencial para la gestión de la Reserva y la conservación de sus recursos naturales.
El estudio fue desarrollado en el marco del convenio entre la Facultad de Ciencias Exactas Químicas y Naturales de la Universidad Nacional de Misiones, a través del proyecto de investigación “Peces de interés ornamental de la provincia de Misiones” y la Municipalidad de Garuhapé, Misiones. El permiso de investigación fue otorgado por el Instituto Misionero de la Biodiversidad (IMiBio) a través de la Disposición Nº 16 -2022.
Área de estudio. El arroyo Tres de Mayo integra la Región de Humedales de los arroyos de Misiones en relieve escarpado, las nacientes se ubican en las Serranías Centrales (26°49’19’’S y 54°47'19’’O) a 310 msnm, municipios de El Alcázar y Garuhapé, en lotes de la empresa Arauco con monte nativo aún conservado. Ocupa una superficie de 113 km2 y 20,2 km de longitud con rumbo O y NO. Por su margen derecha y a 16,5 km de las nacientes, recibe al arroyo Yatetay y luego desemboca en el río Paraná.
El entorno ripario del arroyo Tres de Mayo, está compuesto por vegetación típica de la selva marginal del Distrito Fluvial (Martínez Crovetto 1963). Esta franja angosta en galería alberga especies de la selva misionera, como Tabebuia heptaphylla, Enterolobium contortisiliquum, Parapiptadenia rigida y Peltophorum dubium y otras, como Ocotea acutifolia, Nectandra angustifolia y Cytharexylum montevidense adquieren relevancia en estos ambientes (Cabrera 1976).
Diversos ambientes fluviales fueron distinguidos en el tramo estudiado del arroyo Tres de Mayo, caracterizados principalmente por la pendiente del cauce, la velocidad de la corriente y el tipo de sustrato. En las zonas de pendiente más pronunciada, el flujo del agua es turbulenta sobre un lecho rocoso de basalto, roca granulada y canto rodado con escasa vegetación adherida. Estas condiciones generan una secuencia de ambientes caracterizados por la corriente intensa, alternados con pozas más profundas en las que la velocidad de la corriente disminuye permitiendo el depósito de sustrato más fino sobre el que puede establecerse la vegetación enraizada. A medida que se reduce la pendiente, el lecho de roca basáltica da paso a extensas zonas cubiertas por sedimentos finos (arcilla, arena, hojarasca y materia orgánica), en las que se desarrolla vegetación acuática. En conjunto, esta dinámica genera una elevada heterogeneidad ambiental y una amplia disponibilidad de nichos ecológicos propicios para las distintas etapas del ciclo de vida de los peces.
Los relevamientos fueron realizados en un tramo de 2,5 km que transcurre por la Reserva Municipal. El cauce se caracteriza por el sustrato basáltico con pozas, correderas y saltos. El salto principal se sitúa frente a una gran gruta basáltica originando una depresión denominada localmente “Olla”, en ella se concentran las actividades recreativas de los visitantes. Aguas abajo de este salto, el cauce presenta sustrato de grava más fina y arcilla, producto del aporte de materiales provenientes del sistema terrestre y finalmente desemboca en el río Paraná.
El río Paraná presenta variaciones hidrométricas atribuibles a la regulación ejercida por represas hidroeléctricas emplazadas aguas arriba de la desembocadura del arroyo Tres de Mayo. Estas fluctuaciones, influyen directamente sobre el escurrimiento del agua desde el arroyo hacia el río y afecta tanto la estructura del hábitat como los procesos ecológicos en la zona de confluencia (Baigún 2018).
Cuatro campañas de pesca experimental fueron realizadas estacionalmente entre marzo de 2022 y marzo de 2023. Como artes de pesca fueron utilizadas redes de espera monofilamento de 2,5; 3; 4 y 5 cm entre nudos opuestos y de acuerdo a la estructura física de los ambientes, una red de arrastre o un copo en zonas de menor profundidad con vegetación flotante y palustre. Las redes permanecieron caladas durante 24 horas e inspeccionadas a intervalos de 8 horas en cada uno de los cuatro puntos de muestreos: punto 1. Aguas arriba del salto Tres de Mayo (26°45'32.98"S - 54°55'24.33"O), punto 2. Aguas abajo del salto, «Olla» (26°45'30.57 "S - 54°55'26.21"O), punto 3. Potamón (26°45'27.36"S - 54°55'44.82"O) y punto 4. Potamón con influencia del río Paraná (26°45'36.69"S - 54°56'6.81"O) (Figura 1). Los ejemplares capturados fueron identificados en campo a nivel de especie y devueltos al agua. Algunos individuos fueron eutanasiados con solución de benzocaína (American Veterinary Medical Association 2001) posteriormente fijados en formol 4% y conservados en alcohol al 70%, cuando la identificación requirió la observación de características microscópicas en condiciones de laboratorio o bien para ser incorporados a la Colección Ictiológica del Laboratorio de Genética Evolutiva (LGEP) del Instituto de Biología Subtropical -IBS- Facultad de Ciencias Exactas Químicas y Naturales. UNaM.
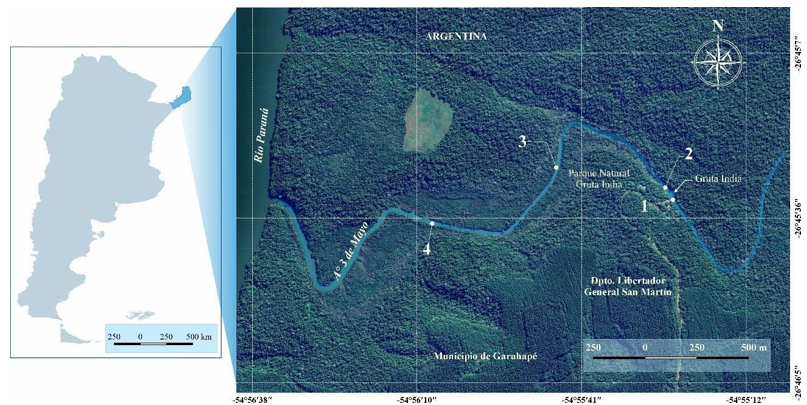
En este trabajo se utiliza la denominación potamón en un sentido ampliado para referirse al sector de menor pendiente del curso de agua, el cual no reúne estrictamente la totalidad de las características clásicamente asociadas a dicho concepto.
El listado de especies, así como su clasificación en órdenes y familias, se elaboró siguiendo la propuesta de Nelson et al. (2016), Reis et al. (2003) y las actualizaciones del clado Characidae a partir de Melo et al. (2024). Asimismo, se consultaron listados de referencia para la ictiofauna de Sudamérica (Reis et al. 2003) y Argentina (Mirande y Koerber 2020, Koerber et al. 2024).
La diversidad alfa fue estimada como número de especies y calculada aplicando el índice de Shannon H´= -Σ Pi + log2 (Pi), donde Pi es la abundancia relativa de cada especie (proporción de individuos de cada especie i en el conjunto total).
La variación en la riqueza de especies de peces entre los sitios de estudio y la completitud del inventario fueron evaluadas mediante el programa EstimateS 9.1.0 (Colwell 2013). Este software genera curvas de acumulación de especies con intervalos de confianza del 95% sin requerir remuestreo, utilizando la función Mao Tau. La determinación del estado del inventario de peces fue realizada mediante los estimadores no paramétricos de riqueza Chao 2 y Jackknife 1, adecuados para estudios en arroyos con hábitats heterogéneos y especies distribuidas de manera heterogénea.
Las curvas de rango-abundancia fueron usadas para comparar la estructura de las comunidades de los ambientes estudiados. Para graficar la curva de rango-abundancia se calculó el logaritmo (base 10) de la proporción de cada especie pi (ni / N) y estos datos se ordenaron desde la especie más abundante a la menos abundante (Feinsinger 2001).
Considerando el peso que otorga a las especies de menor abundancia, se aplicó el Coeficiente de Similitud Cuantitativo de Sørensen para el análisis de la similitud entre los puntos de muestreo. La fórmula fue: Cs = 2C / (A + B), donde C es la suma del valor mínimo de la abundancia de las especies comunes entre las comunidades comparadas, y A y B son las abundancias totales de todas las especies en cada muestra.
La estimación del Índice de Dominancia Comunitaria (IDC) de McNaughton, se realizó según la fórmula IDC = [(Y1 + Y2) / Y] × 100, donde Y1 y Y2 son las abundancias de las dos especies dominantes, y Y la abundancia total de todas las especies.
La constancia específica fue calculada como medida de la frecuencia de aparición de una especie, usando la fórmula: C = (x / n) × 100, donde x es el número de muestras en que aparece la especie y n el número total de muestras. Las especies fueron clasificadas según las categorías propuestas por Lasso (2001): C1: raras o accidentales (C < 25%), C2: comunes o accesorias (25% < C < 50%), C3: comunes o abundantes (C > 50%).
El estado de conservación de las especies fue examinado en base a datos de la Lista Roja de la Unión Internacional para la Conservación de la Naturaleza (UICN 2024), el registro de especies endémicas de Araya et al. (2021) y las actualizaciones de Koerber et al. (2024).
En los sistemas lóticos, como el analizado en este estudio, la producción primaria in situ es relativamente baja, por lo que las comunidades que se desarrollan son predominantemente heterotróficas y dependen en gran medida del aporte de materia orgánica proveniente de la vegetación riparia (Vannote et al. 1980).
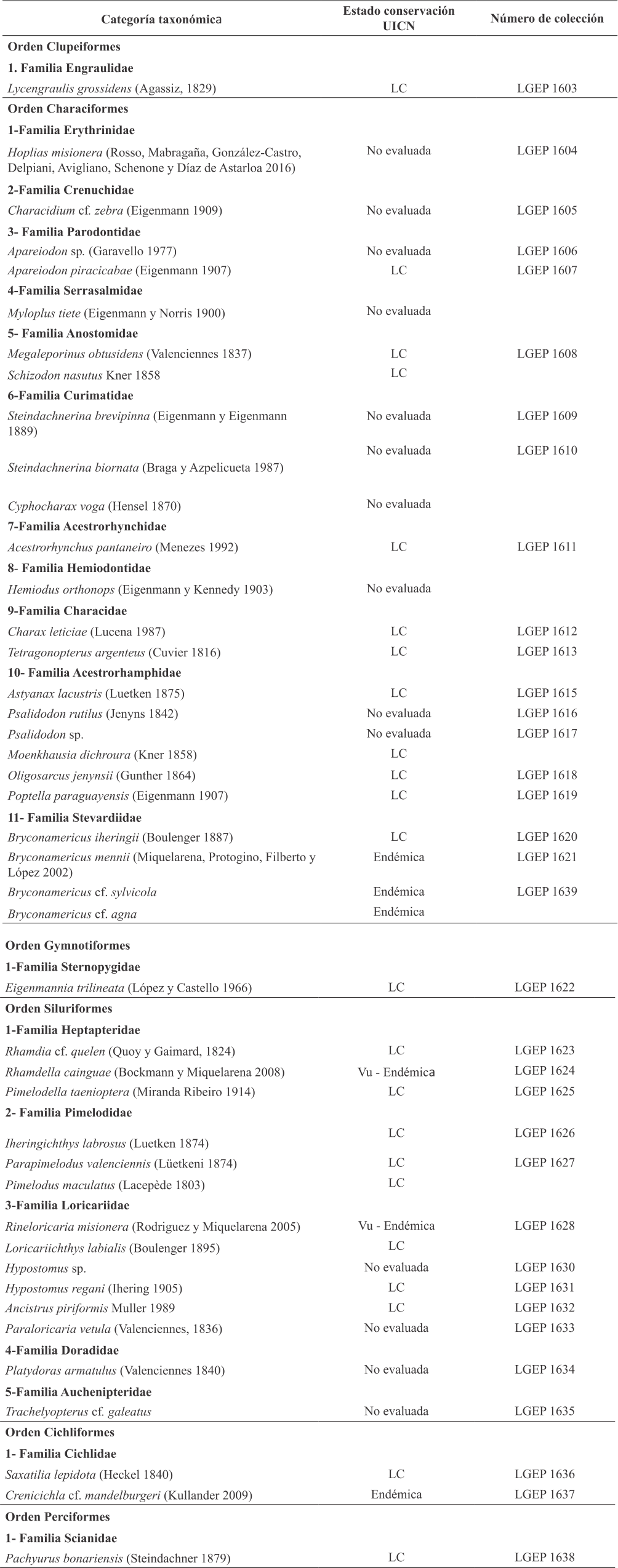
La característica de alta diversidad íctica que distingue a los cursos de agua de la provincia de Misiones (López et al. 2005) también fue hallada en el arroyo Tres de Mayo. Fueron capturados 384 individuos e identificadas 43 especies pertenecientes a seis Órdenes (Tabla 1) de los cuales Characiformes y Siluriformes incluyen el 90% de las especies reconocidas. La elevada representatividad de estos órdenes es una característica de la fauna íctica de la región Neotropical (Albert et al. 2020). Autores como Flores et al. (2020), Fagundes et al. (2015) y Copatti y Copatti (2011) entre otros, han reportado resultados similares en tributarios de los ríos Uruguay y Paraná.
El índice de Shannon fue de H´: 3, lo cual indica alta diversidad al igual que en otros arroyos de la Provincia de Misiones, afluentes del río Paraná, tal como el arroyo Garupá con 3,28 bits de diversidad (Flores et al. 2009).
La curva de acumulación de especies registradas no presenta un comportamiento asintótico, y los estimadores no paramétricos de diversidad (Chao 2 y Jackknife 1) corroboran esta observación al indicar que aún quedan especies por registrar para completar el inventario del arroyo Tres de Mayo (Figura 2). No obstante, el esfuerzo de muestreo realizado permite contar con una estimación sólida de la riqueza específica, alcanzado un 67% de representatividad. Este tipo de inventarios incompletos han sido reportadas previamente en cursos fluviales de Brasil (Copatti y Copatti 2011) y en Misiones, Argentina (Araya 2017).
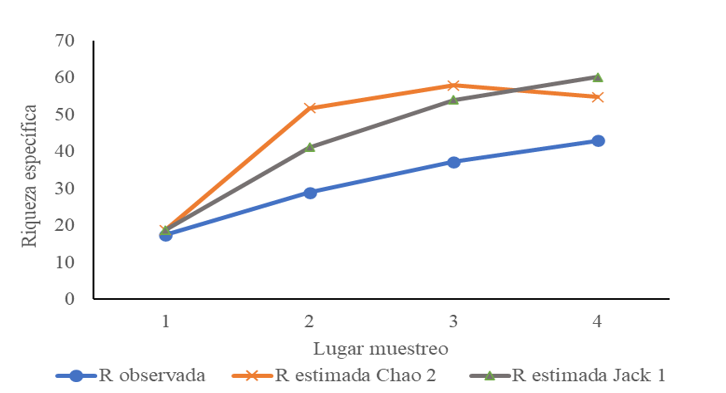
La composición específica de la captura total se concentró en especies como Apareiodon sp. (16%) y Bryconamericus mennii (15%), Steindachnerina brevipinna, S. biornata, A. piracicabae, Astyanax lacustris, Ancistrus piriformis, B. cf. sylvicola, Crenicichla lepidota y C. cf. Mandelburgeri, que representaron el 72% de los individuos registrados, el 28% restante reunió ejemplares pertenecientes a 33 especies cuya abundancia relativa fue menor a 2%.
La baja proporción de especies con abundancia elevada es un patrón observado en una amplia variedad de grupos taxonómicos, incluidos los peces (Magurran et al. 2011). Durante el desarrollo de los muestreos se identificaron 19 especies con 0,25% de abundancia relativa, valor que corresponde a un individuo por cada una.
La estructura de la comunidad de peces, evaluada a partir de la abundancia relativa de las especies registradas, se ajustó a un modelo de distribución log-normal exclusivamente en la zona potámica del arroyo (Figura 3), con la mayor riqueza específica (33 especies) y abundancia (164 individuos). En contraste, en las restantes zonas muestreadas, la estructura comunitaria se correspondió con una distribución de tipo logarítmica, caracterizada por la dominancia de pocas especies y una elevada proporción de especies raras. En la Figura 3 se indican las dos especies más abundantes por lugar de muestreo.
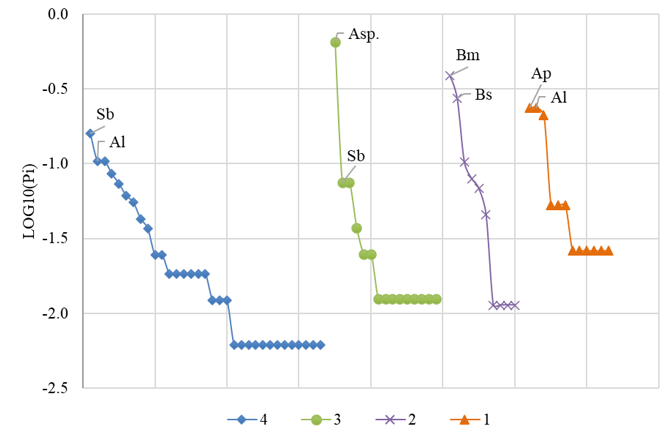
Diversos factores se relacionan con la estructura y composición de las comunidades de peces, entre ellos los gradientes latitudinales, la heterogeneidad del hábitat, factores físicos y químicos del agua, las actividades humanas como los asentamientos, la sobrepesca y la conectividad lateral con ambientes relacionados con el desove o las primeras etapas del desarrollo (Stoffers et al. 2022). El ensamble de peces del arroyo Tres de Mayo, al igual que en otros afluentes a los grandes ríos, está compuesto fundamentalmente por especies de pequeño porte, generalmente de menos de 15 cm de longitud total. Estas especies se caracterizan por la distribución geográfica restringida, escaso o nulo valor comercial y alta dependencia de la vegetación ripariana para su alimentación, abrigo y reproducción (Lowe-McConnell 1999). En este estudio fueron registradas 13 especies de las familias Characidae, Stevardiidae y Acestrorhomphidae, todas de pequeño porte pertenecientes a los géneros Tetragonopterus, Charax, Bryconamericus, Moenkhausia, Poptella, Astyanax y Psalidodon valoradas por aficionados al acuarismo. Aproximadamente 1.200 especies componen el grupo comúnmente nombrados como tetras neotropicales (Reis et al. 2003) con amplia distribución desde Costa Rica hasta la Argentina y con gran variedad de hábitos alimentarios y de estrategias de utilización del hábitat (Kavalco y Pazza 2007).
Otro grupo que compone la ictiofauna de los cursos interiores, incluye especies de mediano y gran porte, reofílicas y migradoras frecuentadoras de la región potámica de los arroyos en busca de abrigo, alimento y áreas de reproducción. En el arroyo estudiado, este grupo estuvo representado por especies de mediano porte como Hemiodus orthonops, Megaleporinus obtusidens (boga tres puntos), Pimelodus maculatus (bagre amarillo), Pachyurus bonariensis (corvina de rio), Lycengraulis grossidens (sardina o anchoa de río), especies muy frecuentes en el río Paraná. El río es la vía de conexión entre la biota de los arroyos y es favorecida por los pulsos recurrentes de crecientes y bajantes (Neiff 1996), estos eventos impulsan la migración y reproducción de los peces. Esta dinámica de pulsos podría contribuir al desplazamiento y arrastre de los peces desde el río al arroyo y viceversa, incluso hasta aquellos de poca o nula movilidad. Este proceso genera mayor diversidad tanto ecológica como morfológica en los primeros kilómetros influenciados por el río Paraná, debido a que en estos ambientes los peces encuentran los factores necesarios para satisfacer sus necesidades de refugio, alimentación y desove (Stoffels et al. 2022).
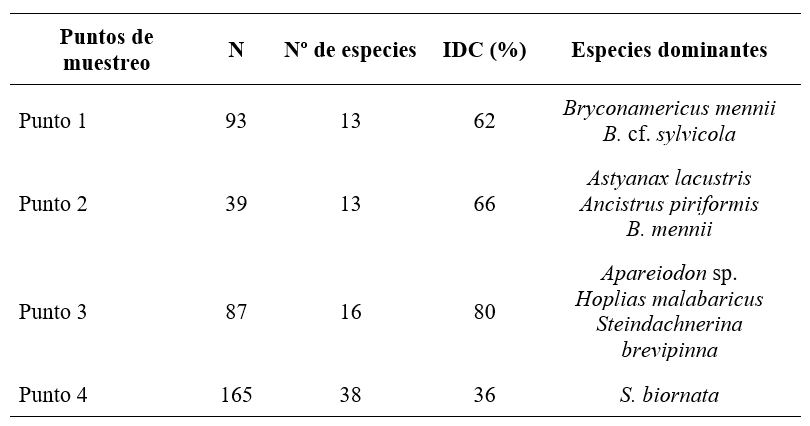
El análisis espacial de la comunidad íctica mostró una similaridad de baja a moderada entre los cuatro puntos de muestreo (20-32%). A. pantaneiro y A. piriformis fueron las dos especies registradas en los cuatro sitios de muestreo. La mayor similitud se observó entre los puntos adyacentes al salto «Olla», probablemente debido a la dominancia de especies pequeñas de los géneros Astyanax y Bryconamericus (Tabla 2). Estas especies encuentran en ambientes de pozas y correderas, los espacios adecuados para la alimentación, protección, reproducción y el desarrollo de todas las etapas de sus ciclos de vida.
Las especies del género Astyanax, ampliamente distribuidas en la región Neotropical y caracterizadas por una elevada diversidad y marcada plasticidad fenotípica, incluyendo taxones endémicos con adaptaciones a condiciones ambientales específicas, constituyen modelos particularmente útiles para el análisis de procesos biogeográficos y evolutivos asociados a la historia geológica de los sistemas fluviales (Calcagnotto et al. 2005). En este contexto, el registro exclusivo de las especies endémicas B. cf. agna y R. misionera catalogada como vulnerable (Araya et al. 2021) en el sitio localizado aguas arriba del salto Tres de Mayo sugiere que esta discontinuidad geomorfológica podría actuar como una barrera natural a la dispersión, favoreciendo procesos de aislamiento poblacional y endemismo. Estos resultados refuerzan la relevancia biogeográfica del área y subrayan su importancia para la conservación de la ictiofauna regional, en particular de especies con distribución restringida y elevado valor de conservación.
La región potámica del arroyo con influencia del río Paraná, se caracterizó por la presencia de especies de mediano a mayor porte, como M. obtusidens, Myloplus tiete y P. maculatus. En el punto 3, fue más elevado el índice de dominancia comunitaria, podría atribuirse a la marcada abundancia de Apareiodon sp., asociada a la presencia de un gran cardumen. Cardúmenes de especies de este género han sido observados en relación con correntadas en canales de desborde durante las crecidas del río Paraná en el Predelta (Almirón et al. 2015).
Los resultados de la constancia de ocurrencia indican que 7 especies fueron comunes o abundantes: Acestrorhynchus pantaneiro, B. mennii, A. piriformis, A. lacustris, B. cf. sylvicola, Crenicichla cf. mandelburgeri y Rhamdella cainguae. Se registraron 29 especies raras o accidentales, capturadas únicamente en uno de los muestreos, de las cuales 21 (72%) corresponden a puntos de muestreo influenciados por el régimen hidrológico del río Paraná. Este hecho resalta la importancia de los afluentes y los ciclos de inundación en el ciclo de vida de los peces, y a su vez podría explicar la elevada diversidad observada, atribuida a la adición de especies como resultado del aumento del nivel del agua.
Estado de conservación de la ictiofauna. La diversidad acuática se encuentra amenazada por el uso del recurso y en la provincia de Misiones uno de sus principales problemas es la escasa protección. Araya et al. (2021) afirman que más de la mitad de los arroyos (36) con especies de peces endémicas carecen de protección y muchos presentan alteraciones como destrucción de la vegetación marginal, represamientos, polución e introducción de especies exóticas. Estas características muestran las deficiencias de los sistemas actuales de áreas protegidas de Misiones respecto a la protección de sus ecosistemas acuáticos y en consecuencia la falta de consideración de los mismos en la toma de decisiones y diseño de áreas de conservación. En el tramo estudiado fueron registradas 22 especies en estado de preocupación menor es decir abundantes y de amplia distribución, dos especies vulnerable (R. cainguae y Rineloricaria misionera) con riesgos de extinción en estado de vida silvestre ya sea por disminución de la población o por la forma de distribución de la misma y 6 especies sin evaluar en relación a los criterios UICN (2024). Fueron reconocidas 6 especies endémicas o de distribución restringida en la provincia de Misiones y la Región de Brasil y Paraguay situación que las ubica en estado de vulnerabilidad (Tabla 1).
Frente a la pérdida de biodiversidad y como respuesta a la necesidad de conservación, una de las principales estrategias globales reconocidas por el Convenio sobre Diversidad Biológica, ha sido la creación de Áreas Protegidas que consideren las características naturales relevantes de los territorios. En la actualidad la visión sobre la conservación de los recursos naturales considera de manera interdisciplinaria, las dimensiones biofísicas y sociales con un enfoque que integra protección y manejo de la biodiversidad permitiendo que conservación biológica y bienestar social sean opciones complementarias.
La alta diversidad registrada y la presencia de especies endémicas, resalta el valor ecológico del ecosistema acuático del arroyo Tres de Mayo en el sector estudiado. La composición y diversidad observadas evidencian un sistema con alta integridad ecológica y una estructura biológica compleja,
El registro de seis especies endémicas, entre ellas R. cainguae y R. misionera clasificadas como Vulnerable según las categorías y criterios de la Lista Roja de la UICN, lo que indica que el arroyo funciona como un refugio clave para la ictiofauna endémica y amenazada, donde la presencia de barreras naturales, como los saltos, condiciona la conectividad longitudinal, favoreciendo procesos de aislamiento y diferenciación de las comunidades ícticas. Este contexto resalta el alto valor ecológico del sistema y la necesidad de implementar estrategias de conservación específicas, a escala de cuenca, que consideren la conectividad fluvial, la protección de los tramos críticos y el mantenimiento de los procesos ecológicos naturales, en concordancia con la normativa ambiental vigente en la provincia de Misiones.
Este trabajo contribuye no sólo a documentar la diversidad presente, sino también a la generación de información clave para el diseño de protocolos de manejo adaptativo en futuros programas de conservación.
Agradecimientos. A la FCEQyN y Municipalidad de Garuhapé por la firma del convenio de colaboración que permitió llevar a cabo la presente investigación. Especial reconocimiento al Guardaparque Rodrigo Martínez Gamba, por sus aportes y acompañamiento en el trabajo de campo. Al Dr. Jorge Casciotta y Dra. Adriana Almirón por contribuir en despejar dudas sobre la identificación taxonómica de peces.
Contribución de los autores. AP, FS, BA y MS: realización de los muestreos de campo, procesamiento de muestras e identificación taxonómica y redacción del artículo en colaboración de todos los autores. CK: contribuyó al muestreo y colaboró en procesamientos de muestras.
Declaración de conflictos de intereses. Los autores declaran no tener conflictos de intereses financieros ni relaciones personales conocidas que pudieran haber influido en el trabajo presentado en este artículo.
Disponibilidad de datos. Los datos estarán disponibles previa solicitud.